1 . 保护环境人人有责。下列有关化学与环境的说法不正确的是
| A.向燃煤中加入生石灰可以减少酸雨的形成 |
| B.汽车尾气排放的氮氧化物是汽油不完全燃烧造成的 |
| C.塑料在自然环境下不易分解,会造成“白色污染” |
| D.绿色化学的核心是利用化学原理和技术手段从源头上减少或消除环境污染 |
您最近一年使用:0次
解题方法
2 . 某实验小组同学用铜与浓硫酸反应制取SO2,验证SO2性质并制备NaHSO3,设计如图所示实验装置。
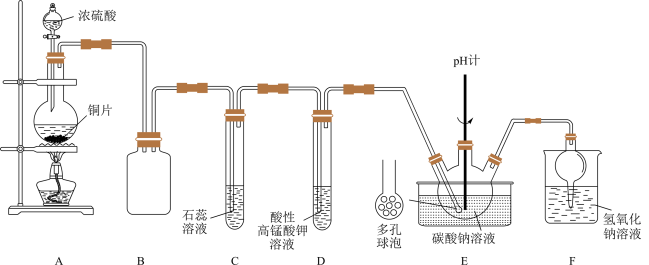
回答下列问题:
(1)C中的实验现象是_____ ,F的作用是_____ 。
(2)A中发生反应的化学方程式是_____ 。
(3)试管D中发生反应的离子方程式为_____ 。
(4)装置E中设计多孔球泡的目的是_____ 。
(5)向装置E中通入SO2可制得NaHSO3.已知:Na2SO3水溶液中H2SO3、HSO 、SO
、SO 随pH的分布如图1所示,Na2SO4的溶解度曲线如图2所示。
随pH的分布如图1所示,Na2SO4的溶解度曲线如图2所示。

①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定何时停止通入SO2的实验操作为_____ 。
②请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案:边搅拌边向NaHSO3溶液中滴加NaOH溶液,测量溶液pH,pH约为_____ 时,停止滴加NaOH溶液,加热浓缩溶液至有大量晶体析出,在高于_____ ℃条件下趁热过滤,用少量无水乙醇洗涤,干燥,密封包装。

回答下列问题:
(1)C中的实验现象是
(2)A中发生反应的化学方程式是
(3)试管D中发生反应的离子方程式为
(4)装置E中设计多孔球泡的目的是
(5)向装置E中通入SO2可制得NaHSO3.已知:Na2SO3水溶液中H2SO3、HSO
 、SO
、SO 随pH的分布如图1所示,Na2SO4的溶解度曲线如图2所示。
随pH的分布如图1所示,Na2SO4的溶解度曲线如图2所示。
①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。实验中确定何时停止通入SO2的实验操作为
②请补充完整由NaHSO3溶液制备无水Na2SO3的实验方案:边搅拌边向NaHSO3溶液中滴加NaOH溶液,测量溶液pH,pH约为
您最近一年使用:0次
3 . 下列有关单质硫的说法中,正确的是
| A.硫是一种黄色晶体,质脆,微溶于CS2 |
| B.硫位于元素周期表的第三周期第VA族 |
| C.硫与铁反应生成FeS,与铜反应生成Cu2S |
| D.单质硫燃烧时,氧气少量时生成SO2,氧气足量时可生成SO3 |
您最近一年使用:0次
解题方法
4 . “绿色化学”是利用化学原理和技术手段,减少或消除产品在生产和应用中涉及的有害化学物质,实现从源头减少或消除环境污染。下列化学反应最符合“绿色化学”理念的是
A. |
B. |
C. |
D. |
您最近一年使用:0次
解题方法
5 . 化学与社会,生产、生活密切相关。下列说法正确的是
| A.为了治理酸雨污染,政府应关闭硫酸厂、火电厂,水泥厂等 |
| B.废旧电池中含有镍、镉等重金属,可用填埋法处理 |
| C.减少燃煤的使用,改用风能、太阳能等新能源符合“低碳生活”理念 |
| D.酸雨样品久置过程中pH减小是因为溶解了更多的CO |
您最近一年使用:0次
名校
6 . 设 为阿伏伽德罗常数的值。下列说法正确的是
为阿伏伽德罗常数的值。下列说法正确的是
 为阿伏伽德罗常数的值。下列说法正确的是
为阿伏伽德罗常数的值。下列说法正确的是A. 分子中所含的 分子中所含的 数目为 数目为 |
B.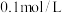 的 的 溶液中所含的 溶液中所含的 数目为 数目为 |
C. 与足量 与足量 充分反应,转移电子数为 充分反应,转移电子数为 |
D.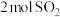 与足量 与足量 反应,生成的 反应,生成的 分子数小于 分子数小于 |
您最近一年使用:0次
2023-07-09更新
|
315次组卷
|
3卷引用:广西玉林市博白县中学2023-2024学年高三上学期开学考试化学试题
解题方法
7 . 用如图所示装置进行铜与浓硫酸的反应,并探究其产物及产物的性质(夹持装置已略去)。

(1)试管①中发生反应的化学方程式是___________ , 此反应中浓硫酸显_____ 性。
(2)若试管②中的试剂为品红溶液,其作用有两个,分别是________________ 。
(3)若试管②中的试剂为酸性KMnO4溶液,实验时,观察到溶液褪色,则说明生成的气体具有_____ 性,该反应的离子方程式是___________ 。
(4)若试管②中的试剂为硫化氢水溶液,实验现象是______________ 。
(5)试管③中试剂的作用是___________ 。

(1)试管①中发生反应的化学方程式是
(2)若试管②中的试剂为品红溶液,其作用有两个,分别是
(3)若试管②中的试剂为酸性KMnO4溶液,实验时,观察到溶液褪色,则说明生成的气体具有
(4)若试管②中的试剂为硫化氢水溶液,实验现象是
(5)试管③中试剂的作用是
您最近一年使用:0次
解题方法
8 . 实验室制备下列气体的方法可行的是
| 气体 | 方法 | |
| A |  | 加热氯化铵固体 |
| B |  | 将铜加入浓硝酸 |
| C |  | 亚硫酸钠固体与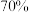 浓硫酸 浓硫酸 |
| D |  | 硫化亚铁与浓硫酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
9 . 下列指定反应的离子方程式正确的是
A. 与水反应: 与水反应: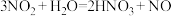 |
B.将少量 通入过量冷氨水中: 通入过量冷氨水中: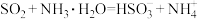 |
C. 与 与 按1∶1通入水中: 按1∶1通入水中: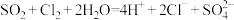 |
D.向 溶液中加入过量的 溶液中加入过量的 溶液并加热: 溶液并加热: |
您最近一年使用:0次
10 . 唐朝初年,瘟疫频发,人们把它归因于一种叫“年”的怪兽。一位叫李田的人就把硝石、硫磺和木炭装在竹筒里,点燃后驱赶怪兽。后来人们靠此驱散了山林瘴气,战胜了疫情。中国古代四大发明之一的“黑火药”是由“一硫二硝三木炭”混合而成。
(1)写出“黑火药”爆炸的化学反应方程式___________ 。
(2)“黑火药”爆炸时,空气中还弥漫着一层淡淡的刺鼻的 气体,它能在一定程度上,杀灭空气中的细菌。日常生产生活中,产生该气体的主要途径是
气体,它能在一定程度上,杀灭空气中的细菌。日常生产生活中,产生该气体的主要途径是___________ (用文字表述,任写一条合理途径)。
(3)某同学将足量的 通入一支装有氯化钡溶液的试管,未见沉淀生成。若向该试管中加入足量___________(填序号),能产生白色沉淀。
通入一支装有氯化钡溶液的试管,未见沉淀生成。若向该试管中加入足量___________(填序号),能产生白色沉淀。
(4)古代曾用硝土[含有 、少量NaCl等]和草木灰(含有
、少量NaCl等]和草木灰(含有 )作原料制取
)作原料制取 。某化学兴趣小组设计了如下实验流程:
。某化学兴趣小组设计了如下实验流程:

①“反应”过程中的离子反应方程式为___________ 。
②如图所示是硝酸钾和氯化钠的溶解度曲线。“一系列操作”包括将滤液___________ 、过滤洗涤、干燥等步骤。

(5)现代国防开矿等使用的烈性炸药,主要成分为硝化甘油 (
(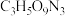 ),它是一种白色或淡黄色黏稠液体,低温易冻结。熔点13℃,沸点218℃(170℃以上会发生爆炸)。
),它是一种白色或淡黄色黏稠液体,低温易冻结。熔点13℃,沸点218℃(170℃以上会发生爆炸)。
①硝化甘油在人体内能缓慢分解出一种双原子明星分子,其相对分子量是30,少量的该分子在人体内会促进血管扩张,防止血管栓塞,因此,被广泛用于治疗心绞痛,该明星分子的化学式为___________ ;
②实验室制备硝化甘油的化学方程式为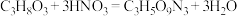 ,用足量浓硝酸、浓硫酸和
,用足量浓硝酸、浓硫酸和 mL
mL  g/cm
g/cm 甘油混合加热到85℃以上,即得到硝化甘油,制备装置如图所示。该装置中仪器a名称为
甘油混合加热到85℃以上,即得到硝化甘油,制备装置如图所示。该装置中仪器a名称为___________ 。

③反应得到16g硝化甘油,则产率为___________ (保留整数)。
(1)写出“黑火药”爆炸的化学反应方程式
(2)“黑火药”爆炸时,空气中还弥漫着一层淡淡的刺鼻的
 气体,它能在一定程度上,杀灭空气中的细菌。日常生产生活中,产生该气体的主要途径是
气体,它能在一定程度上,杀灭空气中的细菌。日常生产生活中,产生该气体的主要途径是(3)某同学将足量的
 通入一支装有氯化钡溶液的试管,未见沉淀生成。若向该试管中加入足量___________(填序号),能产生白色沉淀。
通入一支装有氯化钡溶液的试管,未见沉淀生成。若向该试管中加入足量___________(填序号),能产生白色沉淀。| A.硝酸钾溶液 | B.稀盐酸 | C.氨水 | D.硫化钠溶液 |
 、少量NaCl等]和草木灰(含有
、少量NaCl等]和草木灰(含有 )作原料制取
)作原料制取 。某化学兴趣小组设计了如下实验流程:
。某化学兴趣小组设计了如下实验流程:
①“反应”过程中的离子反应方程式为
②如图所示是硝酸钾和氯化钠的溶解度曲线。“一系列操作”包括将滤液

(5)现代国防开矿等使用的烈性炸药,主要成分为硝化甘油
 (
(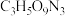 ),它是一种白色或淡黄色黏稠液体,低温易冻结。熔点13℃,沸点218℃(170℃以上会发生爆炸)。
),它是一种白色或淡黄色黏稠液体,低温易冻结。熔点13℃,沸点218℃(170℃以上会发生爆炸)。①硝化甘油在人体内能缓慢分解出一种双原子明星分子,其相对分子量是30,少量的该分子在人体内会促进血管扩张,防止血管栓塞,因此,被广泛用于治疗心绞痛,该明星分子的化学式为
②实验室制备硝化甘油的化学方程式为
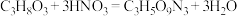 ,用足量浓硝酸、浓硫酸和
,用足量浓硝酸、浓硫酸和 mL
mL  g/cm
g/cm 甘油混合加热到85℃以上,即得到硝化甘油,制备装置如图所示。该装置中仪器a名称为
甘油混合加热到85℃以上,即得到硝化甘油,制备装置如图所示。该装置中仪器a名称为
③反应得到16g硝化甘油,则产率为
您最近一年使用:0次



