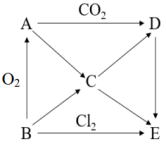
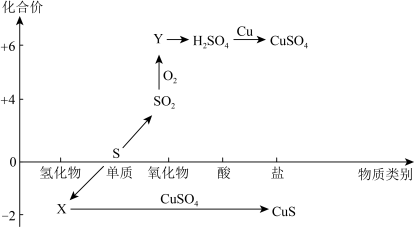
硫及其化合物的“价-类”二维图如下图所示,回答下列问题:___________ ,Y的化学式是___________ 。
(2)检验 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入___________ ,无明显现象,再加入___________ 溶液,若产生白色沉淀,则溶液中含有 。
。
(3)CuS与足量浓硫酸反应也可制得SO2,该反应的化学方程式为:CuS+4H2SO4(浓) CuSO4+4SO2↑+4H2O。
CuSO4+4SO2↑+4H2O。
①请用“双线桥”法标明该反应电子转移的方向和数目___________ 。
②当有1.5NA电子发生转移时,理论上生成SO2的体积(标准状况)为___________ L。
(2)检验
 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入 。
。(3)CuS与足量浓硫酸反应也可制得SO2,该反应的化学方程式为:CuS+4H2SO4(浓)
 CuSO4+4SO2↑+4H2O。
CuSO4+4SO2↑+4H2O。①请用“双线桥”法标明该反应电子转移的方向和数目
②当有1.5NA电子发生转移时,理论上生成SO2的体积(标准状况)为
更新时间:2024-05-06 12:10:44
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
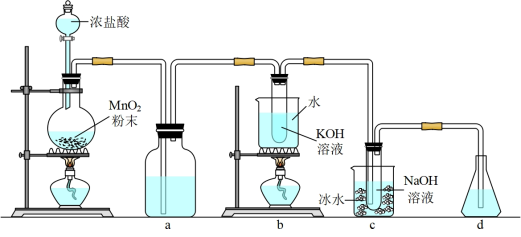
【推荐1】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域.实验室中利用如图装置(部分装置省略)制备KClO3和NaClO,探究其氧化还原性质。
回答下列问题:
(1)a中的试剂为___ 。
(2)b中采用的加热方式是___ ,c中化学反应的离子方程式是___ ,采用冰水浴冷却的目的是___ 。
(3)反应结束后,取出b中试管,经冷却结晶,___ ,___ ,干燥,得到KClO3晶体。
(4)高铁酸钠(Na2FeO4)(其中氧元素是-2价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O。
①用双线桥法在化学方程式中标出电子转移的情况:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O。___
②当反应中有5个FeO 生成时,转移的电子数是
生成时,转移的电子数是___ 个。

回答下列问题:
(1)a中的试剂为
(2)b中采用的加热方式是
(3)反应结束后,取出b中试管,经冷却结晶,
(4)高铁酸钠(Na2FeO4)(其中氧元素是-2价)是一种新型的净水剂,可以通过下述反应制取:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O。
①用双线桥法在化学方程式中标出电子转移的情况:2Fe(OH)3+4NaOH+3NaClO=2Na2FeO4+3NaCl+5H2O。
②当反应中有5个FeO
 生成时,转移的电子数是
生成时,转移的电子数是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如图(部分反应条件及产物略去):
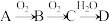
(1)若A在常温下是固体,B是能使品红溶液褪色的有刺激性气味的无色气体:
①D的化学式:___________ ;
②在工业生产中,B气体大量排放,被雨水吸收后形成酸雨,被称为“天堂的眼泪”,会造成水土酸性化、建筑物加速腐蚀等危害。下列说法正确的是___________ 。
A.酸雨不会对动植物产生任何影响
B.使用新型能源不会对酸雨的防治产生效果
C.酸雨指的是pH小于7的雨水
D. 和
和 的过度排放是形成酸雨的主要原因
的过度排放是形成酸雨的主要原因
(2)若A在常温下为气体,C是红棕色气体。
①C的化学式为:___________ ;
②D的浓溶液在常温下可与铜反应并生成C气体,该反应的离子方程式为:___________ ,该反应___________ (填“属于”或“不属于”)氧化还原反应,用双线桥法表示出该反应的电子转移方向和数目:___________ 。
(3)若A是一种金属单质,C是淡黄色固体,写出C生成D的化学方程式___________ 。
(4)若A的水溶液呈碱性,写出A的电子式___________ ,写出A生成B的化学方程式:___________ 。
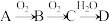
(1)若A在常温下是固体,B是能使品红溶液褪色的有刺激性气味的无色气体:
①D的化学式:
②在工业生产中,B气体大量排放,被雨水吸收后形成酸雨,被称为“天堂的眼泪”,会造成水土酸性化、建筑物加速腐蚀等危害。下列说法正确的是
A.酸雨不会对动植物产生任何影响
B.使用新型能源不会对酸雨的防治产生效果
C.酸雨指的是pH小于7的雨水
D.
 和
和 的过度排放是形成酸雨的主要原因
的过度排放是形成酸雨的主要原因(2)若A在常温下为气体,C是红棕色气体。
①C的化学式为:
②D的浓溶液在常温下可与铜反应并生成C气体,该反应的离子方程式为:
(3)若A是一种金属单质,C是淡黄色固体,写出C生成D的化学方程式
(4)若A的水溶液呈碱性,写出A的电子式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】从钒铬锰矿渣(主要成分为 、
、 、
、 )中提铬的一种工艺流程如下:
)中提铬的一种工艺流程如下: ](在空气中易被氧化.回答下列问题:
](在空气中易被氧化.回答下列问题:
(1)Cr元素位于元素周期表第_______ 周期_______ 族。
(2)用 溶液制备
溶液制备 胶体的化学方程式为
胶体的化学方程式为_______ 。
(3)常温下,各种形态五价钒粒子总浓度的对数[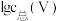 ]与pH关系如图1。已知钒铬锰矿渣硫酸浸液中
]与pH关系如图1。已知钒铬锰矿渣硫酸浸液中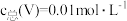 ,“沉钒”过程控制
,“沉钒”过程控制 ,则与胶体共沉降的五价钒粒子的存在形态为
,则与胶体共沉降的五价钒粒子的存在形态为_______ (填化学式)。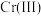 、
、 的沉淀率与pH关系如图2。“沉铬”过程最佳pH为
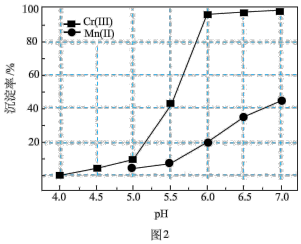
的沉淀率与pH关系如图2。“沉铬”过程最佳pH为_______ ;在该条件下滤液B中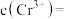
_______  【
【 近似为
近似为 ,
, 的
的 近似为
近似为 】。
】。 的离子方程式为
的离子方程式为_______ 。
(6)“提纯”过程中 的作用为
的作用为_______ 。
 、
、 、
、 )中提铬的一种工艺流程如下:
)中提铬的一种工艺流程如下: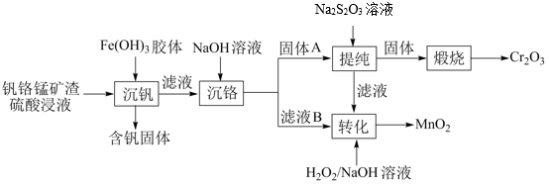
 ](在空气中易被氧化.回答下列问题:
](在空气中易被氧化.回答下列问题:(1)Cr元素位于元素周期表第
(2)用
 溶液制备
溶液制备 胶体的化学方程式为
胶体的化学方程式为(3)常温下,各种形态五价钒粒子总浓度的对数[
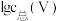 ]与pH关系如图1。已知钒铬锰矿渣硫酸浸液中
]与pH关系如图1。已知钒铬锰矿渣硫酸浸液中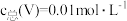 ,“沉钒”过程控制
,“沉钒”过程控制 ,则与胶体共沉降的五价钒粒子的存在形态为
,则与胶体共沉降的五价钒粒子的存在形态为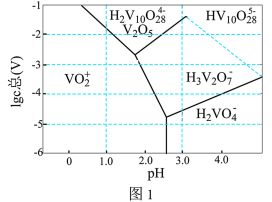
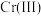 、
、 的沉淀率与pH关系如图2。“沉铬”过程最佳pH为
的沉淀率与pH关系如图2。“沉铬”过程最佳pH为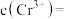
 【
【 近似为
近似为 ,
, 的
的 近似为
近似为 】。
】。
 的离子方程式为
的离子方程式为(6)“提纯”过程中
 的作用为
的作用为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某学习小组用如图装置研究气体X的性质,气体X的主要成分是Cl2,此外还含有少量水蒸气。请回答下列问题:
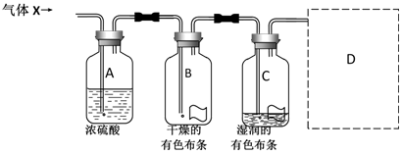
(1)分别描述B、C装置中的现象:干燥的有色布条___ 、湿润的有色布条___ ;结合离子方程式以及物质性质说明B、C装置中现象不同的原因___ 。
(2)Cl2是一种___ 色的有毒气体,为了防止多余Cl2污染空气,应该在D处用如图装置进行尾气处理,用化学方程式表示该原理___ ,气体应该由管___ (填“a”或“b”)通入。若要吸收224 mL Cl2(标况下),至少需要1 mol/L的上述溶液___ mL。

(3)在实际生产中,人们曾用浓氨水(挥发出NH3)来检验氯气管道是否漏气。若管道某处泄漏氯气,就会在该处产生白烟(NH4Cl),同时产生一种可直接排放空气中的气体。完成上述过程中化学反应方程式的配平:NH3+Cl2=NH4Cl+。___

(1)分别描述B、C装置中的现象:干燥的有色布条
(2)Cl2是一种

(3)在实际生产中,人们曾用浓氨水(挥发出NH3)来检验氯气管道是否漏气。若管道某处泄漏氯气,就会在该处产生白烟(NH4Cl),同时产生一种可直接排放空气中的气体。完成上述过程中化学反应方程式的配平:NH3+Cl2=NH4Cl+。
您最近一年使用:0次
【推荐3】为回收利用废镍催化剂(主要成分为NiO,另含Fe2O3、CaO、CuO、BaO等),科研人员研制了一种回收镍和硫酸铜晶体的新工艺。工艺流程如图所示:
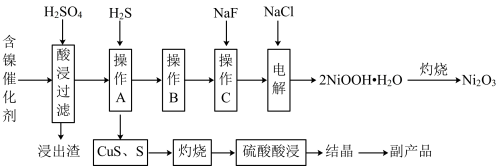
已知:常温下,有关氢氧化物开始沉淀和沉淀完全的pH如下表所示:
请回答下列问题:
(1)加快酸浸速率的常用措施有___________ (任写一条即可)。
(2)“浸出渣”主要成分为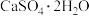 和
和___________ 两种物质。
(3)“操作B”的过程是:先在40~50℃温度下加入 ,其作用是
,其作用是___________ (用离子方程式表示);再调pH至___________ (填pH范围),操作B可除去溶液中的___________ 元素(填元素名称)。
(4)在碱性条件下,电解产生 的原理是:
的原理是: 在阳极被氧化为
在阳极被氧化为 ,
, 再被
再被 氧化产生
氧化产生 沉淀。请写出
沉淀。请写出 被
被 氧化得到
氧化得到 沉淀的离子方程式
沉淀的离子方程式___________ 。
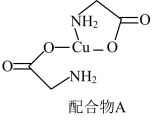
(5)配合物A常用于医药、电镀等方面,其结构如图所示。向硫酸铜溶液中滴入氨基乙酸钠(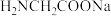 )即可得到它,配合物A中的配位原子的电负性由大到小的顺序是
)即可得到它,配合物A中的配位原子的电负性由大到小的顺序是___________ 。

已知:常温下,有关氢氧化物开始沉淀和沉淀完全的pH如下表所示:
| 氢氧化物 |  |  |  |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
请回答下列问题:
(1)加快酸浸速率的常用措施有
(2)“浸出渣”主要成分为
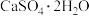 和
和(3)“操作B”的过程是:先在40~50℃温度下加入
 ,其作用是
,其作用是(4)在碱性条件下,电解产生
 的原理是:
的原理是: 在阳极被氧化为
在阳极被氧化为 ,
, 再被
再被 氧化产生
氧化产生 沉淀。请写出
沉淀。请写出 被
被 氧化得到
氧化得到 沉淀的离子方程式
沉淀的离子方程式(5)配合物A常用于医药、电镀等方面,其结构如图所示。向硫酸铜溶液中滴入氨基乙酸钠(
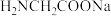 )即可得到它,配合物A中的配位原子的电负性由大到小的顺序是
)即可得到它,配合物A中的配位原子的电负性由大到小的顺序是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】在学习了硫的转化后,某学生绘制了如图转化关系:

(1)写出指定物质的化学式:A___________ ,B___________ ,D___________ 。
(2)写出由铜和浓硫酸制 的化学方程式:
的化学方程式:___________ ,反应中每生成标准状况下22.4L的 ,转移
,转移___________ mol电子。
(3)写出B与 反应的化学方程式:
反应的化学方程式:___________ 。
(4)写出将 与
与 的混合气体通入水中生成
的混合气体通入水中生成 的离子方程式:
的离子方程式:___________ 。
(5)实验室检验溶液中的 所需要的试剂有
所需要的试剂有___________ (填化学式)。

(1)写出指定物质的化学式:A
(2)写出由铜和浓硫酸制
 的化学方程式:
的化学方程式: ,转移
,转移(3)写出B与
 反应的化学方程式:
反应的化学方程式:(4)写出将
 与
与 的混合气体通入水中生成
的混合气体通入水中生成 的离子方程式:
的离子方程式:(5)实验室检验溶液中的
 所需要的试剂有
所需要的试剂有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】研究不同价态硫元素之间的转化是合理利用硫元素的基本途径。
Ⅰ.如图是硫元素的价类二维图及含硫物质相互转化的部分信息。

(1)A的化学式为_______ 。
(2)C有毒,写出实验室用足量的 溶液吸收C的化学方程式
溶液吸收C的化学方程式_______ 。
(3)C→D→E以及C→F→E都是造成酸雨的可能途径,请写出酸雨的一种危害_______ 。
Ⅱ.某小组同学设计实验实现几种价态硫元素的转化。
可选用的实验药品如下:①Na2SO3溶液;②浓硫酸;③ 溶液;④稀硫酸;⑤酸性
溶液;④稀硫酸;⑤酸性 溶液;⑥品红溶液;⑦铜片。
溶液;⑥品红溶液;⑦铜片。
(4)实验ⅰ选择的试剂是_______ (填序号),证明实现转化的现象是_______ ,该转化利用了 的
的_______ 性。
(5)实验ⅱ实现了 价和
价和 价S向0价S的转化,写出该转化反应的离子方程式
价S向0价S的转化,写出该转化反应的离子方程式_______ 。每生成 硫单质,转移的电子数为
硫单质,转移的电子数为_______  。
。
(6)实验ⅲ中发生反应的化学方程式是_______ ,证明实现该转化的现象是_______ 。
Ⅰ.如图是硫元素的价类二维图及含硫物质相互转化的部分信息。

(1)A的化学式为
(2)C有毒,写出实验室用足量的
 溶液吸收C的化学方程式
溶液吸收C的化学方程式(3)C→D→E以及C→F→E都是造成酸雨的可能途径,请写出酸雨的一种危害
Ⅱ.某小组同学设计实验实现几种价态硫元素的转化。
可选用的实验药品如下:①Na2SO3溶液;②浓硫酸;③
 溶液;④稀硫酸;⑤酸性
溶液;④稀硫酸;⑤酸性 溶液;⑥品红溶液;⑦铜片。
溶液;⑥品红溶液;⑦铜片。| 实验序号 | 预期转化 | 选择试剂 | 证明实现转化的现象 |
| ⅰ |  → → | ||
| ⅱ | ①、③、④ | 淡黄色沉淀 | |
| ⅲ |  → → | ②、⑦、⑥ |
 的
的(5)实验ⅱ实现了
 价和
价和 价S向0价S的转化,写出该转化反应的离子方程式
价S向0价S的转化,写出该转化反应的离子方程式 硫单质,转移的电子数为
硫单质,转移的电子数为 。
。(6)实验ⅲ中发生反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】在下图所示的物质转化关系中,A是常见的气态氢化物,B在空气中含量为21%,能使带火星的木条复燃,C、D是造成大气污染的主要物质,E为最高价含氧酸,G是一种紫红色金属单质,(反应条件和部分生成物未列出)。满足条件的A、C、D、E有两组物质,对应所含相异元素为X和Y,B物质所含元素为Z,X、Y、Z中X的原子序号最小。
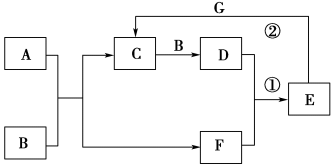
(1)用方框里面标出元素符号和原子序号的形式,画出X、Y、Z在周期表中的位置关系图___________ ,题中图示变化过程中,X元素化合价由低到高依次为__________ 、Y元素化合价由低到高依次为________ ,可以发现X、Y在一些性质上具有________ 性。
(2)请写出Y元素对应物质发生反应①的化学方程式,X元素对应物质发生反应②时X的浓度为(填:浓或稀):____________ 、__________ 。

(1)用方框里面标出元素符号和原子序号的形式,画出X、Y、Z在周期表中的位置关系图
(2)请写出Y元素对应物质发生反应①的化学方程式,X元素对应物质发生反应②时X的浓度为(填:浓或稀):
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】 常用于军事上生产绿色信号弹、曳光弹等。某生产
常用于军事上生产绿色信号弹、曳光弹等。某生产 的化工厂生产排出大量的钡泥(主要含有
的化工厂生产排出大量的钡泥(主要含有 、
、 、
、 等,该厂利用钡泥制取
等,该厂利用钡泥制取 晶体(不含结晶水),部分工艺流程如下:
晶体(不含结晶水),部分工艺流程如下:

已知: 时,可使
时,可使 沉淀完全。请回答下列问题:
沉淀完全。请回答下列问题:
(1)该厂结合本厂实际,化合物X最好 选用_______。
(2)酸溶时, 与稀
与稀 反应的离子方程式为
反应的离子方程式为_______ 。
(3)滤渣2的成分是_______ 。
(4)①反应Ⅰ需调节溶液pH值范围在4~5,目的是_______ 。
②验证该步骤中沉淀已完全 的实验操作是_______ 。
(5)测定所得 晶体的纯度:准确称取w克晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量其质量为m克,则该晶体的纯度为
晶体的纯度:准确称取w克晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量其质量为m克,则该晶体的纯度为_______ 。(提示: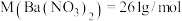 ,
, )
)
 常用于军事上生产绿色信号弹、曳光弹等。某生产
常用于军事上生产绿色信号弹、曳光弹等。某生产 的化工厂生产排出大量的钡泥(主要含有
的化工厂生产排出大量的钡泥(主要含有 、
、 、
、 等,该厂利用钡泥制取
等,该厂利用钡泥制取 晶体(不含结晶水),部分工艺流程如下:
晶体(不含结晶水),部分工艺流程如下:
已知:
 时,可使
时,可使 沉淀完全。请回答下列问题:
沉淀完全。请回答下列问题:(1)该厂结合本厂实际,化合物X
A. | B. | C. | D. |
 与稀
与稀 反应的离子方程式为
反应的离子方程式为(3)滤渣2的成分是
(4)①反应Ⅰ需调节溶液pH值范围在4~5,目的是
②验证该步骤中
(5)测定所得
 晶体的纯度:准确称取w克晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量其质量为m克,则该晶体的纯度为
晶体的纯度:准确称取w克晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量其质量为m克,则该晶体的纯度为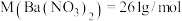 ,
, )
)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】硫代硫酸钠晶体( ,
,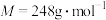 )可用作定影剂、还原剂。
)可用作定影剂、还原剂。
(1)已知: ,
,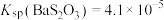 ,
, 。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
限选试剂:稀盐酸、稀 、
、 溶液、
溶液、 溶液、
溶液、 溶液
溶液
(2)利用 标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
①溶液配制:称取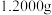 某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在
某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在_______ 中溶解,完全溶解后,全部转移至 的
的_______ 中,加蒸馏水至_______ .
②滴定:取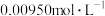 的
的 标准溶液
标准溶液 ,硫酸酸化后加入过量
,硫酸酸化后加入过量 ,发生反应
,发生反应 。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:
。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应: 。加入淀粉溶液作为指示剂,继续滴定,当溶液
。加入淀粉溶液作为指示剂,继续滴定,当溶液_______ ,即为终点。平行滴定3次,样品溶液的平均用量为 ,则样品纯度为
,则样品纯度为_______ %(保留1位小数)。
 ,
,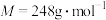 )可用作定影剂、还原剂。
)可用作定影剂、还原剂。(1)已知:
 ,
,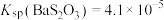 ,
, 。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:
。市售硫代硫酸钠中常含有硫酸根杂质,选用下列试剂设计实验方案进行检验:限选试剂:稀盐酸、稀
 、
、 溶液、
溶液、 溶液、
溶液、 溶液
溶液| 实验步骤 | 现象 |
| ①取少量样品,加入除氧蒸馏水 | ②固体完全溶解得无色澄清溶液 |
| ③ | ④ |
| ⑤静置, |
 标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:
标准溶液定量测定硫代硫酸钠的纯度。测定步骤如下:①溶液配制:称取
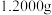 某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在
某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水在 的
的②滴定:取
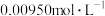 的
的 标准溶液
标准溶液 ,硫酸酸化后加入过量
,硫酸酸化后加入过量 ,发生反应
,发生反应 。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:
。然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应: 。加入淀粉溶液作为指示剂,继续滴定,当溶液
。加入淀粉溶液作为指示剂,继续滴定,当溶液 ,则样品纯度为
,则样品纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某研究小组为研究不同价态含硫物质的转化,设计实验如下,请回答有关问题。
[实验方案]按下图装置进行实验:
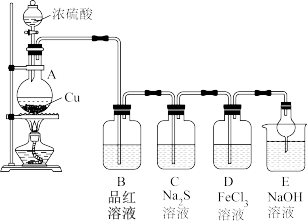
[问题讨论]
(1)A中反应的化学方程式_______ 。
(2)C中出现淡黄色沉淀,反应中Na2S作_______ (填“氧化剂”或“还原剂”)。
(3)若D中有SO 生成,则可说明硫元素的化合价由+4价转化为+6价,检验D中有SO
生成,则可说明硫元素的化合价由+4价转化为+6价,检验D中有SO 生成的方法是:取少量D中反应后的溶液于试管中,
生成的方法是:取少量D中反应后的溶液于试管中,_______ 。写出D中发生反应的离子方程式_______ ,D中FeCl3试剂也可用_______ (填序号)代替。
a.NaCl溶液 b.酸性KMnO4溶液 c.溴水 d.BaCl2溶液
(4)E中溶液的作用是(用离子方程式表示)_______ 。
[实验方案]按下图装置进行实验:

[问题讨论]
(1)A中反应的化学方程式
(2)C中出现淡黄色沉淀,反应中Na2S作
(3)若D中有SO
 生成,则可说明硫元素的化合价由+4价转化为+6价,检验D中有SO
生成,则可说明硫元素的化合价由+4价转化为+6价,检验D中有SO 生成的方法是:取少量D中反应后的溶液于试管中,
生成的方法是:取少量D中反应后的溶液于试管中,a.NaCl溶液 b.酸性KMnO4溶液 c.溴水 d.BaCl2溶液
(4)E中溶液的作用是(用离子方程式表示)
您最近一年使用:0次