名校
1 . 下列叙述正确的是
①冰中存在极性共价键和氢键两种化学键的作用
②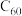 晶体中一个分子周围有12个紧邻分子
晶体中一个分子周围有12个紧邻分子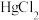 不导电,
不导电,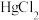 的稀溶液有弱的导电能力且可作手术刀的消毒液。从不同角度分类,
的稀溶液有弱的导电能力且可作手术刀的消毒液。从不同角度分类,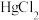 是一种共价化合物、非电解质、盐、分子晶体
是一种共价化合物、非电解质、盐、分子晶体
①冰中存在极性共价键和氢键两种化学键的作用
②
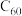 晶体中一个分子周围有12个紧邻分子
晶体中一个分子周围有12个紧邻分子③葡萄糖的一种环状结构简式: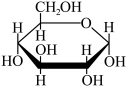
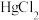 不导电,
不导电,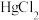 的稀溶液有弱的导电能力且可作手术刀的消毒液。从不同角度分类,
的稀溶液有弱的导电能力且可作手术刀的消毒液。从不同角度分类,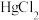 是一种共价化合物、非电解质、盐、分子晶体
是一种共价化合物、非电解质、盐、分子晶体| A.①② | B.②③ | C.①③ | D.②④ |
您最近半年使用:0次
名校
2 . 请回答下列问题:
(1)由磷原子核形成的三种微粒:① 、②
、② 、③
、③ ,半径由大到小的顺序为
,半径由大到小的顺序为_______ (填标号,下同);再失去一个电子所需最低能量由大到小的顺序为_______ 。
(2)比较H-O-H键角大小;H3O+_______ H2O(填“>”、“<”或“=”)。
(3)胍(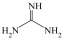 )分子中所有原子共平面,胍中N杂化方式为
)分子中所有原子共平面,胍中N杂化方式为_______ 。
(4)干冰晶体中,每个CO2周围等距离且紧邻的CO2有_______ 个;在冰晶体结构中,每个水分子最多与相邻的_______ 个水分子相连接。同为分子晶体,但干冰中CO2的配位数大于冰中水分子的配位数,其原因是_______ 。
(1)由磷原子核形成的三种微粒:①
 、②
、② 、③
、③ ,半径由大到小的顺序为
,半径由大到小的顺序为(2)比较H-O-H键角大小;H3O+
(3)胍(
 )分子中所有原子共平面,胍中N杂化方式为
)分子中所有原子共平面,胍中N杂化方式为(4)干冰晶体中,每个CO2周围等距离且紧邻的CO2有
您最近半年使用:0次
名校
3 . 环糊精是一类由葡萄糖单元相连形成的闭环低聚糖分子,具有类似截锥状的结构,是现代制药中的一种重要辅料。抗癌药阿霉素与环糊精在水溶液中形成超分子包合物如图,下列说法错误的是
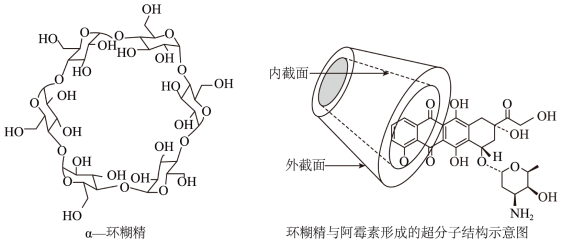
A. 环糊精的结构单元存在转换: 环糊精的结构单元存在转换: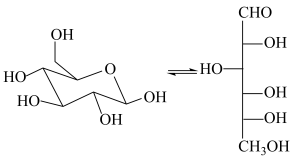 |
| B.环糊精具有分子识别功能 |
| C.形成的超分子中分子间存在范德华力、氢键、共价键等作用 |
| D.形成的超分子增大了阿霉素的水溶性,从而提高其药效 |
您最近半年使用:0次
名校
解题方法
4 . 下列有关晶体的说法中一定正确的是
①原子晶体中只存在非极性共价键;
②稀有气体形成的晶体属于原子晶体;
③SO2与S都属于分子晶体,且SO2的摩尔质量比S的摩尔质量大,所以SO2熔沸点高于S;
④MgCO3与CaCO3都是离子晶体,且Mg2+半径比Ca2+半径小,所以MgCO3的分解温度更高;
⑤分子晶体的堆积均为分子密堆积;
⑥金属晶体和离子晶体都能导电;
⑦离子晶体和金属晶体中均存在阳离子,但金属晶体中却不存在离子键;
⑧依据构成粒子的堆积方式可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体
①原子晶体中只存在非极性共价键;
②稀有气体形成的晶体属于原子晶体;
③SO2与S都属于分子晶体,且SO2的摩尔质量比S的摩尔质量大,所以SO2熔沸点高于S;
④MgCO3与CaCO3都是离子晶体,且Mg2+半径比Ca2+半径小,所以MgCO3的分解温度更高;
⑤分子晶体的堆积均为分子密堆积;
⑥金属晶体和离子晶体都能导电;
⑦离子晶体和金属晶体中均存在阳离子,但金属晶体中却不存在离子键;
⑧依据构成粒子的堆积方式可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体
| A.①③⑦ | B.只有⑦ | C.②④⑤⑦ | D.⑤⑥⑧ |
您最近半年使用:0次
5 . 回答下列问题:
(1) 中含有的含氧官能团名称是
中含有的含氧官能团名称是___________ 。碳原子的杂化方式有___________ ;分子式是___________ ;有___________ 个手性碳原子。
(2)已知熔融的BeCl2不导电,则BeCl2属于___________ 晶体,中心原子的杂化类型为___________ 。
(3)氨水是一种速效氮肥:
①氨水中存在___________ 种氢键,氨极易溶于水的原因是___________ ;
②氨水中含有配位键的粒子有H3O+和X,则X离子中形成的配位键中提供孤电子对的原子是___________ ,X离子能否作为其他配合物的配位体___________ (填“能”或“否”)。
(1)
 中含有的含氧官能团名称是
中含有的含氧官能团名称是(2)已知熔融的BeCl2不导电,则BeCl2属于
(3)氨水是一种速效氮肥:
①氨水中存在
②氨水中含有配位键的粒子有H3O+和X,则X离子中形成的配位键中提供孤电子对的原子是
您最近半年使用:0次
名校
6 . “燕山雪花大如席,纷纷吹落轩辕台”(李白《北风行》),描写了雪景的壮观。下列说法错误的是
| A.水转化为雪的过程是熵减的过程 |
| B.雪花和竹席的主要成分都属于高分子化合物 |
| C.往积雪上撒盐是为了降低水的凝固点,使雪融化 |
| D.雪花的形状受水分子结构和分子间作用力的影响 |
您最近半年使用:0次
7 . 三硫化四磷用于制造火柴及火柴盒摩擦面,分子结构如图所示。下列有关三硫化四磷说法中正确的是
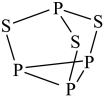
| A.该物质中磷元素的化合价为+3 | B.该物质分子中含有σ键和π键 |
| C.该物质的熔沸点比食盐高 | D.11g该物质含硫原子的数目约为 |
您最近半年使用:0次
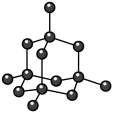
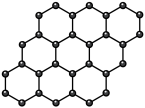
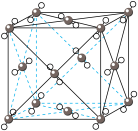
8 . 观察下列模型,判断下列说法错误的是
金刚石 | 碳化硅 | 二氧化硅 | 石墨烯 | 干冰 |
|
|
|
|
|
| A.原子数相同的金刚石和碳化硅,共价键个数之比为1∶2 |
B. 晶体中Si和Si-O键个数比为1∶4 晶体中Si和Si-O键个数比为1∶4 |
| C.石墨烯中碳原子和六元环个数比为2∶1 |
| D.干冰晶体堆积属于分子密堆积 |
您最近半年使用:0次
名校
9 . 下列各项叙述中,正确的是
| A.电负性相差越大的元素间越易形成离子键 |
| B.AB₃型的分子空间结构一定为平面三角形 |
| C.分子晶体中,分子间作用力越大,分子越稳定 |
D.用于幽门螺旋杆菌示踪的 外围电子排布式为2s²2p³ 外围电子排布式为2s²2p³ |
您最近半年使用:0次
10 . 下列说法正确的是
| A.CO2、HClO、P4分子中所有原子均满足最外层8电子稳定结构 |
| B.离子晶体中可能存在共价键,而分子晶体中一定存在共价键 |
| C.氨气很稳定(很高温度才会部分分解),并不是氨气中含有大量的氢键所致 |
| D.金刚石、石英和C60均为空间网状结构的共价晶体,加热熔化时需破坏共价键 |
您最近半年使用:0次