下列各项叙述中,正确的是
| A.电负性相差越大的元素间越易形成离子键 |
| B.AB₃型的分子空间结构一定为平面三角形 |
| C.分子晶体中,分子间作用力越大,分子越稳定 |
D.用于幽门螺旋杆菌示踪的 外围电子排布式为2s²2p³ 外围电子排布式为2s²2p³ |
更新时间:2024-04-26 21:43:27
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】武当山金殿是铜铸鎏金殿。传统鎏金工艺是将金溶于汞中制成“金汞漆”,涂在器物表面,然后加火除汞,使金附着在器物表面。下列说法正确的是
| A.古代大量使用铜制品是因为自然界中铜含量最高 | B.铜原子第一电离能低于锌原子 |
| C.用电化学方法也可实现铜上覆金,金做阴极 | D.铜原子简写的电子排布式:[Ar]4S1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】元素X的价电子排布为(n+1)sn(n+1)pn+2,元素Y位于第四周期的ds区,其基态原子不存在不成对电子。X与Y所形成化合物晶体的晶胞如图所示。下列说法错误的是
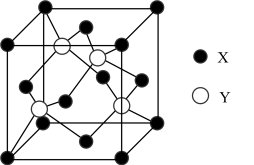

| A.X元素可形成多种同素异形体 | B.晶胞中含有4个X原子 |
| C.X、Y形成的晶体属于原子晶体 | D.X与Y所形成化合物晶体的化学式为YX |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】前四周期元素X、Y、Z、W、T的原子序数依次增大,Y、Z、W位于同一周期,X的最简单氢化物分子的空间结构为正四面体形,Y在同周期中电负性最小,二元化合物E中元素Y和W的质量比为23∶16;同周期元素简单离子中,元素Z形成的离子半径最小;T元素的价电子排布式为3d64s2。下列说法正确的是
| A.简单离子的半径:Y>Z>W |
| B.最高价氧化物对应水化物的酸性:W>Z>X |
| C.W和T的单质混合加热可得化合物TW |
| D.W的单质在足量的氧气中燃烧,所得产物溶于水可得强酸 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】最新研究表明,用Sb(CH)3、Sb(CH3)2Br和Sb(CH3)Br2三种化合物进行重组反应可生成空间位阻最小的离子化合物一[Sb(CH3)5]2[Sb2(CH3)2Br6]。已知锑(Sb)与砷(As)同主族且位于砷的下一周期,下列说法不正确的是
| A.Sb的价电子排布式为5s25p3 |
| B.第一电离能:Br>Sb>As |
| C.电负性:Br>C>H。 |
| D.[Sb(CH3)5]2[Sb2(CH3)2Br6]中存在离子键和共价键 |
您最近半年使用:0次
【推荐2】五种前四周期元素X、Y、Z、W、R在周期表中的位置如图所示。下列叙述正确的是


| A.简单氢化物的沸点:W<X |
| B.五种元素均在元素周期表的s区 |
| C.电负性:Y>W>X |
| D.五种元素所形成单质的晶体类型不同 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】有关杂化轨道的说法不正确的是
| A.杂化前后的轨道数不变,但轨道的形状发生了改变 |
| B.sp3、sp2、sp杂化轨道的夹角分别为109°28′、120°、180° |
| C.四面体形、三角锥形、V形分子的结构可以用sp3杂化轨道解释 |
| D.杂化轨道全部参与形成化学键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列分子中,结构构成平面三角形的是( )
| A.HgCl2 | B.BF3 | C.TeCl4 | D.SF6 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】X、Y、Z、W是原子序数依次增大的前四周期元素。基态X原子的2p轨道上有4个电子,X、Y同主族,Y、Z同周期,基态Z原子能量最高的能级上有1个未成对电子,基态W原子的3d能级上只有1对成对电子。下列说法正确的是
| A.气态氢化物的热稳定性:Y>X |
| B.Y2Z2分子中存在极性键和非极性键 |
| C.加热条件下,Z与W的单质化合生成WZ2 |
D.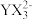 的空间构型为平面三角形 的空间构型为平面三角形 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】卤化钠(NaX)和四卤化钛(TiX4)的熔点如图所示。下判断不正确的是
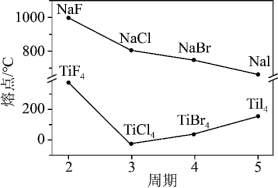
| A.TiF4的熔点反常升高是由于氢键的作用 | B.NaX随X–半径增大,离子键减弱 |
| C.四氯化钛中存在共价键和分子间作用力 | D.由图可看出F的电负性强于Cl、Br、I |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列有关物质结构和性质的比较中,错误的是
| A.熔点:MgCl2>AlCl3 |
| B.键角:CS2>SO2 |
| C.沸点:NH3>HF |
| D.沸点:对羟基苯甲醛>邻羟基苯甲醛 |
您最近半年使用:0次


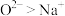
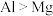

 ;沸点
;沸点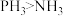
 ;沸点
;沸点


