下列性质的比较中,不正确 的是
A.电负性: | B.微粒半径: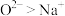 |
C.第一电离能: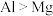 | D.酸性: |
更新时间:2023-01-08 09:05:43
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列有关卤素的说法错误的是( )
| A.从HF、HCl、HBr、HI酸性递增的事实,可推出F、Cl、Br、I的非金属性递增的规律 |
| B.淀粉碘化钾溶液在空气中变蓝,4I-+O2+2H2O=2I2+4OH- |
| C.卤化银(除氟化银)均为不溶于水的有色固体 |
| D.HF、HCl、HBr、HI的热稳定性依次减弱,还原性依次增强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述中,A的金属性肯定比B的金属性强的是
| A.A原子的最外层电子数比B原子的最外层电子数少 |
| B.A的氢氧化物为两性氧化物,B的氢氧化物为弱碱 |
| C.1molA从酸中置换出来的H+生成的H2比1molB从酸中置换出来的H+生成的H2多 |
| D.A元素的电负性比B元素的电负性小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】短周期元素X、Y、Z、W、E原子序数依次增大。X是密度最小的金属,其电荷密度大,是当前动力电池的重要构成元素。Y与X同主族。Z原子核外最内层与最外层电子总数相等,其单质常用于地下管道、轮船等金属的腐蚀防护。W、E相邻,可形成所有原子最外层 电子稳定结构的
电子稳定结构的 化合物。下列说法
化合物。下列说法正确 的是
 电子稳定结构的
电子稳定结构的 化合物。下列说法
化合物。下列说法A.原子半径: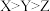 |
B.简单氢化物的热稳定性: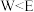 |
| C.Y和Z元素的最高价氧化物的水化物能互相反应 |
D.化合物 中E的化合价为正价 中E的化合价为正价 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】W、X、Y、Z均为短周期主族元素,原子序数依次增加。W原子最外层电子数是其所在周期数的2倍;Y+和X2-的电子层结构相同;Z的原子序数等于W和Y的核外电子数之和。下列说法正确的是
| A.Z的氢化物的酸性比WX2的水化物的强,说明Z的非金属性比W的强 |
| B.离子半径大小:Z>Y>X |
| C.X和Y形成的化合物为离子化合物且阳离子和阴离子的个数之比为2:1 |
| D.Z元素的气态氢化物的热稳定性比X的高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】反应NH4C1+NaNO2=NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列有关反应中相关元素和物质的说法正确的是
| A.元素的第一电离能:O>N>Na |
| B.P元素能形成PCl5,则同主族的N元素也能形成NCl5 |
| C.Na元素的焰色反应是Na原子能级跃迁的结果,是金属特有的化学性质 |
D.NO 中N原子采取sp2杂化,NO 中N原子采取sp2杂化,NO 是V型结构 是V型结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】现有四种元素的基态原子的电子排布式:①1s22s22p4②1s22s22p63s1③1s22s22p3④1s22s22p5,则下列有关比较中不正确 的是
| A.非金属性:④>①>③ | B.第一电离能:④>③>①>② |
| C.最高正化合价:④>①>③>② | D.电负性:④>①>③>② |
您最近一年使用:0次
【推荐1】下列有关物质结构与性质的说法错误的是
| A.I2易溶于CCl4,可从I2和CCl4都是非极性分子的角度解释 |
| B.氟的电负性大于氯的电负性,导致三氟乙酸的酸性大于三氯乙酸 |
| C.对羟基苯甲酸存在分子内氢键,是其沸点比邻羟基苯甲酸的高的主要原因 |
D.AgCl溶于氨水,是由于AgCl与NH3反应生成了可溶性配合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、Q、W是原子序数依次增大的前四周期元素,其中X是宇宙中含量最多的元素; 元素原子最高能级的不同轨道都有电子,并且自旋方向相同;
元素原子最高能级的不同轨道都有电子,并且自旋方向相同; 元素原子的价层电子排布是
元素原子的价层电子排布是 ;Q、W元素原子的最外层均只有1个电子,但
;Q、W元素原子的最外层均只有1个电子,但 元素原子中只有两种形状的电子云,
元素原子中只有两种形状的电子云, 元素原子的次外层内的所有轨道的电子均成对。下列说法正确的是
元素原子的次外层内的所有轨道的电子均成对。下列说法正确的是
 元素原子最高能级的不同轨道都有电子,并且自旋方向相同;
元素原子最高能级的不同轨道都有电子,并且自旋方向相同; 元素原子的价层电子排布是
元素原子的价层电子排布是 ;Q、W元素原子的最外层均只有1个电子,但
;Q、W元素原子的最外层均只有1个电子,但 元素原子中只有两种形状的电子云,
元素原子中只有两种形状的电子云, 元素原子的次外层内的所有轨道的电子均成对。下列说法正确的是
元素原子的次外层内的所有轨道的电子均成对。下列说法正确的是A.电负性: | B.键角: |
C. 的阴阳离子比为 的阴阳离子比为 | D.W元素位于元素周期表的d区 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】X、Y、Z、W、R 为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示。下列说法错误的是
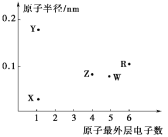
| A.简单离子半径:Y<W | B.元素的电负性:Z<W |
| C.R 为氧元素 | D.X 与 Z 可以形成正四面体结构的分子 |
您最近一年使用:0次

 、
、 、
、 、
、
 、
、
 ),判断下列说法正确的是
),判断下列说法正确的是





