根据下列五种元素的电离能数据(单位: ),判断下列说法正确的是
),判断下列说法正确的是
 ),判断下列说法正确的是
),判断下列说法正确的是| 元素代号 |  |  |  |  |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
| A.元素的电负性最大的可能是U元素 |
| B.R和S均可能与U在同一主族 |
| C.U元素可能在元素周期表的s区 |
| D.原子的价电子排布为ns2np3的可能是T元素 |
更新时间:2022-07-28 15:18:36
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】短周期主族元素X、Y、Z、W、Q原子序数依次增大,X原子在s区中半径最小,基态Z原子的价电子排布式为 ,Y元素的简单氢化物可用作制冷剂,W元素在同周期元素中第一电离能最小,Q原子的最外层电子数与Z和W的最外层电子数之和相等。下列说法正确的是
,Y元素的简单氢化物可用作制冷剂,W元素在同周期元素中第一电离能最小,Q原子的最外层电子数与Z和W的最外层电子数之和相等。下列说法正确的是
 ,Y元素的简单氢化物可用作制冷剂,W元素在同周期元素中第一电离能最小,Q原子的最外层电子数与Z和W的最外层电子数之和相等。下列说法正确的是
,Y元素的简单氢化物可用作制冷剂,W元素在同周期元素中第一电离能最小,Q原子的最外层电子数与Z和W的最外层电子数之和相等。下列说法正确的是A.第一电离能: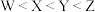 |
| B.Z分别与其他四种元素形成的二元化合物至少有两种 |
| C.Y、Z、W、Q的简单氢化物中沸点最高的是Z |
D.工业上电解饱和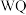 溶液制备W单质 溶液制备W单质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】根据元素周期律和物质结构的知识,以下有关排序正确的是
A.离子半径: | B.第一电离能:N>O>C |
| C.熔点:SiC < SiCl4 < MgBr2 | D.键角:ASH3 > PH3 > NH3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】酞菁钴被广泛应用于光电材料、光动力学光敏材料等方面。酞菁钴(II)结构如图所示(Co均形成单键,部分化学键未画明)。下列说法错误的是( )
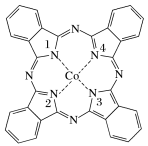

| A.酞菁钴(II)中三种非金属元素的电负性大小顺序为N>C>H |
| B.酞菁钴(II)中碳原子的杂化方式只有sp2杂化 |
| C.1号和3号N原子的VSEPR模型均为平面三角形 |
| D.2号和4号N原子与Co(Ⅱ)是通过配位键结合 |
您最近一年使用:0次
【推荐2】下列与分子性质有关的说法正确的是
| A.氟代丙二酸(HOOC—CF2—COOH)酸性强于丙二酸(HOOC—CH2—COOH)是因为F原子吸引电子能力大于H原子,导致氟代丙二酸羧基中-OH的极性更大更易电离出H+ |
B.邻硝基苯酚(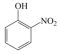 )的沸点高于对硝基苯酚( )的沸点高于对硝基苯酚(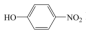 )是因为后者形成了分子间氢键 )是因为后者形成了分子间氢键 |
| C.C的电负性强于Si,所以CH4的熔沸点高于SiH4 |
| D.I2受热易升华,是因为分子内共价键键能较小所致 |
您最近一年使用:0次





