现有四种元素的基态原子的电子排布式:①1s22s22p4②1s22s22p63s1③1s22s22p3④1s22s22p5,则下列有关比较中不正确 的是
| A.非金属性:④>①>③ | B.第一电离能:④>③>①>② |
| C.最高正化合价:④>①>③>② | D.电负性:④>①>③>② |
更新时间:2022-02-28 18:36:36
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列表达方式错误的是
A.四氯化碳的电子式: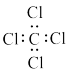 | B.氟化钠的电子式: |
| C.硫离子的核外电子排布式:1s22s22p63s23p6 | D.碳-12原子: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】周期表中VIA族元素及其化合物应用广泛。H2S(燃烧热为562.2kJ•mol-1)是一种易燃的有毒气体,可制取各种硫化物;硫酸、硫酸盐是重要化工原料;硫酰氯(SO2Cl2)是重要的化工试剂,常作氯化剂或氯磺化剂。硒(34Se)(和碲(52Te)的单质及其化合物在电子、冶金、材料等领域有广阔的发展前景,工业上以精炼铜的阳极泥(含CuSe)为原料回收Se,以电解强碱性Na2TeO3溶液制备Te。下列说法正确的是
| A.H2O2是非极性分子 | B.SO3中的∠O-S-O与SO 中的相等 中的相等 |
| C.基态Se原子核外价电子排布式为4s24p4 | D.VIA族元素氢化物的沸点从上到下依次增大 |
您最近一年使用:0次
【推荐1】以下有关元素性质的说法不正确的是
| A.具有下列电子排布式的原子中:①1s22s22p63s23p2,②1s22s22p3,③1s22s22p2,④1s22s22p63s23p4,原子半径最大的是① |
| B.具有下列价电子排布式的原子中:①3s23p1,②3s23p2,③3s23p3,④3s23p4,第一电离能最大的是③ |
| C.①Na、K、Rb,②N、P、As,③O、S、Se,④Na、P、Cl中,元素的电负性随原子序数增大而递增的是④ |
| D.电子构型为[Xe]4f145d76s2的元素位于周期表中的f区 |
您最近一年使用:0次
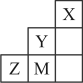
【推荐2】元素周期表前四周期元素的一部分如图所示,X、Y、Z、M均为主族元素,其中M元素原子的最外层电子数为其次外层电子数的 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是
| A.第一电离能:Z>M | B.电负性:Y>M>Z |
| C.离子半径:X->Y2- | D.Y元素基态原子的简化电子排布式:[Ne]3s23p4 |
您最近一年使用:0次
【推荐1】下列各项叙述中,正确的是
| A.N、P、As的电负性随原子序数的增大而增大 |
| B.价电子排布为3d54s2的元素位于第四周期VA族,是p区元素 |
| C.2p和3p轨道形状均为哑铃形,能量也相等 |
D.氮原子的最外层电子排布图: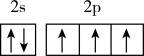 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】克菌丹是一种用于农作物的保护性杀菌剂,世界卫生组织公布其为致癌物,其结构简式如图所示。下列说法正确的是
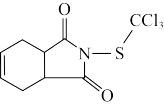

| A.电负性:O>Cl>S | B.热稳定性: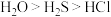 |
C.该分子中S采用 杂化 杂化 | D.酸性: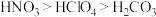 |
您最近一年使用:0次

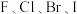 等,位于周期表VIIA族。卤族元素形成物质种类众多,磷可形成多种卤化物,其中固态
等,位于周期表VIIA族。卤族元素形成物质种类众多,磷可形成多种卤化物,其中固态 和
和 的结构分别是
的结构分别是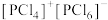 和
和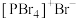 。溴化碘
。溴化碘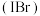 的化学性质与卤素相似。下列物质结构与性质或物质性质与用途具有对应关系的是
的化学性质与卤素相似。下列物质结构与性质或物质性质与用途具有对应关系的是
 水溶液呈中性,可用于氯碱工业制取
水溶液呈中性,可用于氯碱工业制取
 的酸性弱于
的酸性弱于 的酸性
的酸性

