1 . 硫酸是重要的化工原料,某兴趣小组对浓硫酸的性质进行如下探究。
(1)棉布上滴浓H2SO4后破洞。体现了浓H2SO4的_______ (填“脱水”“吸水”或“强氧化”、下同)性;在冷的浓H2SO4中放入铁片无明显现象,体现了浓H2SO4的_______ 性。
为了检验浓硫酸与木炭在加热条件下反应产生的SO2和CO2气体,设计了如图所示实验装置,a、b、c为止水夹,B是用于储气的气囊。(已知淀粉溶液遇I2变蓝)
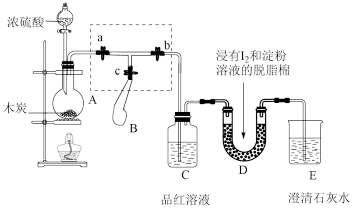
(2)装置A中发生反应的化学方程式为_______ 。
(3)实验时,装置C中的现象为_______ 。
(4)此实验成败的关键在于控制反应产生气体的速率不能过快,因此设计了虚框部分的装置,正确的操作顺序是_______ (填序号)。
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b
③打开止水夹a和c,关闭止水夹b
(5)若要检验浓硫酸与木炭在加热条件下生成的水蒸气,可在装置_______ 之间加上一个盛有无水CuSO4的硬质玻璃管。
(6)当D中产生_______ 现象时,可以说明使E中澄清石灰水变浑浊的是CO2,而不是SO2;写出D中发生反应的化学方程式_______ 。
(7)当D中反应转移电子0.3mol时,参加反应的气体体积(标准状况下)为_______ L。
(1)棉布上滴浓H2SO4后破洞。体现了浓H2SO4的
为了检验浓硫酸与木炭在加热条件下反应产生的SO2和CO2气体,设计了如图所示实验装置,a、b、c为止水夹,B是用于储气的气囊。(已知淀粉溶液遇I2变蓝)

(2)装置A中发生反应的化学方程式为
(3)实验时,装置C中的现象为
(4)此实验成败的关键在于控制反应产生气体的速率不能过快,因此设计了虚框部分的装置,正确的操作顺序是
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b
③打开止水夹a和c,关闭止水夹b
(5)若要检验浓硫酸与木炭在加热条件下生成的水蒸气,可在装置
(6)当D中产生
(7)当D中反应转移电子0.3mol时,参加反应的气体体积(标准状况下)为
您最近一年使用:0次
2022-02-20更新
|
568次组卷
|
2卷引用:吉林省长春外国语学校2022-2023学年高一下学期6月月考化学试题
名校
解题方法
2 . 甲同学通过查询资料知道,一定浓度的硝酸与镁反应时,可得到二氧化氮、一氧化氮、氮气三种气体。该同学用下列仪器组装装置来直接验证有二氧化氮、一氧化氮生成并制取氮化镁 (假设实验中每步转化均是完全的) 。查阅文献得知:
①二氧化氮沸点为21.1 ℃、熔点为-11 ℃,一氧化氮沸点为-151 ℃、熔点为-164 ℃;
②镁也能与二氧化碳反应;
③氮化镁遇水反应生成氢氧化镁和氨气。
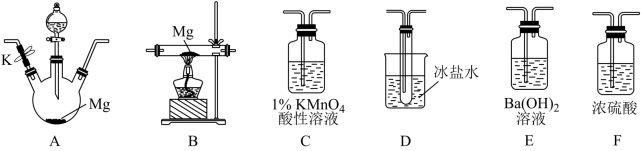
(1)实验中先打开开关K,通过导管向装置内通入二氧化碳气体以排出装置内的空气,停止通入二氧化碳的标志是___________ 。
(2)为实现上述实验目的,所选用的仪器的正确连接方式是A→___________ →E,确定还原产物中有二氧化氮的现象是___________ ,实验中要多次使用装置F,第二次使用F的目的是___________ 。
(3)实验过程中,发现在D中产生预期现象的同时,C中溶液颜色慢慢褪去,试写出C中反应的离子方程式:___________ 。
(4)甲同学在A中开始反应时,马上点燃B处的酒精灯,实验结束后通过测试发现B处的产品纯度不高,原因是___________ 。
①二氧化氮沸点为21.1 ℃、熔点为-11 ℃,一氧化氮沸点为-151 ℃、熔点为-164 ℃;
②镁也能与二氧化碳反应;
③氮化镁遇水反应生成氢氧化镁和氨气。

(1)实验中先打开开关K,通过导管向装置内通入二氧化碳气体以排出装置内的空气,停止通入二氧化碳的标志是
(2)为实现上述实验目的,所选用的仪器的正确连接方式是A→
(3)实验过程中,发现在D中产生预期现象的同时,C中溶液颜色慢慢褪去,试写出C中反应的离子方程式:
(4)甲同学在A中开始反应时,马上点燃B处的酒精灯,实验结束后通过测试发现B处的产品纯度不高,原因是
您最近一年使用:0次
2021-04-06更新
|
311次组卷
|
4卷引用:吉林省白城市第一中学2020-2021学年高一下学期3月阶段性考试化学试题
解题方法
3 . 根据要求完成下列各小题实验目的。(a、b为弹簧夹,(加热及固定装置已略去)
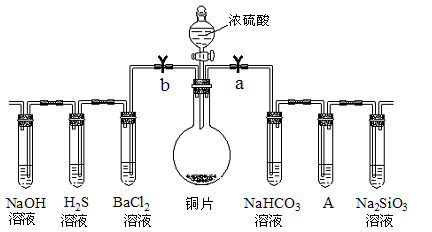
Ⅰ.验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
(1)连接仪器、_______ 、加药品后,打开a关闭b,然后滴入浓硫酸,加热。
(2)装置A中试剂是_______ ,装浓硫酸的仪器名称为_______
(3)能说明碳的非金属性比硅强的实验现象是_______
Ⅱ.验证SO2的氧化性、还原性和酸性氧化物的通性。
(1)在Ⅰ(1)操作后打开b,关闭a。
(2)一段时间后,H2S溶液中的现象是_______ ,化学方程式是_______ 。
(3)BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
写出其中SO2显示还原性生成沉淀的离子方程式_______

Ⅰ.验证碳、硅非金属性的相对强弱。(已知酸性:亚硫酸>碳酸)
(1)连接仪器、
(2)装置A中试剂是
(3)能说明碳的非金属性比硅强的实验现象是
Ⅱ.验证SO2的氧化性、还原性和酸性氧化物的通性。
(1)在Ⅰ(1)操作后打开b,关闭a。
(2)一段时间后,H2S溶液中的现象是
(3)BaCl2溶液中无明显现象,将其分成两份,分别滴加下列溶液,将产生的沉淀的化学式填入下表相应位置。
| 滴加的溶液 | 氯水 | 氨水 |
| 沉淀的化学式 |
您最近一年使用:0次
名校
4 . 某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示装置进行有关实验。
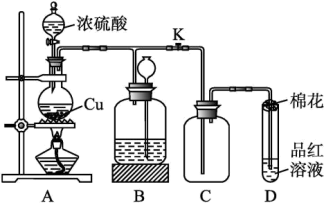
(1)装置A中发生反应的化学方程式为___________
(2)装置D中试管口放置的棉花应浸一种溶液,这种溶液是___________ 其作用是___________
(3)装置B的作用是___________ 当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是___________ B中应放置的液体是___________ (填字母)
A.水 B.酸性高锰酸钾 C.浓溴水 D.饱和NaHSO3
(4)实验中,取一定质量的铜片和一定体积18 mol•L-1的浓硫酸放在圆底烧瓶中共热,反应完毕时,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余,下列药品能用来证明反应结束后的烧瓶中有余酸的是___________ (填字母)。
a.铁粉 b.BaCl2溶液 c.银粉 d.Na2CO3溶液
(5)实验完毕,待A中烧瓶内液体冷却后,过滤,向滤液中加入少量的蒸馏水稀释,溶液为蓝色。为了证明蓝色只与Cu2+有关,而与其他离子无关,某同学设计了下列实验,其中对实验目的没有意义的是___________ 。(填序号)
①观察稀硫酸溶液呈无色;②观察CuSO4粉末呈白色;③稀释CuSO4溶液,溶液蓝色变浅;④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色;⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍呈蓝色。

(1)装置A中发生反应的化学方程式为
(2)装置D中试管口放置的棉花应浸一种溶液,这种溶液是
(3)装置B的作用是
A.水 B.酸性高锰酸钾 C.浓溴水 D.饱和NaHSO3
(4)实验中,取一定质量的铜片和一定体积18 mol•L-1的浓硫酸放在圆底烧瓶中共热,反应完毕时,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余,下列药品能用来证明反应结束后的烧瓶中有余酸的是
a.铁粉 b.BaCl2溶液 c.银粉 d.Na2CO3溶液
(5)实验完毕,待A中烧瓶内液体冷却后,过滤,向滤液中加入少量的蒸馏水稀释,溶液为蓝色。为了证明蓝色只与Cu2+有关,而与其他离子无关,某同学设计了下列实验,其中对实验目的没有意义的是
①观察稀硫酸溶液呈无色;②观察CuSO4粉末呈白色;③稀释CuSO4溶液,溶液蓝色变浅;④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色;⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍呈蓝色。
您最近一年使用:0次
2021-04-06更新
|
131次组卷
|
3卷引用:吉林省白城市第一中学2020-2021学年高一下学期3月阶段性考试化学试题
名校
解题方法
5 . 近年我国某些城市酸雨污染较为严重,主要是因为大量燃烧含硫量高的煤。
【实验目的】通过实验证明煤中含有碳元素和硫元素。
(1)查阅资料知,二氧化硫能使高锰酸钾溶液褪色。请完成该反应的离子方程式:
____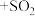 ____
____ _____=_____
_____=_____ _____
_____ ____
____ 。
。____________
(2)根据上述资料,甲同学和丙同学分别设计实验方案进行探究。
【实验操作】甲同学进行了如图所示A、B两步实验。
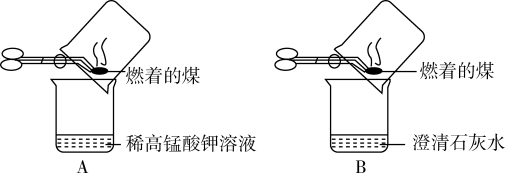
【实验现象】A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊。
【得出结论】煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
①乙同学认为甲同学的方案不合理,其理由是_____________________ 。
【实验操作】丙同学进行了如图所示实验。
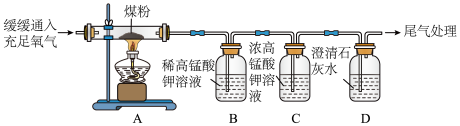
②C装置的作用是_____________________ 。
③证明煤中含有碳元素和硫元素的现象是_______________________ 。
④C装置中的浓高锰酸钾溶液也可以替换为_______________ (填标号)。
A.足量I2的淀粉溶液B.足量饱和 溶液
溶液
C.足量 溶液D.足量溴水
溶液D.足量溴水
【实验目的】通过实验证明煤中含有碳元素和硫元素。
(1)查阅资料知,二氧化硫能使高锰酸钾溶液褪色。请完成该反应的离子方程式:
____
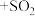 ____
____ _____=_____
_____=_____ _____
_____ ____
____ 。
。(2)根据上述资料,甲同学和丙同学分别设计实验方案进行探究。
【实验操作】甲同学进行了如图所示A、B两步实验。

【实验现象】A中稀高锰酸钾溶液褪色,B中澄清石灰水变浑浊。
【得出结论】煤燃烧生成二氧化硫和二氧化碳,证明煤中含有碳元素和硫元素。
①乙同学认为甲同学的方案不合理,其理由是
【实验操作】丙同学进行了如图所示实验。

②C装置的作用是
③证明煤中含有碳元素和硫元素的现象是
④C装置中的浓高锰酸钾溶液也可以替换为
A.足量I2的淀粉溶液B.足量饱和
 溶液
溶液C.足量
 溶液D.足量溴水
溶液D.足量溴水
您最近一年使用:0次
2020-10-10更新
|
405次组卷
|
6卷引用:吉林省洮南市第一中学2022-2023学年高一下学期阶段性测试化学试题
6 . 用下列实验装置进行相应实验,装置(加热和夹持装置已省略)正确且能达到相应实验目的的是( )
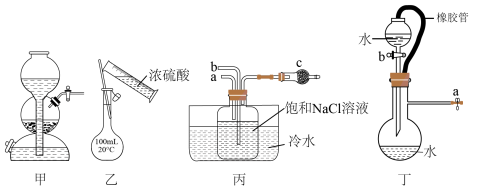

A.装置丙是模拟侯氏制碱法的部分装置,则从a口通入的气体为 |
B.用 浓硫酸配制 浓硫酸配制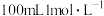 稀硫酸会涉及图乙所示操作 稀硫酸会涉及图乙所示操作 |
C.实验室可用浓盐酸和 制备氯气,用装置甲作为发生装置,其优点是随关随停 制备氯气,用装置甲作为发生装置,其优点是随关随停 |
| D.检验装置丁的气密性:关闭止水夹a,打开活塞b,水能持续顺利流下,则表示装置气密性不好 |
您最近一年使用:0次
2023-10-17更新
|
306次组卷
|
2卷引用:吉林省部分名校2023-2024学年高二上学期10月联考化学试题
名校
7 . 下列实验操作不能达到实验目的的是( )
| 实验目的 | 实验操作 | |
| A | 检验蔗糖是否水解 | 向20%蔗糖溶液中加入少量稀硫酸,加热;再加入新制氢氧化铜悬浊液,观察现象 |
| B | 乙醇和乙酸制备乙酸乙酯 | 先加入一定量乙醇,再加浓硫酸和乙酸,最后加入适量沸石并加热 |
| C | 鉴别硬脂酸钠和硬脂酸钾 | 分别蘸取两种物质在酒精灯火焰上灼烧,观察火焰的颜色 |
| D | 比较水和乙醇中氢的活泼性 | 分别将少量钠投入盛有水和乙醇的烧杯中,观察现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-04-23更新
|
316次组卷
|
2卷引用:长春吉大附中实验学校高二下学期网上学习效果检测化学试题
8 . 下列装置能达到实验目的的是
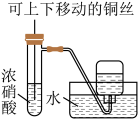 | 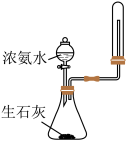 | 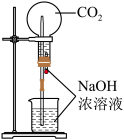 |  |
| A.制备并收集少量NO2气体 | B.实验室快速制备NH3 | C.进行喷泉实验 | D.实验室制备乙酸乙酯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-10-09更新
|
186次组卷
|
4卷引用:吉林省长春市博硕学校(原北京师范大学长春附属学校)2022-2023学年高三上学期第五次月考化学试题
9 . 实验装置不能达到实验目的的是
| A | B |
 |  |
| 稀释浓硫酸 | 制备并检验 气体 气体 |
| C | D |
 | 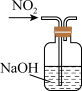 |
用该装置制备少量白色的 沉淀 沉淀 | 吸收 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 用下列仪器或装置(图中夹持略)进行相应实验,能达到实验目的的是
| A | B | C | D |
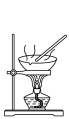 | 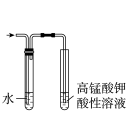 | 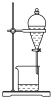 | 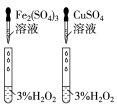 |
蒸发结晶制备 晶体 晶体 | 检验溴乙烷消去产物 | 分离苯和溴苯 | 探究不同催化剂 对  分解速率的影响 分解速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-18更新
|
661次组卷
|
6卷引用:吉林市第一中学2021-2022学年高三下学期4月教学质量检测理科综合化学试题



