某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示装置进行有关实验。
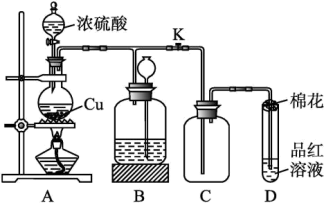
(1)装置A中发生反应的化学方程式为___________
(2)装置D中试管口放置的棉花应浸一种溶液,这种溶液是___________ 其作用是___________
(3)装置B的作用是___________ 当D处有明显的现象后,关闭旋塞K,移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中现象是___________ B中应放置的液体是___________ (填字母)
A.水 B.酸性高锰酸钾 C.浓溴水 D.饱和NaHSO3
(4)实验中,取一定质量的铜片和一定体积18 mol•L-1的浓硫酸放在圆底烧瓶中共热,反应完毕时,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余,下列药品能用来证明反应结束后的烧瓶中有余酸的是___________ (填字母)。
a.铁粉 b.BaCl2溶液 c.银粉 d.Na2CO3溶液
(5)实验完毕,待A中烧瓶内液体冷却后,过滤,向滤液中加入少量的蒸馏水稀释,溶液为蓝色。为了证明蓝色只与Cu2+有关,而与其他离子无关,某同学设计了下列实验,其中对实验目的没有意义的是___________ 。(填序号)
①观察稀硫酸溶液呈无色;②观察CuSO4粉末呈白色;③稀释CuSO4溶液,溶液蓝色变浅;④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色;⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍呈蓝色。

(1)装置A中发生反应的化学方程式为
(2)装置D中试管口放置的棉花应浸一种溶液,这种溶液是
(3)装置B的作用是
A.水 B.酸性高锰酸钾 C.浓溴水 D.饱和NaHSO3
(4)实验中,取一定质量的铜片和一定体积18 mol•L-1的浓硫酸放在圆底烧瓶中共热,反应完毕时,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余,下列药品能用来证明反应结束后的烧瓶中有余酸的是
a.铁粉 b.BaCl2溶液 c.银粉 d.Na2CO3溶液
(5)实验完毕,待A中烧瓶内液体冷却后,过滤,向滤液中加入少量的蒸馏水稀释,溶液为蓝色。为了证明蓝色只与Cu2+有关,而与其他离子无关,某同学设计了下列实验,其中对实验目的没有意义的是
①观察稀硫酸溶液呈无色;②观察CuSO4粉末呈白色;③稀释CuSO4溶液,溶液蓝色变浅;④往CuSO4溶液中加入足量NaOH溶液,生成蓝色沉淀,过滤,滤液呈无色;⑤往CuSO4溶液中加入足量BaCl2的溶液,生成白色沉淀,过滤,滤液仍呈蓝色。
更新时间:2021-04-06 23:17:07
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】按照要求回答问题。
(1)非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的 ,则A物质为
,则A物质为___________ ,C→D的化学方程式:___________ 。

(2)物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据如图所示回答问题:

①检验某物质一定是Y的方法是___________ 。
②W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为___________ ;若反应后收集到336mL气体产物(标准状况),则电子转移数目为___________ 。
③欲制备 ,从氧化还原角度分析,合理的是
,从氧化还原角度分析,合理的是___________ (填序号)。
A. B.
B. C.
C. D.
D.
(1)非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的
 ,则A物质为
,则A物质为
(2)物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据如图所示回答问题:

①检验某物质一定是Y的方法是
②W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为
③欲制备
 ,从氧化还原角度分析,合理的是
,从氧化还原角度分析,合理的是A.
 B.
B. C.
C. D.
D.
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组对化合物X开展探究实验。
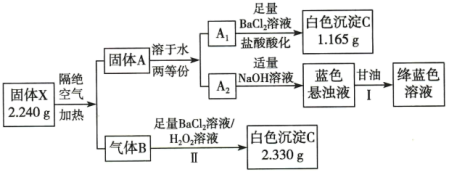
其中:X是易溶于水的强酸盐,由3种元素组成;A和B均为纯净物;B可使品红水溶液褪色。请回答:
关于气体B使品红水溶液褪色的原因,一般认为:B不能使品红褪色,而是B与水反应的生成物使品红褪色。请设计实验证明_______ 。

其中:X是易溶于水的强酸盐,由3种元素组成;A和B均为纯净物;B可使品红水溶液褪色。请回答:
关于气体B使品红水溶液褪色的原因,一般认为:B不能使品红褪色,而是B与水反应的生成物使品红褪色。请设计实验证明
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】二氧化硫的制备
(1)反应原理:_________ ,利用强酸制弱酸的原理制备SO2
(2)实验装置:
①气体发生装置类型:_________ [固液常温制取气体]
②发生装置所用仪器的名称为__________ 、____________
(3)在还原性探究实验中,发生反应:_________
(4)在氧化性探究实验中,发生反应:_________
(5)在漂白性探究实验中,品红溶液褪色,加热后________
(6)尾气处理:__________
(7)SO2密度比空气大,在水中溶解度较大,选择________ 法收集
(8)思考探究:除去酸性气体中HCl的方法?_________
| 发生装置(原理) | 性质探究 | 尾气处理 |
 | ||
(2)实验装置:
①气体发生装置类型:
②发生装置所用仪器的名称为
(3)在还原性探究实验中,发生反应:
(4)在氧化性探究实验中,发生反应:
(5)在漂白性探究实验中,品红溶液褪色,加热后
(6)尾气处理:
(7)SO2密度比空气大,在水中溶解度较大,选择
(8)思考探究:除去酸性气体中HCl的方法?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】在烧瓶放20 g蔗糖,依次加入少量水、20mL浓硫酸,蔗糖逐渐变黑,体积膨胀,形成疏松多孔的黑面包,烧瓶发烫,品红溶液颜色变淡。请回答:

(1)仪器a的名称___________
(2)小试管盛装试剂___________
(3)浓硫酸与碳反应方程式___________ :
(4)下列说法不正确的是___________
A 蔗糖变黑说明发生过程 C12H22O11→C+H2O
B 品红颜色变淡说明SO2有漂白性
C 上述实验体现浓硫酸的脱水性、吸水性和氧化性
D 将气体依次通过饱和碳酸氢钠溶液、澄清石灰水,石灰水变浑浊证明含有CO2

(1)仪器a的名称
(2)小试管盛装试剂
(3)浓硫酸与碳反应方程式
(4)下列说法不正确的是
A 蔗糖变黑说明发生过程 C12H22O11→C+H2O
B 品红颜色变淡说明SO2有漂白性
C 上述实验体现浓硫酸的脱水性、吸水性和氧化性
D 将气体依次通过饱和碳酸氢钠溶液、澄清石灰水,石灰水变浑浊证明含有CO2
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】汽车尾气中的有害气体主要有NO、碳氢化合物及CO,某校同学设计实验将模拟汽车尾气转化为无害气体。回答下列问题;

(1) 为了配制模拟尾气,甲组同学用上图所示装置分别制备NO、乙烯及CO三袋气体。
① 在实验室中用装置A制取NO,分液漏斗中盛放的是_______ (填试剂名称)。
② 用 (乙烯利)与NaOH溶液并用装置B制取乙烯,反应生成乙烯的化学方程式为(已知磷转化为Na3 PO4)
(乙烯利)与NaOH溶液并用装置B制取乙烯,反应生成乙烯的化学方程式为(已知磷转化为Na3 PO4)_______________________ 。
③ 用H2C2O4与浓硫酸制取CO的化学方程式:H2C2O4 CO↑ + CO2 ↑+ H2O↑,然后进行提纯,选用上图装置预制一袋干燥纯净的CO,各接口连接的顺序为(气流从左至右)
CO↑ + CO2 ↑+ H2O↑,然后进行提纯,选用上图装置预制一袋干燥纯净的CO,各接口连接的顺序为(气流从左至右)___________ →g,其中装置C中主要仪器的名称是________ ,装置D中盛放的药品是_______ 。
(2) 乙组同学将甲组制得的气体与空气按适当比例混合形成模拟尾气(NO、CO、C2 H4及空气),按如图所示装置进行尾气转化并检验。

① 为检验催化反应后的气体中是否有CO2生成和乙烯的残留,G、H中盛放的试剂依次是_______ (填标号)。
a. NaOH溶液 b. 酸性KMnO4溶液 c. 澄清石灰水 d. Br2/CCl4溶液
② 通“模拟尾气”前,需先将催化剂加热到反应所需的温度,其目的是__________________ ;写出其中CO与NO完全转化为无害气体的化学方程式:_____________________ 。

(1) 为了配制模拟尾气,甲组同学用上图所示装置分别制备NO、乙烯及CO三袋气体。
① 在实验室中用装置A制取NO,分液漏斗中盛放的是
② 用
 (乙烯利)与NaOH溶液并用装置B制取乙烯,反应生成乙烯的化学方程式为(已知磷转化为Na3 PO4)
(乙烯利)与NaOH溶液并用装置B制取乙烯,反应生成乙烯的化学方程式为(已知磷转化为Na3 PO4)③ 用H2C2O4与浓硫酸制取CO的化学方程式:H2C2O4
 CO↑ + CO2 ↑+ H2O↑,然后进行提纯,选用上图装置预制一袋干燥纯净的CO,各接口连接的顺序为(气流从左至右)
CO↑ + CO2 ↑+ H2O↑,然后进行提纯,选用上图装置预制一袋干燥纯净的CO,各接口连接的顺序为(气流从左至右)(2) 乙组同学将甲组制得的气体与空气按适当比例混合形成模拟尾气(NO、CO、C2 H4及空气),按如图所示装置进行尾气转化并检验。

① 为检验催化反应后的气体中是否有CO2生成和乙烯的残留,G、H中盛放的试剂依次是
a. NaOH溶液 b. 酸性KMnO4溶液 c. 澄清石灰水 d. Br2/CCl4溶液
② 通“模拟尾气”前,需先将催化剂加热到反应所需的温度,其目的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】已知甲、乙、丙、丁、戊是中学化学中常见的物质,常温下,戊是一种无色无味的液体,它们之间有如下反应关系。

(1)若甲是一种黑色晶体,且具有磁性。乙是一种常见的挥发性酸,丁为无色气体,则反应的离子方程式为:_____________________________
(2)若甲是一种紫红色单质,乙是一种常见的难挥发性酸,反应时生成的丁是无色气体,反应的化学方程式是________________ ,将过量丁气体通入到石蕊溶液中,将看到的现象为:_____________________
(3)若实验室中利用固体甲和固体乙的反应制备气体丙,丙是一种无色、刺激性气味、密度比空气小的气体,则甲、乙为:__________________ (填化学式),
实验室通常如何证明有丙生成:___________________________ 。
(4)若甲为常见有色气体单质,乙为强碱,该反应的离子方程式为:_____________________ ,已知丙由三种元素组成,其电子式_______________________

(1)若甲是一种黑色晶体,且具有磁性。乙是一种常见的挥发性酸,丁为无色气体,则反应的离子方程式为:
(2)若甲是一种紫红色单质,乙是一种常见的难挥发性酸,反应时生成的丁是无色气体,反应的化学方程式是
(3)若实验室中利用固体甲和固体乙的反应制备气体丙,丙是一种无色、刺激性气味、密度比空气小的气体,则甲、乙为:
实验室通常如何证明有丙生成:
(4)若甲为常见有色气体单质,乙为强碱,该反应的离子方程式为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某同学为了探究甲烷、乙烯分别与卤素反应的情况,设计了以下实验,请回答问题。
Ⅰ.取2支硬质大试管,通过排饱和食盐水法先后各收集半试管甲烷和半试管氯气。分别用铁架台固定好,按如图的A、B装置进行实验,片刻后观察,补充并完成下列实验报告的内容。

④1 mol甲烷与足量Cl2发生取代反应时,得到最多的产物是___________ (填化学式)。
Ⅱ. 探究乙烯与溴的加成反应。因实验室制得的乙烯中通常会含有少量的SO2等杂质气体,为此他设计了如图所示的实验装置:

(1)①②装置中可盛放的试剂是:①___________ 、②___________ (填字母)。
A. 品红 B. NaOH溶液 C. 溴水 D. 酸性高锰酸钾溶液
(2)除杂后观察到③中现象为___________ ,写出发生反应的化学方程式___________ 。
通过探究,该同学得出结论:甲烷和乙烯在不同条件下均能与卤素反应。
Ⅲ. 现有H2、Cl2、乙烷、乙烯这四种原料,请你设计一种制取一氯乙烷的最佳实验方案,请用化学方程式表示出来(注意:原料不一定要全部选用)___________ 。
Ⅰ.取2支硬质大试管,通过排饱和食盐水法先后各收集半试管甲烷和半试管氯气。分别用铁架台固定好,按如图的A、B装置进行实验,片刻后观察,补充并完成下列实验报告的内容。

| 实验操作及现象 | 实验结论 | |
| A | ①在漫射日光条件下,试管内: | ③CH4与Cl2在 |
| B | ②迅速剥开黑纸,立即观察:试管内气体颜色为黄绿色 | |
Ⅱ. 探究乙烯与溴的加成反应。因实验室制得的乙烯中通常会含有少量的SO2等杂质气体,为此他设计了如图所示的实验装置:

(1)①②装置中可盛放的试剂是:①
A. 品红 B. NaOH溶液 C. 溴水 D. 酸性高锰酸钾溶液
(2)除杂后观察到③中现象为
通过探究,该同学得出结论:甲烷和乙烯在不同条件下均能与卤素反应。
Ⅲ. 现有H2、Cl2、乙烷、乙烯这四种原料,请你设计一种制取一氯乙烷的最佳实验方案,请用化学方程式表示出来(注意:原料不一定要全部选用)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某研究性学习小组欲探究氯气的化学性质,设计如图所示的实验装置。

已知:该装置气密性良好;铜粉放在耐高温托盘内(防止硬质玻璃管炸裂)。
请回答下列问题:
(1)为防止铜与空气中的氧气反应,在加热之前应该进行的操作为____ 。
(2)当观察到AgNO3溶液中出现白色沉淀时,点燃酒精灯加热;写出AgNO3溶液中生成白色沉淀的化学方程式:____ 。
(3)硬质玻璃管中的反应现象为__ ,反应的化学方程式为___ 。
(4)装置中空试管的作用是____ 。
(5)烧杯中氢氧化钠溶液的作用是___ ,发生反应的化学方程式为____ 。

已知:该装置气密性良好;铜粉放在耐高温托盘内(防止硬质玻璃管炸裂)。
请回答下列问题:
(1)为防止铜与空气中的氧气反应,在加热之前应该进行的操作为
(2)当观察到AgNO3溶液中出现白色沉淀时,点燃酒精灯加热;写出AgNO3溶液中生成白色沉淀的化学方程式:
(3)硬质玻璃管中的反应现象为
(4)装置中空试管的作用是
(5)烧杯中氢氧化钠溶液的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室研究不同价态元素的转化,对于物质的制备和应用至关重要。
(1)实验室可以用如右图所示装置研究S(+6)→S(+4)。
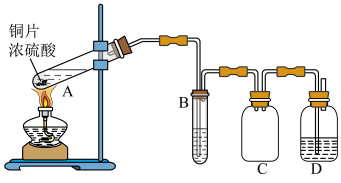
①装置C的作用是___________ ;
②B、D盛放的试剂分别应为___________ 、___________ (填字母标号)
a.BaCl2溶液
b.KI淀粉溶液
c.FeSO4溶液
d.NaOH溶液
e.品红
③实验结束后,发现A中溶液几乎为无色,且试管中有较多的白色固体。试管中溶液显无色,体现了浓硫酸的___________ 性质;
④实验结束后,若要证明A中白色固体为CuSO4,需要采取的操作是___________ 。
(2)硫代硫酸钠(Na2S2O3)是用途广泛的化工产品。某同学欲探究其能否用做脱氯剂(除去游离氯),设计如图所示的实验。
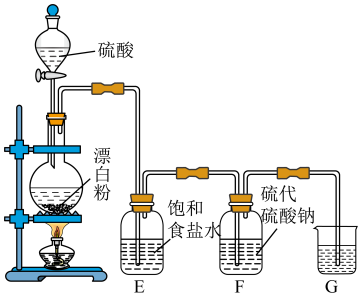
已知:S2O32-+2H+=S↓+SO2↑+H2O
①烧瓶中发生反应的化学方程式为___________ ;
②若要判断Na2S2O3能否做脱氯剂,该同学还需要进行的实验是___________ ;
③I2标准溶液是测定硫代硫酸钠纯度的重要试剂,其浓度可以通过基准物质As2O3来标定:称取a g As2O3置于锥形瓶中,加入适量NaOH恰好将As2O3转化成Na3AsO3,加入淀粉溶液做指示剂,再用I2溶液进行滴定,消耗I2标准溶液体积为v mL。
i.滴定反应(产物之一是AsO43-)的离子方程式为______________________ ;
ii.I2标准溶液的物质的量浓度为___________ 。(用含a、v的代数式表示)
(1)实验室可以用如右图所示装置研究S(+6)→S(+4)。

①装置C的作用是
②B、D盛放的试剂分别应为
a.BaCl2溶液
b.KI淀粉溶液
c.FeSO4溶液
d.NaOH溶液
e.品红
③实验结束后,发现A中溶液几乎为无色,且试管中有较多的白色固体。试管中溶液显无色,体现了浓硫酸的
④实验结束后,若要证明A中白色固体为CuSO4,需要采取的操作是
(2)硫代硫酸钠(Na2S2O3)是用途广泛的化工产品。某同学欲探究其能否用做脱氯剂(除去游离氯),设计如图所示的实验。

已知:S2O32-+2H+=S↓+SO2↑+H2O
①烧瓶中发生反应的化学方程式为
②若要判断Na2S2O3能否做脱氯剂,该同学还需要进行的实验是
③I2标准溶液是测定硫代硫酸钠纯度的重要试剂,其浓度可以通过基准物质As2O3来标定:称取a g As2O3置于锥形瓶中,加入适量NaOH恰好将As2O3转化成Na3AsO3,加入淀粉溶液做指示剂,再用I2溶液进行滴定,消耗I2标准溶液体积为v mL。
i.滴定反应(产物之一是AsO43-)的离子方程式为
ii.I2标准溶液的物质的量浓度为
您最近一年使用:0次



