吉林省吉林市2024届高三下学期第四次模拟考试化学试题
吉林
高三
模拟预测
2024-05-18
225次
整体难度:
适中
考查范围:
物质结构与性质、有机化学基础、化学与STSE、化学反应原理、认识化学科学、常见无机物及其应用、化学实验基础
吉林省吉林市2024届高三下学期第四次模拟考试化学试题
吉林
高三
模拟预测
2024-05-18
225次
整体难度:
适中
考查范围:
物质结构与性质、有机化学基础、化学与STSE、化学反应原理、认识化学科学、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
1. 化学与生活、生产密切相关。下列叙述错误的是
| A.误服氯化钡应大量吞食牛奶、生蛋清,还应加服纯碱解毒 |
| B.广泛pH试纸不能准确测得“84”消毒液的pH |
| C.CO2排放量的增加将破坏海洋珊瑚礁(主要成分CaCO3)的生存 |
| D.节日燃放烟花是利用金属的焰色试验,这与原子核外电子跃迁有关 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
3. 按照国家绿色发展规划,与化学化工相关的新质生产力涉及了“新能源”“绿色低碳” “新材料”等问题。下列有关说法错误的是

| A.潮汐能、波浪能、生物质能和氢能均属于新型能源 |
| B.“绿色低碳”是指采用含碳量低的烃类作为燃料 |
| C.如图甲烷经一氯甲烷生成低碳烯烃的途径体现了“节能减排”思想 |
| D.国产红旗轿车中部分材料采用了碳纤维,碳纤维属于新型无机非金属材料 |
【知识点】 新型无机非金属材料 绿色化学与可持续发展解读
您最近一年使用:0次
4. 臭氧能氧化CN-,故常被用来治理电镀工业中的含氰废水,其化学反应原理为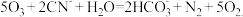 下列说法正确的是
下列说法正确的是
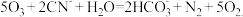 下列说法正确的是
下列说法正确的是| A.O3和O2互为同位素关系 |
| B.该反应是熵减的过程 |
| C.该反应中,每生成1 mol N2转移6 mol电子 |
| D.反应中所涉及的N2、O2为非极性分子,O3为极性分子 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
5. 能正确表示下列反应的离子方程式为
A.明矾溶液与过量氨水混合: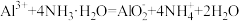 |
| B.氯水久置颜色逐渐褪去:4Cl2+4H2O = HClO4+7HCl |
C.用Na2S2O3做碘量法实验时,pH过低溶液变浑浊: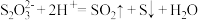 |
D.苯酚钠溶液中通入少量CO2,出现白色浑浊:2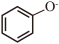 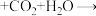 2 2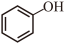 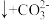 |
您最近一年使用:0次
单选题
|
适中(0.65)
6. NO2和N2O4存在平衡:2NO2(g) N2O4(g) ΔH<0。下列分析正确的是
N2O4(g) ΔH<0。下列分析正确的是
 N2O4(g) ΔH<0。下列分析正确的是
N2O4(g) ΔH<0。下列分析正确的是| A.常温下,11.2LNO2和N2O4混合气体的物质的量为0.5mol |
| B.断裂2molNO2中的共价键所需能量小于断裂1molN2O4中的共价键所需能量 |
| C.恒温时,缩小容积,平衡正向移动,气体颜色变浅 |
| D.恒容时,水浴加热,气体颜色变浅 |
【知识点】 温度对化学平衡移动的影响解读 压强对化学平衡移动的影响解读
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
7. 维生素A又称视黄醇或抗干眼病因子,人体缺乏维生素A会出现皮肤干燥、夜盲症等症状。其结构简式如图所示,下列说法正确的是

| A.维生素A的分子式为C20H28O |
| B.该分子与足量H2反应生成的有机化合物中含有3个手性碳原子 |
| C.该分子能发生取代反应、加成反应、氧化反应、加聚反应 |
| D.维生素A是易溶于水的醇 |
【知识点】 有机官能团的性质及结构 多官能团有机物的结构与性质解读
您最近一年使用:0次
单选题
|
较易(0.85)
8. 某化学兴趣小组利用如图所示装置进(电化学实验(C、D、E、F为铂夹)。断开K3,闭合K1、K2,反应一段时间后,A、B两试管中共收集到气体336mL(折算为标准状况)。再断开K2,闭合K1、K3后,下列说法正确的是

| A.电源放电时,电极a的电势比b的低 |
| B.滤纸1的D电极附近橙红色变黄 |
| C.试管B中电极反应为O2+4e-+2H2O=4OH- |
| D.滤纸2上理论上能析出3.24gAg |
您最近一年使用:0次
单选题
|
适中(0.65)
9. 我国科学家成功合成了世界上首个五氮阴离子盐,局部结构如图所示。其中含有两种10电子离子、一种18电子离子,W、X、Y、Z为原子序数依次增大的短周期元素,Z的单质可以用于自来水消毒,图中虚线表示氢键。下列说法正确的是
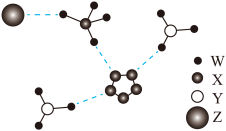
| A.五氮阴离子盐中两种阳离子的立体结构相同 |
| B.X、Y、Z对应的最简单氢化物中沸点最高的是X |
| C.Z的氧化物对应的水化物均为强酸 |
D.五氮阴离子盐中含有的大π键为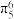 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
11. 微生物脱盐电池既可以处理废水中的乙酸和铵盐,又可以实现海水淡化,原理如图所示。下列说法正确的是
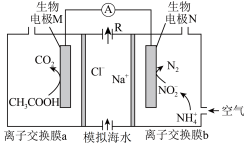
| A.离子交换膜a为阳离子交换膜,b为阴离子交换膜 |
| B.出口R处一定为纯水 |
| C.生成CO2的电极反应式为CH3COOH+2H2O-8e- = 2CO2↑+8H+ |
| D.M极每生成0.1mol CO2,理论上可以从模拟海水中除去117gNaCl |
您最近一年使用:0次
单选题
|
适中(0.65)
12. 分子结构修饰在药物设计与合成中有广泛的应用。某新型合成药物的中间体结构如图所示,科学家需要对其进行成酯修饰后患者才能服用。已知连在同一碳上的两个羟基易脱水,下列说法正确的是
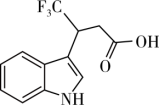
| A.对该化合物分子进行成酯修饰目的是增强其水溶性 |
| B.分析该化合物的质谱图,可获得分子中含有的官能团的信息 |
| C.1mol该化合物最多与4molNaOH反应 |
| D.该化合物分子中最多有11个碳原子共平面 |
您最近一年使用:0次
单选题
|
适中(0.65)
13. 有一种有超导性的硼镁化合物,其晶体结构、晶胞沿c轴的投影图如图所示,已知在投影图中,B位于三个Mg形成的正三角形的中心,阿伏加德罗常数值为NA,图中长度单位均为厘米,关于其晶体下列说法正确的是
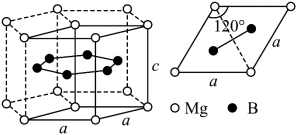
| A.该化合物的化学式为Mg3B2 |
| B.该晶体中Mg的配位数为8 |
| C.每个B原子周围都有2个与之等距离且最近的B原子 |
D.该晶体的密度为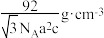 |
您最近一年使用:0次
单选题
|
适中(0.65)
14. 类比pH,对于稀溶液pc=-lgc,pKa=-lgKa.常温下,向某浓度H2A溶液中加入NaOH(s),保持溶液体积和温度不变,测得pH与pc(H2A)、pc(HA-)、pc(A2-)变化如图所示。下列说法正确的是
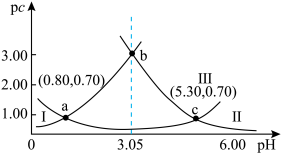
| A.pH=3.05时,c(HA-)>c(A2-)>c(H2A) |
| B.Ka1(H2A)的数量级为10-6 |
| C.c点时,c(Na+)=(10-8.70+3×10-0.7-10-5.30 ) mol·L-1 |
| D.若醋酸的pKa=4.76,则HA-与CH3COO-不能大量共存 |
您最近一年使用:0次
单选题
|
适中(0.65)
15. 镍电池芯废料中主要含有金属镍,还含有金属钴、铁、铝。一种从镍电池芯废料中回收金属的工艺流程如下:
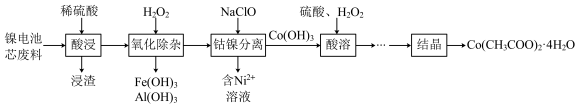
| A.“酸浸”时,若改用浓硫酸,反应速率更快,效果更好 |
| B.H2O2在“氧化除杂”和“酸溶”中的作用相同 |
| C.“酸溶”时,为了加快反应速率,可以采取高温条件 |
| D.“结晶”时,应加热至出现少量晶膜时,再冷却结晶 |
【知识点】 有关铁及其化合物转化的流程题型解读 常见无机物的制备解读
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
较难(0.4)
解题方法
16. 芳基亚胺酯是重要的有机反应中间体,受热易分解,可由腈在酸催化下与醇发生Pinner反应制备,原理如下图所示。
Ⅱ.向容器中持续通入HCl气体4小时,密封容器。
Ⅲ.室温下在HCl氛围中继续搅拌反应液24小时,冷却至0℃,抽滤得白色固体,用乙腈洗涤。
Ⅳ.将洗涤后的白色固体加入饱和Na2CO3溶液中,在15℃低温下反应,用有机溶剂萃取3次,合并有机相。
V.向有机相中加入无水硫酸钠,抽滤,蒸去溶剂得产品19.50g。
回答下列问题:
(1)实验室中可用浓盐酸和浓硫酸制备干燥HCl气体,下列仪器中一定需要的为_______ (填仪器名称)。_______ (填标号)。_______ ;实验中选择低温的原因为_______ 。
(4)第Ⅳ步萃取时可选用的有机溶剂为_______(填标号)。
(5)第Ⅳ将洗涤后的白色固体加入饱和Na2CO3溶液中,饱和Na2CO3的作用是_______ 。
(6)抽滤装置如下图所示,其相对于普通过滤的优点是_______ 。
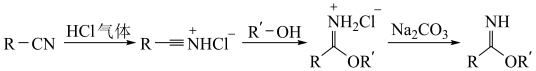
某实验小组以苯甲腈(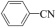 )和三氟乙醇(CF3CH2OH)为原料合成苯甲亚胺三氟乙酯。步骤如下:
)和三氟乙醇(CF3CH2OH)为原料合成苯甲亚胺三氟乙酯。步骤如下:
Ⅱ.向容器中持续通入HCl气体4小时,密封容器。
Ⅲ.室温下在HCl氛围中继续搅拌反应液24小时,冷却至0℃,抽滤得白色固体,用乙腈洗涤。
Ⅳ.将洗涤后的白色固体加入饱和Na2CO3溶液中,在15℃低温下反应,用有机溶剂萃取3次,合并有机相。
V.向有机相中加入无水硫酸钠,抽滤,蒸去溶剂得产品19.50g。
回答下列问题:
(1)实验室中可用浓盐酸和浓硫酸制备干燥HCl气体,下列仪器中一定需要的为

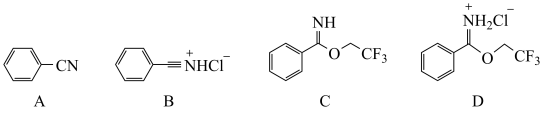
(4)第Ⅳ步萃取时可选用的有机溶剂为_______(填标号)。
| A.甲醇 | B.乙酸 | C.丙酮 | D.乙酸乙酯 |
(5)第Ⅳ将洗涤后的白色固体加入饱和Na2CO3溶液中,饱和Na2CO3的作用是
(6)抽滤装置如下图所示,其相对于普通过滤的优点是
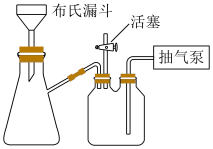
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
解题方法
17. 我国是最早制得和使用金属锌的国家。某湿法炼锌的萃余液中含有H+、Na+、Zn2+、Fe2+、Mn2+、Co2+、Cd2+、Ni2+、 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
回答下列问题:
(1)按照核外电子排布可把元素周期表分成5个区,Zn元素在_______ 区。
(2)“氧化”时,pH=1,所用氧化剂过二硫酸钠(Na2S2O8)中硫元素化合价为_______ ,Mn2+被氧化为MnO2,Fe2+与Na2S2O8反应的离子方程式是_______ 。
(3)“调pH”时,pH=4,所得滤渣1中除含有MnO2外,还有_______ 。
(4)“除钴镍”时,有机净化剂的基本组分为大分子立体网格结构的聚合物,其净化原理可表示为: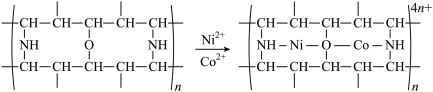 ,Co2+、Ni2+能发生上述转化而Zn2+不能,推测可能的原因为
,Co2+、Ni2+能发生上述转化而Zn2+不能,推测可能的原因为_____ 。
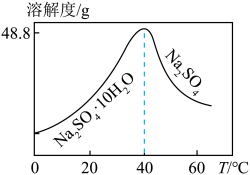
(5)“沉锌” 所得滤液经处理可得Na2SO4溶液,已知Na2SO4的溶解度随温度变化如图所示,由该溶液制备无水Na2SO4的操作为_____ 、洗涤、干燥。_____ 。
 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图: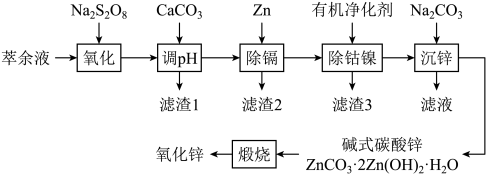
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 |
| Ksp近似值 | 10-38 | 10-17 | 10-17 |
(1)按照核外电子排布可把元素周期表分成5个区,Zn元素在
(2)“氧化”时,pH=1,所用氧化剂过二硫酸钠(Na2S2O8)中硫元素化合价为
(3)“调pH”时,pH=4,所得滤渣1中除含有MnO2外,还有
(4)“除钴镍”时,有机净化剂的基本组分为大分子立体网格结构的聚合物,其净化原理可表示为:
 ,Co2+、Ni2+能发生上述转化而Zn2+不能,推测可能的原因为
,Co2+、Ni2+能发生上述转化而Zn2+不能,推测可能的原因为(5)“沉锌” 所得滤液经处理可得Na2SO4溶液,已知Na2SO4的溶解度随温度变化如图所示,由该溶液制备无水Na2SO4的操作为
您最近一年使用:0次
18. 绿色能源是未来能源发展的重要方向,氢能是重要的绿色能源。
(1)氢气是一种环保的气体,不会污染大气且热值高。已知:H2O(g)=H2O(l) ΔH=-44 kJ·mol-1,相关化学键的键能表示如下:
表示氢气燃烧热的热化学方程式_______ 。
(2)催化制氢是目前大规模制取氢气的方法之一:CO(g)+H2O(g) CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1。在T1℃时,将0.10 mol CO与0.40 mol H2O充入5 L的容器中,反应平衡后CO的物质的量分数x(CO)=0.12。
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1。在T1℃时,将0.10 mol CO与0.40 mol H2O充入5 L的容器中,反应平衡后CO的物质的量分数x(CO)=0.12。_______ %。
②由T1℃时上述实验数据计算得到v正~x(CO)和v逆~x(H2)的关系可用图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为_______ (填字母)。
③研究表明,一氧化碳催化变换反应的速率方程为: ],Kp为平衡常数,k为反应的速率常数,在气体组成和催化剂一定的情况下,反应速率与温度变化的关系曲线如图所示。温度升高时,CO催化变换反应的Kp
],Kp为平衡常数,k为反应的速率常数,在气体组成和催化剂一定的情况下,反应速率与温度变化的关系曲线如图所示。温度升高时,CO催化变换反应的Kp_______ (填“增大”“减小”或“不变”),根据速率方程分析,T>Tm时,v逐渐减小的原因是_______ 。 CH4(g)+2H2O(g),在一定条件下该反应存在:v正(H2)=k1·c4(H2)·c(CO2),v逆(H2O)= k2·c2(H2O)·c(CH4),可知k1·c4(H2)·c(CO2)=k2·c2(H2O)·c(CH4),则该反应的平衡常数K=
CH4(g)+2H2O(g),在一定条件下该反应存在:v正(H2)=k1·c4(H2)·c(CO2),v逆(H2O)= k2·c2(H2O)·c(CH4),可知k1·c4(H2)·c(CO2)=k2·c2(H2O)·c(CH4),则该反应的平衡常数K=____ (用含k1,k2的代数式表示)。
(4)光催化H2O制H2技术也是研究热点。光催化材料还原H2O的机理如图所示,光照时,低能价带失去电子并产生空穴(h+,具有强氧化性)。在低能价带上,H2O直接转化为O2的电极反应式为_______ 。
(1)氢气是一种环保的气体,不会污染大气且热值高。已知:H2O(g)=H2O(l) ΔH=-44 kJ·mol-1,相关化学键的键能表示如下:
| 化学键 | O=O | H-H | O-H |
| 键能E/(kJ·mol-1) | 497 | 436 | 463 |
(2)催化制氢是目前大规模制取氢气的方法之一:CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1。在T1℃时,将0.10 mol CO与0.40 mol H2O充入5 L的容器中,反应平衡后CO的物质的量分数x(CO)=0.12。
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1。在T1℃时,将0.10 mol CO与0.40 mol H2O充入5 L的容器中,反应平衡后CO的物质的量分数x(CO)=0.12。
②由T1℃时上述实验数据计算得到v正~x(CO)和v逆~x(H2)的关系可用图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为
③研究表明,一氧化碳催化变换反应的速率方程为:
 ],Kp为平衡常数,k为反应的速率常数,在气体组成和催化剂一定的情况下,反应速率与温度变化的关系曲线如图所示。温度升高时,CO催化变换反应的Kp
],Kp为平衡常数,k为反应的速率常数,在气体组成和催化剂一定的情况下,反应速率与温度变化的关系曲线如图所示。温度升高时,CO催化变换反应的Kp
 CH4(g)+2H2O(g),在一定条件下该反应存在:v正(H2)=k1·c4(H2)·c(CO2),v逆(H2O)= k2·c2(H2O)·c(CH4),可知k1·c4(H2)·c(CO2)=k2·c2(H2O)·c(CH4),则该反应的平衡常数K=
CH4(g)+2H2O(g),在一定条件下该反应存在:v正(H2)=k1·c4(H2)·c(CO2),v逆(H2O)= k2·c2(H2O)·c(CH4),可知k1·c4(H2)·c(CO2)=k2·c2(H2O)·c(CH4),则该反应的平衡常数K=(4)光催化H2O制H2技术也是研究热点。光催化材料还原H2O的机理如图所示,光照时,低能价带失去电子并产生空穴(h+,具有强氧化性)。在低能价带上,H2O直接转化为O2的电极反应式为

您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
19. 化合物 是合成抗病毒药物普拉那韦的原料,其合成路线如下。
是合成抗病毒药物普拉那韦的原料,其合成路线如下。_______ 。
(2)D的化学名称为_______ 。
(3)E→F的反应类型为_______ 。
(4)J的结构简式为_______ 。
(5)M分子中含有两个六元环,则 →M的反应方程式为
→M的反应方程式为_______ 。
(6)在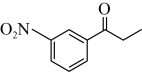 的同分异构体中,满足下列条件的结构有
的同分异构体中,满足下列条件的结构有_______ 种(不考虑立体异构)。
①核磁共振氢谱有5组峰
②遇FeCl3溶液显色
③1mol该物质与银氨溶液反应,最多可生成4molAg
写出其中一种结构简式:_______ 。
 是合成抗病毒药物普拉那韦的原料,其合成路线如下。
是合成抗病毒药物普拉那韦的原料,其合成路线如下。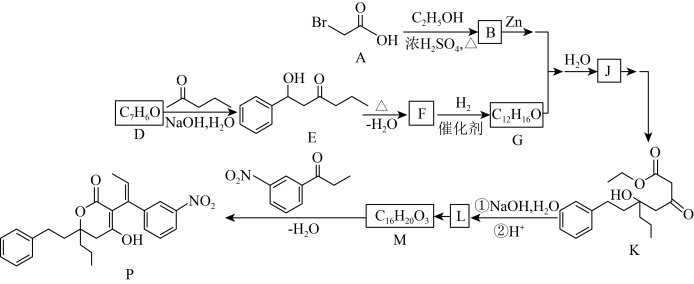
已知: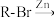
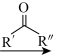

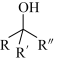
(2)D的化学名称为
(3)E→F的反应类型为
(4)J的结构简式为
(5)M分子中含有两个六元环,则
 →M的反应方程式为
→M的反应方程式为(6)在
 的同分异构体中,满足下列条件的结构有
的同分异构体中,满足下列条件的结构有①核磁共振氢谱有5组峰
②遇FeCl3溶液显色
③1mol该物质与银氨溶液反应,最多可生成4molAg
写出其中一种结构简式:
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:物质结构与性质、有机化学基础、化学与STSE、化学反应原理、认识化学科学、常见无机物及其应用、化学实验基础
试卷题型(共 19题)
题型
数量
单选题
15
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 电子基态与激发态 | |
| 2 | 0.65 | 分子的手性 含有氢键的物质 | |
| 3 | 0.65 | 新型无机非金属材料 绿色化学与可持续发展 | |
| 4 | 0.65 | 化学反应进行方向的判据 几组常见同素异形体 极性分子和非极性分子 电子转移计算 | |
| 5 | 0.65 | 离子方程式的书写 离子方程式的正误判断 苯酚的弱酸性 | |
| 6 | 0.65 | 温度对化学平衡移动的影响 压强对化学平衡移动的影响 | |
| 7 | 0.94 | 有机官能团的性质及结构 多官能团有机物的结构与性质 | |
| 8 | 0.85 | 原电池电极反应式书写 原电池、电解池综合考查 电解池有关计算 | |
| 9 | 0.65 | 元素周期律、元素周期表的推断 杂化轨道理论 价层电子对互斥理论的应用 氢键对物质性质的影响 | |
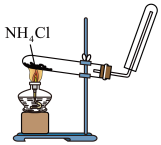
| 10 | 0.65 | 氨气的实验室制法 二氧化氮与水反应 配合物 | |
| 11 | 0.65 | 原电池正负极判断 原电池电极反应式书写 电解原理的应用 原电池有关计算 | |
| 12 | 0.65 | 卤代烃的水解反应 羧酸的酸性 | |
| 13 | 0.65 | 简单配合物的成键 晶胞的有关计算 | |
| 14 | 0.65 | 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 弱电解质的电离平衡常数 | |
| 15 | 0.65 | 有关铁及其化合物转化的流程题型 常见无机物的制备 | |
| 二、解答题 | |||
| 16 | 0.4 | 常用仪器及使用 物质分离、提纯综合应用 常见有机物的制备 | 实验探究题 |
| 17 | 0.65 | 溶度积常数相关计算 电解池电极反应式及化学方程式的书写与判断 元素周期表结构分析 物质制备的探究 | 工业流程题 |
| 18 | 0.65 | 根据△H=反应物的键能之和-生成物的键能之和进行计算 化学平衡常数的影响因素及应用 化学平衡常数的有关计算 原电池电极反应式书写 | 原理综合题 |
| 19 | 0.4 | 根据要求书写同分异构体 醛基的加成反应 羧酸酯化反应 有机合成综合考查 | 有机推断题 |


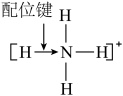
 的结构式
的结构式
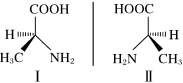
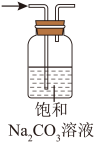
 中混有的少量HCl
中混有的少量HCl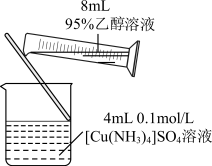
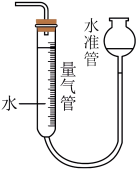

 体积
体积

