我国是最早制得和使用金属锌的国家。某湿法炼锌的萃余液中含有H+、Na+、Zn2+、Fe2+、Mn2+、Co2+、Cd2+、Ni2+、 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
回答下列问题:
(1)按照核外电子排布可把元素周期表分成5个区,Zn元素在_______ 区。
(2)“氧化”时,pH=1,所用氧化剂过二硫酸钠(Na2S2O8)中硫元素化合价为_______ ,Mn2+被氧化为MnO2,Fe2+与Na2S2O8反应的离子方程式是_______ 。
(3)“调pH”时,pH=4,所得滤渣1中除含有MnO2外,还有_______ 。
(4)“除钴镍”时,有机净化剂的基本组分为大分子立体网格结构的聚合物,其净化原理可表示为: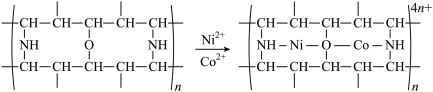 ,Co2+、Ni2+能发生上述转化而Zn2+不能,推测可能的原因为
,Co2+、Ni2+能发生上述转化而Zn2+不能,推测可能的原因为_____ 。
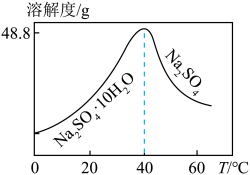
(5)“沉锌” 所得滤液经处理可得Na2SO4溶液,已知Na2SO4的溶解度随温度变化如图所示,由该溶液制备无水Na2SO4的操作为_____ 、洗涤、干燥。_____ 。
 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图: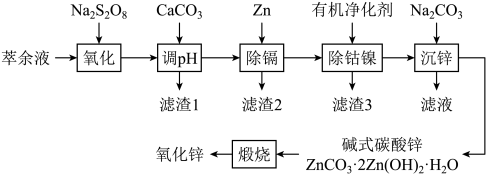
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 |
| Ksp近似值 | 10-38 | 10-17 | 10-17 |
(1)按照核外电子排布可把元素周期表分成5个区,Zn元素在
(2)“氧化”时,pH=1,所用氧化剂过二硫酸钠(Na2S2O8)中硫元素化合价为
(3)“调pH”时,pH=4,所得滤渣1中除含有MnO2外,还有
(4)“除钴镍”时,有机净化剂的基本组分为大分子立体网格结构的聚合物,其净化原理可表示为:
 ,Co2+、Ni2+能发生上述转化而Zn2+不能,推测可能的原因为
,Co2+、Ni2+能发生上述转化而Zn2+不能,推测可能的原因为(5)“沉锌” 所得滤液经处理可得Na2SO4溶液,已知Na2SO4的溶解度随温度变化如图所示,由该溶液制备无水Na2SO4的操作为
更新时间:2024-05-19 07:49:43
|
相似题推荐
【推荐1】工业废水中常含有一定量的 ,会危害生态系统,必须进行处理。
,会危害生态系统,必须进行处理。
方法 I:转化为Cr(OH)SO4,Cr(OH)SO4是纺织印染中常用的媒染剂,变废为宝。该法用酸性含铬废液(含 、Cr3+及少量Cu2+、Fe3+等)制备Cr(OH)SO4·nH2O 晶体,工艺流程如下:
、Cr3+及少量Cu2+、Fe3+等)制备Cr(OH)SO4·nH2O 晶体,工艺流程如下:

已知相关金属离子[c(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下
回答下列问题
(1)“氧化”时 Cr3+在 Ag+催化下氧化为 ,完成下列离子方程式:
,完成下列离子方程式:______ 。
______Cr3++ ______ + ______
+ ______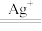 ______
______ + ______
+ ______ +______
+______
(2)将Cr3+氧化为 的目的是
的目的是______ 。
(3)“调 pH”目的是除去______ 。
(4)从Cr(OH)SO4溶液得到Cr(OH)SO4·nH2O晶体,还需进行的操作为:______ 、 ______ 、过滤、洗涤、干燥。
方法 II:电解转化为Cr(OH)3沉淀,从而使铬含量低于排放标准。该法以Fe为电极电解含 的酸性废水,装置如图所示:
的酸性废水,装置如图所示:

(5)B是电源的______ 极,阳极的电极反应式为______ 。
(6)废水中的 转化为Cr(OH)3沉淀的主要原因是
转化为Cr(OH)3沉淀的主要原因是 与阳极产物发生反应生成 Cr3+,该反应的离子方程式为:
与阳极产物发生反应生成 Cr3+,该反应的离子方程式为:______ ,电解过程中消耗了大量H+,使得溶液产生 Cr(OH)3和Fe(OH)3沉淀。
 ,会危害生态系统,必须进行处理。
,会危害生态系统,必须进行处理。 方法 I:转化为Cr(OH)SO4,Cr(OH)SO4是纺织印染中常用的媒染剂,变废为宝。该法用酸性含铬废液(含
 、Cr3+及少量Cu2+、Fe3+等)制备Cr(OH)SO4·nH2O 晶体,工艺流程如下:
、Cr3+及少量Cu2+、Fe3+等)制备Cr(OH)SO4·nH2O 晶体,工艺流程如下: 
已知相关金属离子[c(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下
| 离子 | 开始沉淀的pH | 沉淀完全 |
| Fe3+ | 1.4 | 3.0 |
| Cu2+ | 4.2 | 6.7 |
| Cr3+ | 4.0 | 6.8 |
(1)“氧化”时 Cr3+在 Ag+催化下氧化为
 ,完成下列离子方程式:
,完成下列离子方程式:______Cr3++ ______
 + ______
+ ______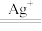 ______
______ + ______
+ ______ +______
+______(2)将Cr3+氧化为
 的目的是
的目的是(3)“调 pH”目的是除去
(4)从Cr(OH)SO4溶液得到Cr(OH)SO4·nH2O晶体,还需进行的操作为:
方法 II:电解转化为Cr(OH)3沉淀,从而使铬含量低于排放标准。该法以Fe为电极电解含
 的酸性废水,装置如图所示:
的酸性废水,装置如图所示:
(5)B是电源的
(6)废水中的
 转化为Cr(OH)3沉淀的主要原因是
转化为Cr(OH)3沉淀的主要原因是 与阳极产物发生反应生成 Cr3+,该反应的离子方程式为:
与阳极产物发生反应生成 Cr3+,该反应的离子方程式为:
您最近一年使用:0次
【推荐2】某兴趣小组用含镍废催化剂(主要含有 ,还含有
,还含有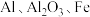 及其他不溶于酸、碱的杂质)制备
及其他不溶于酸、碱的杂质)制备 ,其流程如下:
,其流程如下: 近似值如表所示;已知:
近似值如表所示;已知: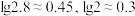 。
。
回答下列问题:
(1)加 溶液进行浸出时搅拌可提高浸出速率,原因为
溶液进行浸出时搅拌可提高浸出速率,原因为___________ ,“滤液1”中含有的主要阴离子为___________ (填化学式)。
(2)加入 “氧化”时发生反应的离子方程式为
“氧化”时发生反应的离子方程式为___________ 。
(3)“除杂”时加 调节溶液的
调节溶液的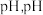 需大于
需大于_______ ,(保留1位小数,离子浓度 时认为该离子沉淀完全),简述加
时认为该离子沉淀完全),简述加 调节溶液的
调节溶液的 除杂的原理:
除杂的原理:_______ 。
(4)“一系列操作”主要包括___________ 、___________ 、过滤、洗涤、干燥等。
 ,还含有
,还含有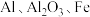 及其他不溶于酸、碱的杂质)制备
及其他不溶于酸、碱的杂质)制备 ,其流程如下:
,其流程如下: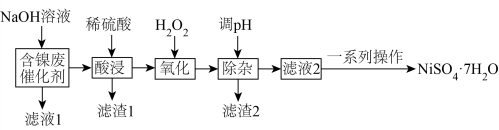
 近似值如表所示;已知:
近似值如表所示;已知: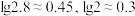 。
。| 化学式 |  |  |  |
 近似值 近似值 |  |  | 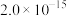 |
(1)加
 溶液进行浸出时搅拌可提高浸出速率,原因为
溶液进行浸出时搅拌可提高浸出速率,原因为(2)加入
 “氧化”时发生反应的离子方程式为
“氧化”时发生反应的离子方程式为(3)“除杂”时加
 调节溶液的
调节溶液的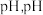 需大于
需大于 时认为该离子沉淀完全),简述加
时认为该离子沉淀完全),简述加 调节溶液的
调节溶液的 除杂的原理:
除杂的原理:(4)“一系列操作”主要包括
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
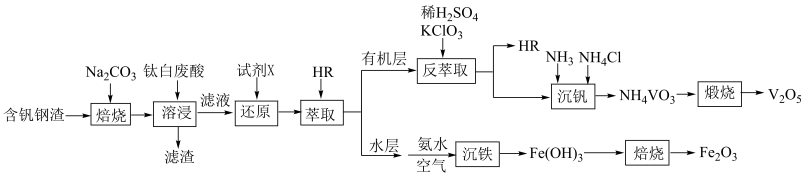
【推荐3】以含钒钢渣(含 、
、 和少量
和少量 、
、 )和钛白废酸(含
)和钛白废酸(含 、
、 、
、 、
、 )为原料提取钒,实现“以废治废”。工艺流程如图:
)为原料提取钒,实现“以废治废”。工艺流程如图:
已知:有机萃取剂 的萃取原理为
的萃取原理为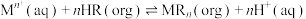 ,其中
,其中 表示有机溶液,酸性条件下
表示有机溶液,酸性条件下 能萃取
能萃取 而不能萃取
而不能萃取 ,
, 对+4价钒萃取能力强,而对+5价钒的萃取能力较弱。
对+4价钒萃取能力强,而对+5价钒的萃取能力较弱。
回答下列问题:
(1)在空气中“焙烧”时, 转化为
转化为 的化学方程式为
的化学方程式为___________ 。
(2)“溶浸”时生成的滤渣除了 外,还有
外,还有___________ (填化学式)。
(3)“还原”的目的是将溶液中的+5价钒和 分别转化为+4价钒与
分别转化为+4价钒与 ,利于+4价钒的萃取并实现钒和铁元素分离,加入的化学试剂
,利于+4价钒的萃取并实现钒和铁元素分离,加入的化学试剂 可能为___________(填标号)。
可能为___________(填标号)。
(4)在“萃取”操作后从水层中获得 的离子方程式是
的离子方程式是___________ 。
(5)在“反萃取”操作中 和
和 反应生成
反应生成 和
和 ,反应中氧化剂与还原剂的物质的量之比为
,反应中氧化剂与还原剂的物质的量之比为___________ 。
(6)上述流程中可循环利用的物质除 外,还有
外,还有___________ (填化学式)。
(7)常温“沉钒”,维持溶液中 的总浓度为
的总浓度为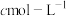 ,
, 。“沉钒”后溶液中
。“沉钒”后溶液中
___________  [已知
[已知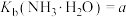 ;
; ]。
]。
 、
、 和少量
和少量 、
、 )和钛白废酸(含
)和钛白废酸(含 、
、 、
、 、
、 )为原料提取钒,实现“以废治废”。工艺流程如图:
)为原料提取钒,实现“以废治废”。工艺流程如图:
已知:有机萃取剂
 的萃取原理为
的萃取原理为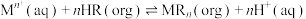 ,其中
,其中 表示有机溶液,酸性条件下
表示有机溶液,酸性条件下 能萃取
能萃取 而不能萃取
而不能萃取 ,
, 对+4价钒萃取能力强,而对+5价钒的萃取能力较弱。
对+4价钒萃取能力强,而对+5价钒的萃取能力较弱。回答下列问题:
(1)在空气中“焙烧”时,
 转化为
转化为 的化学方程式为
的化学方程式为(2)“溶浸”时生成的滤渣除了
 外,还有
外,还有(3)“还原”的目的是将溶液中的+5价钒和
 分别转化为+4价钒与
分别转化为+4价钒与 ,利于+4价钒的萃取并实现钒和铁元素分离,加入的化学试剂
,利于+4价钒的萃取并实现钒和铁元素分离,加入的化学试剂 可能为___________(填标号)。
可能为___________(填标号)。A. | B. | C. | D. |
(4)在“萃取”操作后从水层中获得
 的离子方程式是
的离子方程式是(5)在“反萃取”操作中
 和
和 反应生成
反应生成 和
和 ,反应中氧化剂与还原剂的物质的量之比为
,反应中氧化剂与还原剂的物质的量之比为(6)上述流程中可循环利用的物质除
 外,还有
外,还有(7)常温“沉钒”,维持溶液中
 的总浓度为
的总浓度为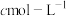 ,
, 。“沉钒”后溶液中
。“沉钒”后溶液中
 [已知
[已知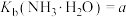 ;
; ]。
]。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】利用 加氢制甲醇等清洁燃料,是实现
加氢制甲醇等清洁燃料,是实现 减排较为可行的方法。一定温度下,
减排较为可行的方法。一定温度下, 和
和 在催化剂作用下可发生以下两个反应:
在催化剂作用下可发生以下两个反应:
反应Ⅰ:

反应Ⅱ:

(1)相同温度下,反应 的
的
_______ 。
(2)在催化、恒压条件下,向密闭容器中投入一定量 和
和 。其他条件相同,升高温度,判断甲醇选择性以及
。其他条件相同,升高温度,判断甲醇选择性以及 的平衡转化率的变化,并说明理由:
的平衡转化率的变化,并说明理由:_______ 。已知: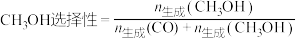 。
。
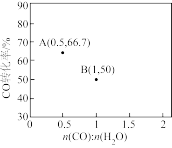
(3)氢气可通过水煤气法获得,原理为 。在进气比
。在进气比 不同时,测得平衡时CO转化率如图,A和B两点对应的温度关系:
不同时,测得平衡时CO转化率如图,A和B两点对应的温度关系:
_______  (填“<”、“>”、或“=”),判断的理由是
(填“<”、“>”、或“=”),判断的理由是_______ 。
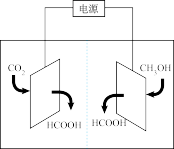
(4)如图装置可将 和甲醇转化为甲酸。阳极的电极反应式为
和甲醇转化为甲酸。阳极的电极反应式为_______ 。
(5) 加氢制甲醇的部分反应机理如图所示。
加氢制甲醇的部分反应机理如图所示。

“ ”表示物质在催化剂表面被吸附,“
”表示物质在催化剂表面被吸附,“ ”表示自由基中未成对电子。已知
”表示自由基中未成对电子。已知 在催化剂表面会形成两种吸附态的H,一种显正电性,一种显负电性。
在催化剂表面会形成两种吸附态的H,一种显正电性,一种显负电性。
①根据元素的电负性变化规律分析,过程ⅰ中参与反应的显正电性与显负电性氢原子的数目比为_______ ;
②结合化学键的断裂和形成,过程ⅱ可描述为_______ 。
 加氢制甲醇等清洁燃料,是实现
加氢制甲醇等清洁燃料,是实现 减排较为可行的方法。一定温度下,
减排较为可行的方法。一定温度下, 和
和 在催化剂作用下可发生以下两个反应:
在催化剂作用下可发生以下两个反应:反应Ⅰ:


反应Ⅱ:


(1)相同温度下,反应
 的
的
(2)在催化、恒压条件下,向密闭容器中投入一定量
 和
和 。其他条件相同,升高温度,判断甲醇选择性以及
。其他条件相同,升高温度,判断甲醇选择性以及 的平衡转化率的变化,并说明理由:
的平衡转化率的变化,并说明理由: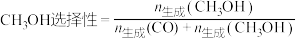 。
。(3)氢气可通过水煤气法获得,原理为
 。在进气比
。在进气比 不同时,测得平衡时CO转化率如图,A和B两点对应的温度关系:
不同时,测得平衡时CO转化率如图,A和B两点对应的温度关系:
 (填“<”、“>”、或“=”),判断的理由是
(填“<”、“>”、或“=”),判断的理由是
(4)如图装置可将
 和甲醇转化为甲酸。阳极的电极反应式为
和甲醇转化为甲酸。阳极的电极反应式为
(5)
 加氢制甲醇的部分反应机理如图所示。
加氢制甲醇的部分反应机理如图所示。
“
 ”表示物质在催化剂表面被吸附,“
”表示物质在催化剂表面被吸附,“ ”表示自由基中未成对电子。已知
”表示自由基中未成对电子。已知 在催化剂表面会形成两种吸附态的H,一种显正电性,一种显负电性。
在催化剂表面会形成两种吸附态的H,一种显正电性,一种显负电性。①根据元素的电负性变化规律分析,过程ⅰ中参与反应的显正电性与显负电性氢原子的数目比为
②结合化学键的断裂和形成,过程ⅱ可描述为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】2016年10月17日7点30分,神舟十一号载人飞船发射升空。制造航天飞船的主要材料是铝,工业上制铝时用冰晶石(Na3AlF6)做助熔剂,冰晶石制备流程有如下两种:
方案一:以纯碱和萤石(CaF2)为主要原料
方案二:以碳酸氢铵和六氟合硅酸为主要原料

(1)方案一中B可作为建筑材料,化合物A 是________ ,写出由C制备冰晶石的化学方程式__________________ 。
(2)方案二中反应1产生的气体是_____________ ,反应2后滤液中主要成分的用途_________ 。
(3)方案二中反应2化学方程式______________________ 。
(4)工业电解制铝的阴极反应式为_________________ ,以石墨为电极维持电流180千安电解5小时生成铝270千克,则电流效率η(η=实际产量/理论产量)为_______ 。(法拉第常数F = 96500 C·mol-1)
方案一:以纯碱和萤石(CaF2)为主要原料

方案二:以碳酸氢铵和六氟合硅酸为主要原料

(1)方案一中B可作为建筑材料,化合物A 是
(2)方案二中反应1产生的气体是
(3)方案二中反应2化学方程式
(4)工业电解制铝的阴极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】生活污水中的氮和磷主要以铵盐和磷酸盐形式存在,可用电解法从溶液中去除。电解装置如图:

以铁作阴极、石墨作阳极,可进行除氮;翻转电源正负极,以铁作阳极、石墨作阴极,可进行除磷。
I.电解除氮
(1)在碱性溶液中,NH3能直接在电极放电,转化为N2,相应的电极反应式为:_______ 。
(2)有Cl-存在时,除氮原理如图所示

主要依靠有效氯(HClO、ClO-)将NH4+ 或NH3氧化为N2。在不同pH条件下进行电解时,氮的去除率和水中有效氯浓度如图:
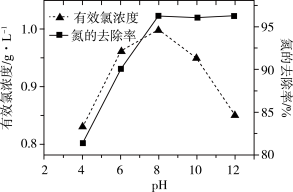
①当pH<8时,主要发生HClO氧化NH4+ 的反应,其离子方程式为:____________ 。
②结合平衡移动原理解释,当pH<8时,氮的去除率随pH的降低而下降的原因是:_____ 。
II.电解除磷
(3)除磷的原理是利用Fe2+ 将PO43- 转化为Fe3(PO4)2沉淀。
如图为某含Cl- 污水在氮磷联合脱除过程中溶液pH的变化。推测在20-40 min时脱除的元素是________ 。

(4)测定污水磷含量的方法如下:取100mL污水,调节至合适pH后用AgNO3溶液使磷全部转化为Ag3PO4沉淀。将沉淀过滤并洗涤后,用硝酸溶解,再使用NH4SCN溶液滴定产生的Ag+,发生反应Ag++SCN-=AgSCN↓,共消耗c mol/LNH4SCN溶液V mL。则此污水中磷的含量为_________ mg/L(以磷元素计)。

以铁作阴极、石墨作阳极,可进行除氮;翻转电源正负极,以铁作阳极、石墨作阴极,可进行除磷。
I.电解除氮
(1)在碱性溶液中,NH3能直接在电极放电,转化为N2,相应的电极反应式为:
(2)有Cl-存在时,除氮原理如图所示

主要依靠有效氯(HClO、ClO-)将NH4+ 或NH3氧化为N2。在不同pH条件下进行电解时,氮的去除率和水中有效氯浓度如图:

①当pH<8时,主要发生HClO氧化NH4+ 的反应,其离子方程式为:
②结合平衡移动原理解释,当pH<8时,氮的去除率随pH的降低而下降的原因是:
II.电解除磷
(3)除磷的原理是利用Fe2+ 将PO43- 转化为Fe3(PO4)2沉淀。
如图为某含Cl- 污水在氮磷联合脱除过程中溶液pH的变化。推测在20-40 min时脱除的元素是

(4)测定污水磷含量的方法如下:取100mL污水,调节至合适pH后用AgNO3溶液使磷全部转化为Ag3PO4沉淀。将沉淀过滤并洗涤后,用硝酸溶解,再使用NH4SCN溶液滴定产生的Ag+,发生反应Ag++SCN-=AgSCN↓,共消耗c mol/LNH4SCN溶液V mL。则此污水中磷的含量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】下表列出了周期表短周期中7种元素的有关数据:
根据上表信息,回答下列问题:
(1)元素①、②、⑦的最高价氧化物的水化物酸性从大到小的顺序是___________ (填化学式),元素⑤、⑥、⑦的简单离子半径从大到小的顺序是___________ (填离子符号)。
(2)元素③、⑥中氢化物稳定性更强的是___________ (填化学式),③的最高价氧化物的水化物的浓溶液与①的单质反应的化学方程式为___________ 。
(3)7种元素中金属性最强的单质在氧气中完全燃烧所得产物的电子式___________ ,该物质含有的化学键为:___________ 。
(4)下列关于元素周期表的叙述,正确的是___________(填标号)。
| 元素编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径(nm) | 0.077 | 0.110 | 0.102 | 0.152 | 0.186 | 0.071 | 0.099 |
| 最高价态 | +4 | +5 | +6 | +1 | +1 | 0 | +7 |
| 最低价态 | -4 | -3 | -2 | 0 | 0 | -1 | -1 |
(1)元素①、②、⑦的最高价氧化物的水化物酸性从大到小的顺序是
(2)元素③、⑥中氢化物稳定性更强的是
(3)7种元素中金属性最强的单质在氧气中完全燃烧所得产物的电子式
(4)下列关于元素周期表的叙述,正确的是___________(填标号)。
| A.元素周期表共有7个横行,称为周期;共有16个纵行,称为族 |
| B.前20号元素称为短周期元素 |
| C.副族元素中,没有非金属元素 |
| D.ⅠA族的元素都被称作碱金属元素 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知A、B、C为同一短周期的三种元素,它们的原子序数依次增大且和为41;A是该周期中(除稀有气体元素外)原子半径最大的元素,B元素的原子核外M层上的电子数比K层上的电子数多1。
回答下列问题:
(1)A原子的结构示意图为_________ ;
(2)C元素位于周期表的第_____ 周期、第____ 族;
(3)A和C形成的化合物的电子式为_________ ;
(4)写出B的最高价氧化物与A的最高价氧化物对应水化物的溶液之间反应的离子方程式_______________________________________ 。
回答下列问题:
(1)A原子的结构示意图为
(2)C元素位于周期表的第
(3)A和C形成的化合物的电子式为
(4)写出B的最高价氧化物与A的最高价氧化物对应水化物的溶液之间反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下列各物质是中学化学中常见的物质,甲为常见金属单质,乙、丙、丁是非金属单质,其它为化合物,B、D分别为黑色粉末和黑色晶体,G为淡黄色固体,J为生活中常见的调味品,I为红褐色固体,①是实验室制取丁的反应之一,F为棕黄色溶液。各物质间的转化如下图所示,回答下列各问题(部分生成物未列出):
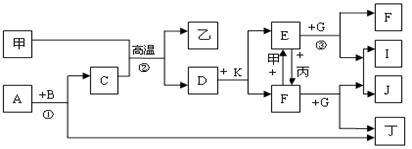
(1)写出乙的化学式_______ 、A的电子式_________ 、甲在周期表中位置是__________ ;
(2)写出G的一种用途____________________ ;
(3)写出B与K的浓溶液反应的化学方程式:_______________________________ ;
(4)整个转换过程中属于氧化还原反应的数目有__________ 个;
(5)写出反应③E与A按物质的量之比2:1的反应的离子方程式___ 。

(1)写出乙的化学式
(2)写出G的一种用途
(3)写出B与K的浓溶液反应的化学方程式:
(4)整个转换过程中属于氧化还原反应的数目有
(5)写出反应③E与A按物质的量之比2:1的反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】氨基甲酸铵(NH2COONH4)是一种易分解、易与水反应的白色固体、难溶于CCl4。实验室可将干燥二氧化碳和氨气通入CCl4中进行制备,反应原理为2NH3(g)+CO2(g)=NH2COONH4(s) ,反应放热,回答下列问题: _______ ,装置己中盛放的试剂为_______ ,庚中饱和碳酸氢钠溶液的作用_______ 。
(2)简述检验装置乙气密性的操作_______ 。
(3)氨气的发生装置可以选择上图中的_______ ,制取氨气的化学方程式为_______ 。
(4)预制备产品,选择上图中必要的装置,其连接顺序为_______ :
发生装置→_______→FG←_______←KJ←_______(按气流方向,用大写字母表示)。
(5)反应结束后,从反应后的混合物中分离出产品的实验操作是_______ 。
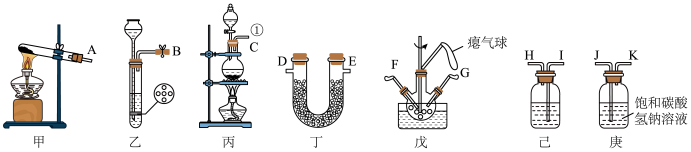
(2)简述检验装置乙气密性的操作
(3)氨气的发生装置可以选择上图中的
(4)预制备产品,选择上图中必要的装置,其连接顺序为
发生装置→_______→FG←_______←KJ←_______(按气流方向,用大写字母表示)。
(5)反应结束后,从反应后的混合物中分离出产品的实验操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】Fe/Fe3O4磁性材料在很多领域具有应用前景,其制备过程如下(各步均在N2氛围中进行):
①称取9.95gFeCl2•4H2O(Mr=199),配成50mL溶液,转移至恒压滴液漏斗中。
②向三颈烧瓶中加入100mL14mol•L-1KOH溶液。
③持续磁力搅拌,将FeCl2溶液以2mL•min-1的速度全部滴入三颈烧瓶中,100℃下回流3h。
④冷却后过滤,依次用热水和乙醇洗涤所得黑色沉淀,在40℃干燥。
⑤管式炉内焙烧2h,得产品3.24g。
部分装置如图:

回答下列问题:
(1)仪器a的名称是_______ ;使用恒压滴液漏斗的原因是_______ 。
(2)实验室制取N2有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和装置,选出一种可行的方法,化学方程式为_______ ,对应的装置为_______ (填字母)。
可供选择的试剂:CuO(s)、NH3(g)、Cl2(g)、O2(g)、饱和NaNO2(aq)、饱和NH4Cl(aq)
可供选择的发生装置(净化装置略去):
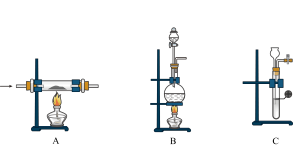
(3)三颈烧瓶中反应生成了Fe和Fe3O4,离子方程式为_______ 。
(4)步骤④中判断沉淀是否已经用水洗涤干净,应选择的试剂为_______ ;使用乙醇洗涤的目的是_______ 。
(5)该实验所得磁性材料的产率为________ (保留3位有效数字)。
①称取9.95gFeCl2•4H2O(Mr=199),配成50mL溶液,转移至恒压滴液漏斗中。
②向三颈烧瓶中加入100mL14mol•L-1KOH溶液。
③持续磁力搅拌,将FeCl2溶液以2mL•min-1的速度全部滴入三颈烧瓶中,100℃下回流3h。
④冷却后过滤,依次用热水和乙醇洗涤所得黑色沉淀,在40℃干燥。
⑤管式炉内焙烧2h,得产品3.24g。
部分装置如图:

回答下列问题:
(1)仪器a的名称是
(2)实验室制取N2有多种方法,请根据元素化合物知识和氧化还原反应相关理论,结合下列供选试剂和装置,选出一种可行的方法,化学方程式为
可供选择的试剂:CuO(s)、NH3(g)、Cl2(g)、O2(g)、饱和NaNO2(aq)、饱和NH4Cl(aq)
可供选择的发生装置(净化装置略去):

(3)三颈烧瓶中反应生成了Fe和Fe3O4,离子方程式为
(4)步骤④中判断沉淀是否已经用水洗涤干净,应选择的试剂为
(5)该实验所得磁性材料的产率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】常温常压酸浸全湿法从氧化镍矿中提取镍的工艺有安全性好、能耗低、浸出时短、生产成本低等优点,以某氧化镍矿石(NiO,含有的杂质为SiO2、以及Fe、Zn、Mg、Ca等元素的氢氧化物、氧化物或硅酸盐)为原料,生产流程如下:
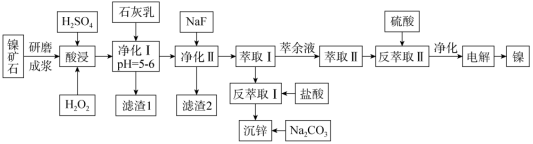
已知:(1)相关金属离子[Co(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
(3)锌的萃取过程反应为:
萃取:2RNa+Zn2+=R2Zn+2Na+
反萃取:R2Zn+2H+=2RH+Zn2+
回答以下问题:
(1)矿石需要先经过研磨成浆,其原因是___________ 。
(2)依据下列图象1、2,选择合适的实验条件,硫酸浓度为___________ ,浸出矿浆液固比___________ 。


(3)滤渣1的主要成分为___________ ;加入NaF的作用是___________ 。
(4)沉锌的过程会生成碱式盐,写出沉锌的离子方程式:___________ 。
(5)电解硫酸镍溶液制备单质镍的化学反应方程式为___________ ;沉积镍后的电解液可返回___________ (填操作单元的名称)继续使用。

已知:(1)相关金属离子[Co(Mn+)=0.1 mol·L-1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Fe3+ | Fe2+ | Zn2+ | Mg2+ | Ni2+ |
| 开始沉淀的pH | 1.5 | 6.3 | 6.2 | 10.4 | 7.7 |
| 沉淀完全的pH | 2.8 | 8.3 | 8.2 | 12.4 | 9.5 |
(3)锌的萃取过程反应为:
萃取:2RNa+Zn2+=R2Zn+2Na+
反萃取:R2Zn+2H+=2RH+Zn2+
回答以下问题:
(1)矿石需要先经过研磨成浆,其原因是
(2)依据下列图象1、2,选择合适的实验条件,硫酸浓度为


(3)滤渣1的主要成分为
(4)沉锌的过程会生成碱式盐,写出沉锌的离子方程式:
(5)电解硫酸镍溶液制备单质镍的化学反应方程式为
您最近一年使用:0次



