解题方法
1 . 下列实验操作能达到目的的是
选项 | 操作 | 目的 |
A | 向待测液中滴加盐酸酸化的BaCl2溶液 | 检验待测液合 |
B | 向含Fe3+的NiSO4溶液中加入过量NiO,过滤 | 提纯NiSO4溶液 |
C | 将含乙醇蒸气的乙烯通过酸性KMnO4溶液 | 除去乙烯中乙醇蒸气 |
D | 分别向对甲基苯酚和苯酚中滴加FeCl3溶液 | 区别对甲基苯酚和苯酚 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 根据下列操作及现象能得出相应结论的是
选项 | 操作及现象 | 结论 |
A | 在足量稀硫酸中加入Cu2O粉末,得到蓝色溶液和红色固体 |  只表现氧化性 只表现氧化性 |
B | 向苯酚溶液中滴加溴水产生白色沉淀且pH降低 | 苯酚与溴单质发生加成反应 |
C | 在石灰石表面滴加盐酸,将生成的气体通入硅酸钠溶液,产生白色胶状沉淀 | 非金属性: |
D | 在酸性高锰酸钾溶液中滴加甲苯,溶液褪色 | 苯环活化了甲基 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 下列各组指定粒子数目相等的是
A. 和 和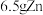 分别与足量稀硝酸反应转移电子数 分别与足量稀硝酸反应转移电子数 |
B. 乙二醇含 乙二醇含 杂化的原子数和常温常压下 杂化的原子数和常温常压下 氖气含原子数 氖气含原子数 |
C.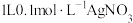 溶液制得 溶液制得 胶粒数与 胶粒数与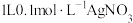 溶液中 溶液中 数 数 |
D. 和 和 的混合气体含分子数和标准状况下 的混合气体含分子数和标准状况下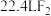 含原子数 含原子数 |
您最近一年使用:0次
4 . 下列离子方程式正确且符合题意的是
A.向 浊液中滴加 浊液中滴加 溶液产生蓝色沉淀: 溶液产生蓝色沉淀: |
B.向 溶液中滴加 溶液中滴加 溶液产生气泡: 溶液产生气泡: |
C.向变质的 溶液中滴加 溶液中滴加 溶液,溶液变红色: 溶液,溶液变红色: |
D.向 白色浊液中滴加氡水,溶液变澄清: 白色浊液中滴加氡水,溶液变澄清: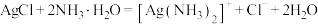 |
您最近一年使用:0次
5 . 化学与生产、生活息息相关。下列叙述错误的是
| A.服用小苏打水溶液可以减缓人体胃酸过多症状 |
| B.为了人体健康,禁止使用食品抗氧化剂和增色剂 |
| C.鼓励使用聚乳酸和聚碳酸酯等可自然降解材料 |
| D.及时改造高能耗和高污染企业并对“三废”先处理后排放 |
您最近一年使用:0次
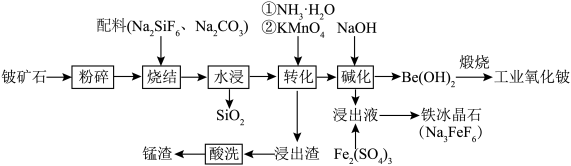
6 . 铍作为一种稀有元素,在航空航天、电子加工等领域具有重要意义。用铍矿石(含BeO及少量Ca、Mg、Mn元素)与配料生产工业氧化铍的工艺流程如下: 的还原产物为
的还原产物为 。回答下列问题:
。回答下列问题:
(1)若缺少粉碎步骤,产生的影响为_______ 。
(2)烧结时,若铍矿石中BeO恰好转化为 ,Si元素转化为
,Si元素转化为 ,则BeO发生反应的化学方程式为
,则BeO发生反应的化学方程式为_______ 。
(3)水浸后溶液中仍有未反应的 ,加入
,加入 后会转化为
后会转化为 沉淀,所得产物可除去溶液中的钙、镁元素,
沉淀,所得产物可除去溶液中的钙、镁元素, 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(4)水浸后溶液中Mn元素以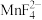 形式存在,加入稍过量
形式存在,加入稍过量 溶液煮沸50min至溶液
溶液煮沸50min至溶液______ 时说明反应结束。结合平衡移动原理解释酸洗时控制溶液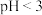 的原因:
的原因:______ 。
(5)碱化时,室温下加入NaOH,控制 ,析出颗粒状的
,析出颗粒状的 ,所得浸出液中
,所得浸出液中 ,此时溶液中
,此时溶液中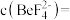
___  。已知
。已知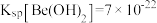 ,
,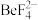 的解离常数
的解离常数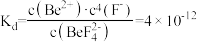
(6)碱化后浸出液中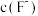 远高于排放标准,向其中加入硫酸铁生成
远高于排放标准,向其中加入硫酸铁生成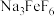 ,
, 为八面体结构,则Fe原子采取的杂化方式为
为八面体结构,则Fe原子采取的杂化方式为____ (填标号)。
A. B.
B. C.
C.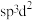
 的还原产物为
的还原产物为 。回答下列问题:
。回答下列问题:(1)若缺少粉碎步骤,产生的影响为
(2)烧结时,若铍矿石中BeO恰好转化为
 ,Si元素转化为
,Si元素转化为 ,则BeO发生反应的化学方程式为
,则BeO发生反应的化学方程式为(3)水浸后溶液中仍有未反应的
 ,加入
,加入 后会转化为
后会转化为 沉淀,所得产物可除去溶液中的钙、镁元素,
沉淀,所得产物可除去溶液中的钙、镁元素, 发生反应的离子方程式为
发生反应的离子方程式为(4)水浸后溶液中Mn元素以
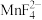 形式存在,加入稍过量
形式存在,加入稍过量 溶液煮沸50min至溶液
溶液煮沸50min至溶液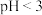 的原因:
的原因:(5)碱化时,室温下加入NaOH,控制
 ,析出颗粒状的
,析出颗粒状的 ,所得浸出液中
,所得浸出液中 ,此时溶液中
,此时溶液中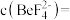
 。已知
。已知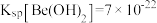 ,
,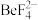 的解离常数
的解离常数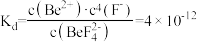
(6)碱化后浸出液中
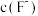 远高于排放标准,向其中加入硫酸铁生成
远高于排放标准,向其中加入硫酸铁生成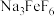 ,
, 为八面体结构,则Fe原子采取的杂化方式为
为八面体结构,则Fe原子采取的杂化方式为A.
 B.
B. C.
C.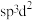
您最近一年使用:0次
7 . 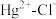 体系中存在平衡:
体系中存在平衡: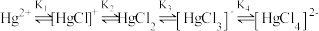 。常温下,用一定浓度的
。常温下,用一定浓度的 溶液滴定NaCl溶液的过程中,溶液中含Hg微粒的分布分数
溶液滴定NaCl溶液的过程中,溶液中含Hg微粒的分布分数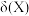 随
随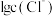 的变化曲线如图所示。已知:
的变化曲线如图所示。已知: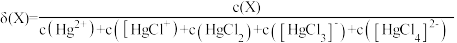 。下列说法错误的是
。下列说法错误的是
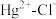 体系中存在平衡:
体系中存在平衡: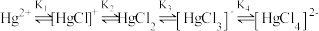 。常温下,用一定浓度的
。常温下,用一定浓度的 溶液滴定NaCl溶液的过程中,溶液中含Hg微粒的分布分数
溶液滴定NaCl溶液的过程中,溶液中含Hg微粒的分布分数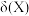 随
随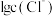 的变化曲线如图所示。已知:
的变化曲线如图所示。已知: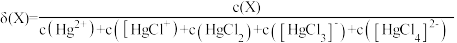 。下列说法错误的是
。下列说法错误的是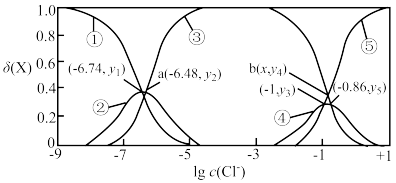
A.曲线③表示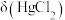 随 随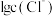 的变化关系 的变化关系 |
B. |
| C.增大氯化钠溶液的浓度,a点向右移动 |
D.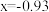 |
您最近一年使用:0次
解题方法
8 . 下列反应的离子方程式正确的是
A.向硫化钠溶液中通入足量二氧化硫: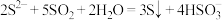 |
B.向 溶液中加入足量烧碱溶液: 溶液中加入足量烧碱溶液: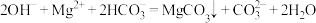 |
C.向次氯酸钙溶液中通入过量二氧化碳: |
D.向 溶液中通入少量 溶液中通入少量 : :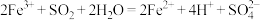 |
您最近一年使用:0次
昨日更新
|
191次组卷
|
2卷引用:湖南省2024届普通高中高三下学期学业水平选择性考试临考预测押题密卷化学试题(B卷)
9 . 由下列实验步骤得到的实验现象、结论或解释均正确的是
| 选项 | 实验步骤 | 实验现象 | 结论或解释 |
| A | 向 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | 溶液紫色褪去 |  具有还原性 具有还原性 |
| B | 用玻璃棒蘸取NaClO溶液点在pH试纸上 | 试纸变白 | NaClO溶液呈中性 |
| C | 向 溶液中同时通入 溶液中同时通入 和 和 | 出现白色沉淀 | 白色沉淀为 |
| D | 向2mL 溶液中先滴加4滴 溶液中先滴加4滴 KCl溶液,再滴加4滴 KCl溶液,再滴加4滴 KI溶液 KI溶液 | 先产生白色沉淀,再产生黄色沉淀 | 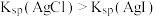 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
10 . 为实现“碳中和”“碳达峰”,碳的循环利用是重要措施。利用氢气和CO反应生成甲烷,涉及的反应如下:
i.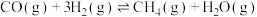

ii.

iii.

回答下列问题:
(1)在25℃和101kPa下, 转变为
转变为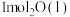 时放出44.0kJ热量,
时放出44.0kJ热量, 的燃烧热为
的燃烧热为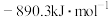 ,CO的燃烧热为
,CO的燃烧热为 ,
, 的燃烧热为
的燃烧热为 ,则
,则
________  。
。
(2)一定温度下,在恒容的密闭容器中进行上述反应,平衡时CO的转化率及 的选择性随
的选择性随 变化的情况如图所示[已知
变化的情况如图所示[已知 的选择性
的选择性 ]。
]。 选择性变化的曲线是
选择性变化的曲线是________ (填“甲”或“乙”),保持 不变,曲线甲由B点达到A点需要的条件为
不变,曲线甲由B点达到A点需要的条件为________ 。
②相同温度下,向恒容容器内加入 和1molCO,初始压强为10MPa,平衡时
和1molCO,初始压强为10MPa,平衡时 的物质的量为
的物质的量为________ mol,反应ii的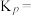
________ (保留小数点后一位)。
(3) 催化加氢制甲醇也是碳循环的重要途径。
催化加氢制甲醇也是碳循环的重要途径。 在某催化剂表面与氢气作用制备甲醇的反应机理如图所示。催化循环中产生的中间体微粒共
在某催化剂表面与氢气作用制备甲醇的反应机理如图所示。催化循环中产生的中间体微粒共________ 种, 催化加氢制甲醇总反应的化学方程式为
催化加氢制甲醇总反应的化学方程式为________ 。
i.
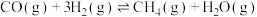

ii.


iii.


回答下列问题:
(1)在25℃和101kPa下,
 转变为
转变为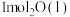 时放出44.0kJ热量,
时放出44.0kJ热量, 的燃烧热为
的燃烧热为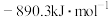 ,CO的燃烧热为
,CO的燃烧热为 ,
, 的燃烧热为
的燃烧热为 ,则
,则
 。
。(2)一定温度下,在恒容的密闭容器中进行上述反应,平衡时CO的转化率及
 的选择性随
的选择性随 变化的情况如图所示[已知
变化的情况如图所示[已知 的选择性
的选择性 ]。
]。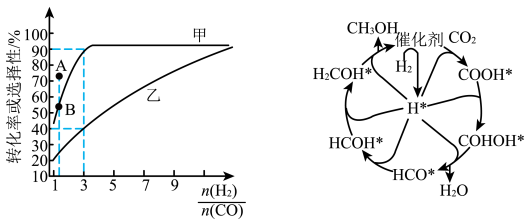
 选择性变化的曲线是
选择性变化的曲线是 不变,曲线甲由B点达到A点需要的条件为
不变,曲线甲由B点达到A点需要的条件为②相同温度下,向恒容容器内加入
 和1molCO,初始压强为10MPa,平衡时
和1molCO,初始压强为10MPa,平衡时 的物质的量为
的物质的量为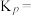
(3)
 催化加氢制甲醇也是碳循环的重要途径。
催化加氢制甲醇也是碳循环的重要途径。 在某催化剂表面与氢气作用制备甲醇的反应机理如图所示。催化循环中产生的中间体微粒共
在某催化剂表面与氢气作用制备甲醇的反应机理如图所示。催化循环中产生的中间体微粒共 催化加氢制甲醇总反应的化学方程式为
催化加氢制甲醇总反应的化学方程式为
您最近一年使用:0次
昨日更新
|
178次组卷
|
5卷引用: 湖南省北师联盟2024届高三下学期模拟考试三模化学试题




