解题方法
1 . 已知实验室常用二氧化锰粉末和浓盐酸制取氯气,其反应的化学方程式为: ,某实验小组用下图所示装置制取纯净干燥的氯气。
,某实验小组用下图所示装置制取纯净干燥的氯气。
(1)盛放浓盐酸的仪器的名称为___________
(2)B是除杂装置,盛放的试剂是___________ (填“饱和食盐水”或“饱和NaHCO3溶液”);
(3)C装置利用了浓硫酸的___________ (填“吸水性”“脱水性”或“强氧化性”);
(4)该制取过程中,收集氯气的方法是___________ (填“A”或“B”);
A.向下排空气法 B.向上排空气法
(5)为防止Cl2污染环境,E烧杯中盛装冷的NaOH溶液,请完善该反应的离子方程式:Cl2+2OH-=Cl-+___________ +H2O,在常温下,人们利用该反应制得漂白液,漂白液的有效成分为___________ (填“NaCl”或“NaClO”),该反应___________ (填“是 ”或“不是”)氧化还原反应。
(6)欲制取2.24L标准状况下的Cl2,至少需要MnO2的质量为___________ g。
 ,某实验小组用下图所示装置制取纯净干燥的氯气。
,某实验小组用下图所示装置制取纯净干燥的氯气。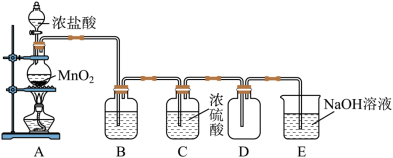
(1)盛放浓盐酸的仪器的名称为
(2)B是除杂装置,盛放的试剂是
(3)C装置利用了浓硫酸的
(4)该制取过程中,收集氯气的方法是
A.向下排空气法 B.向上排空气法
(5)为防止Cl2污染环境,E烧杯中盛装冷的NaOH溶液,请完善该反应的离子方程式:Cl2+2OH-=Cl-+
(6)欲制取2.24L标准状况下的Cl2,至少需要MnO2的质量为
您最近一年使用:0次
2 . 下表是元素周期表的一部分,针对表中的①~⑨种元素,回答下列问题:
(1)元素⑧在周期表中的位置是___________ 。
(2)表中的①~⑨种元素,其最高价氧化物对应的水化物酸性最强的含氧酸
是___________ (填化学式),上述主族元素中原子半径最大的是___________ (填化学式)。
(3)元素④与⑧的简单氢化物稳定性强的是___________ (填化学式)。
(4)钾元素与⑨形成的化合物的电子式为___________ ,该化合物是由___________ (填“离子”、“共价”)键形成的。
(5)⑤⑥⑦的金属性强弱为:___________ (用元素符号表示),⑦和⑧最高价氧化物的水化物相互反应的离子方程式为______________________
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | Ar |
(2)表中的①~⑨种元素,其最高价氧化物对应的水化物酸性最强的含氧酸
是
(3)元素④与⑧的简单氢化物稳定性强的是
(4)钾元素与⑨形成的化合物的电子式为
(5)⑤⑥⑦的金属性强弱为:
您最近一年使用:0次
3 . 铁与空气接触时会形成氧化物,如一块低碳钢可以被三种氧化物膜所覆盖与金属接触的一侧是FeO,与空气接触的一侧是 ,而中间则是
,而中间则是 。
。
(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的___________ (填化学式)。
(2) 的一种用途是
的一种用途是___________ 。(填“用作油漆、涂料 ”或“磁电机”);
(3)FeO可作化妆品中的色素,它还能进行一系列转化: 。
。
① 时应加入的试剂是
时应加入的试剂是___________ (填“H2SO4”或“Na2SO4”)。
②“速力菲”(主要有效成分是 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入___________ (填“KSCN”或“K2SO4”),若出现___________ (填“红色”或“浅绿色”)现象,则证明该药物已变质。
③在 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成___________ (填“红褐色”或“黄色”),其中沉淀颜色发生变化的化学方程式为___________ 。
 ,而中间则是
,而中间则是 。
。(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的
(2)
 的一种用途是
的一种用途是(3)FeO可作化妆品中的色素,它还能进行一系列转化:
 。
。①
 时应加入的试剂是
时应加入的试剂是②“速力菲”(主要有效成分是
 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入③在
 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
您最近一年使用:0次
解题方法
4 . 回答下列问题
(1)葡萄酒酿制过程中,葡萄汁中某些细菌的繁殖会影响发酵,添加适量的___________ (填“CO2”或“SO2”)可以起到杀菌作用。
(2)SO2可由浓硫酸与木炭在加热条件下可反应生成,为检验反应的其他产物以及验证其性质,某同学设计了如下图所示的实验。请据此回答下列问题:___________ ↑+2H2O,在该反应中,体现了C的___________ (填“还原性”或“氧化性”,下同),浓硫酸的___________ 。
②B装置中的实验现象是___________ ,证明产物中有SO2生成,体现了SO2的___________ (填“漂白性”或“氧化性”)
③若装置C中酸性高锰酸钾溶液仍为红色,则D装置中澄清石灰水的作用是证明产物中有___________ (填“SO2”或“CO2”)生成。
(1)葡萄酒酿制过程中,葡萄汁中某些细菌的繁殖会影响发酵,添加适量的
(2)SO2可由浓硫酸与木炭在加热条件下可反应生成,为检验反应的其他产物以及验证其性质,某同学设计了如下图所示的实验。请据此回答下列问题:
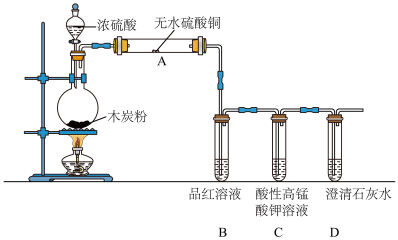
②B装置中的实验现象是
③若装置C中酸性高锰酸钾溶液仍为红色,则D装置中澄清石灰水的作用是证明产物中有
您最近一年使用:0次
5 . 下列化学用语表示正确的是
| A.NaCl的电子式:Na+Cl- |
B.HCl的电子式: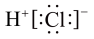 |
C. 的结构示意图: 的结构示意图: |
D.硫酸钾的电离方程式: |
您最近一年使用:0次
6 . 下列有关氯气的性质,说法正确的是
| A.氯气有毒 |
| B.纯净的H2不能在Cl2中燃烧 |
| C.将Cl2与Fe反应生成FeCl2 |
| D.Cl2能使湿润的有色纸条褪色,说明Cl2具有漂白性 |
您最近一年使用:0次
7 . 根据金属钠与水(滴有酚酞)反应的现象,下列有关说法错误的是
| A.钠熔化成闪亮的小球,说明钠的熔点低且反应放热 |
| B.反应后溶液的颜色逐渐变红,说明反应生成了碱 |
| C.该反应中每1mol的Na得到1mol的电子 |
| D.当火灾现场存放有大量金属钠时不能用水来灭火 |
您最近一年使用:0次
8 . 下列关于元素周期表中关于氯元素的信息如图所示,说法正确是
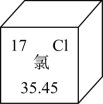
| A.氯元素的原子序数为17 | B.氯原子核内中子数为17 |
| C.氯元素不能形成离子化合物 | D.氯元素不属于非金属元素 |
您最近一年使用:0次
解题方法
9 . 下列反应中,属于氧化还原反应的是
A.2Fe(OH)3 Fe2O3+3H2O Fe2O3+3H2O | B.CaO+SO3=CaSO4 |
| C.NaOH+HCl=NaCl+H2O | D.Zn+H2SO4=ZnSO4+H2↑ |
您最近一年使用:0次
10 . 钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在_______ 中。
(2)除去碳酸钠固体中碳酸氢钠的方法是______________ 。
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入_______ (填“铁粉”或“铜粉”)。
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:_______________ 。
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于__________ (填“碱性”或“两性”)氧化物。
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在
(2)除去碳酸钠固体中碳酸氢钠的方法是
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于
您最近一年使用:0次



