名校
解题方法
1 . 化合价和物质类别是整理元素及化合物知识的两个要素,可表示为“价—类”二维图。铁元素的“价—类”二维图如图所示,下列说法正确的是
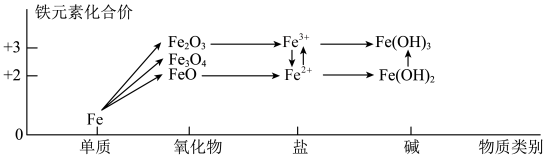
| A.高温条件下Fe和水蒸气反应生成Fe(OH)2和H2,该反应为置换反应 |
| B.FeO在加热的条件下能被氧气氧化成Fe3O4 |
| C.将饱和的FeCl3溶液加热煮沸可制得氢氧化铁胶体 |
| D.Fe(OH)2浊液露置于空气中,由白色立即变为红褐色 |
您最近一年使用:0次
2024-04-26更新
|
145次组卷
|
2卷引用:湖南省常德石门一中2023-2024年上学期高一年级化学期末考试卷(适用湖南地区))
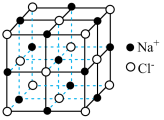
2 . 几种晶体的晶胞(或晶体结构)如图所示,下列说法正确的是
|
|
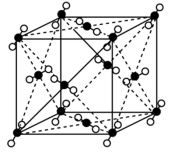
NaCl晶胞 | CO2晶胞 |
|
|
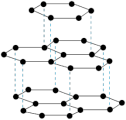
金刚石晶胞 | 石墨晶体结构 |
| A.NaCl中Na+的配位数小于干冰中CO2分子的配位数 |
| B.氯化钠晶体中,每个Na+周围距离最近且相等的Na+有6个 |
C.若金刚石的晶胞边长为a,其中两个最近的碳原子之间的距离为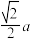 |
| D.石墨晶体层内是共价键,层间是范德华力,所以石墨是一种过渡晶体 |
您最近一年使用:0次
2024-04-26更新
|
181次组卷
|
2卷引用:湖南省常德市汉寿县第一中学2023-2024学年高二下学期6月期末考试化学试题
名校
解题方法
3 . I.氧化还原反应原理在研究物质性质及物质转化方面具有重要的价值。
(1)生活中常用的“84”消毒液与洁厕净(主要成分是盐酸)混合时会产生大量的有毒气体,写出该反应的离子方程式___________ 。
(2)火药是中国的四大发明之一,永远值得中华儿女骄傲。黑火药在发生爆炸时,发生如下反应2KNO3+3C+S=K2S+N2↑+3CO2↑,则生成1molN2反应过程中转移电子的数目为___________ 。
(3)中国古代著作中有“银针验毒”的记录,其原理为4Ag+2H2S+O2=2X+2H2O,则X的化学式是___________ ,其中 H2S在该反应中___________ (填序号)。
A.作氧化剂 B.作还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(4)砒霜(As2O3)与Zn可以发生如下反应As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O,其中氢元素的化合价未发生改变。在上述反应中As2O3,显示出来的性质是___________ (填“还原性”或“氧化性”)。
II.元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:___________ 。
(6)在①~⑨元素中,原子半径最大的元素,其某种氧化物可用于呼吸面具中氧气来源,请写出该物质与二氧化碳反应化学方程式___________ 。
(7)写出⑤、⑦两种元素所形成的最高价氧化物对应的水化物反应的离子方程式是___________ 。
(8)比较④与⑨的简单气态氢化物的稳定性___________ >___________ (填化学式)。
(9)由下列元素形成的化合物中含有离子键的是___________。
(10)写出⑤在空气中燃烧产物的电子式:___________ 。
(1)生活中常用的“84”消毒液与洁厕净(主要成分是盐酸)混合时会产生大量的有毒气体,写出该反应的离子方程式
(2)火药是中国的四大发明之一,永远值得中华儿女骄傲。黑火药在发生爆炸时,发生如下反应2KNO3+3C+S=K2S+N2↑+3CO2↑,则生成1molN2反应过程中转移电子的数目为
(3)中国古代著作中有“银针验毒”的记录,其原理为4Ag+2H2S+O2=2X+2H2O,则X的化学式是
A.作氧化剂 B.作还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(4)砒霜(As2O3)与Zn可以发生如下反应As2O3+6Zn+6H2SO4=2AsH3+6ZnSO4+3H2O,其中氢元素的化合价未发生改变。在上述反应中As2O3,显示出来的性质是
II.元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:

(6)在①~⑨元素中,原子半径最大的元素,其某种氧化物可用于呼吸面具中氧气来源,请写出该物质与二氧化碳反应化学方程式
(7)写出⑤、⑦两种元素所形成的最高价氧化物对应的水化物反应的离子方程式是
(8)比较④与⑨的简单气态氢化物的稳定性
(9)由下列元素形成的化合物中含有离子键的是___________。
| A.①③ | B.②③ | C.①④ | D.⑥⑨ |
您最近一年使用:0次
名校
4 . 元素铊的相关信息如图所示。下列有关卡片信息解读不正确的是

| A.铊的元素符号为Tl | B.205Tl的中子数比质子数多43 |
| C.铊的相对原子质量为204.4g | D.铊原子的质子数为81 |
您最近一年使用:0次
名校
5 . 经检测,某化工厂排出的废水呈酸性,且其中含有大量 Na+、Cu2+、SO 、Cl-、NO
、Cl-、NO 。
。
(1)下列离子中,能大量存在于该废水中的是___________(填标号)
(2)某化学社团小组成员欲除去废水样品中的Cu2+和SO ,最终得到中性溶液,设计的方案流程如图:
,最终得到中性溶液,设计的方案流程如图:___________ (写化学式)。“溶液3”中的离子为Na+、Cl-和某种离子M,测得Na+、Cl-浓度分别为xmol/L、ymol/L,则M的物质的量浓度为___________ mol/L(用含x、y的代数式表示)。
②“分离操作”的名称是___________ ,需用到的玻璃仪器主要有___________ 。
③向“白色沉淀2”中加入足量盐酸,沉淀___________ 。(填“质量不变”、“部分溶解”、“全部溶解”)
(3)若某K2CO3溶液中含mmol K2CO3,向其中滴入一定量的稀盐酸,恰好使溶液中Cl-和HCO 的物质的量浓度之比为2∶1,则滴入的稀盐酸中的HCl的物质的量等于
的物质的量浓度之比为2∶1,则滴入的稀盐酸中的HCl的物质的量等于___________ mol(用含字母m的代数式表示)。
 、Cl-、NO
、Cl-、NO 。
。(1)下列离子中,能大量存在于该废水中的是___________(填标号)
| A.Ag+ | B.Mg2+ | C.OH- | D.HCO |
(2)某化学社团小组成员欲除去废水样品中的Cu2+和SO
 ,最终得到中性溶液,设计的方案流程如图:
,最终得到中性溶液,设计的方案流程如图: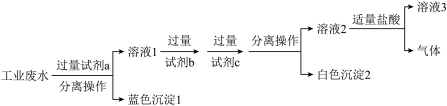
②“分离操作”的名称是
③向“白色沉淀2”中加入足量盐酸,沉淀
(3)若某K2CO3溶液中含mmol K2CO3,向其中滴入一定量的稀盐酸,恰好使溶液中Cl-和HCO
 的物质的量浓度之比为2∶1,则滴入的稀盐酸中的HCl的物质的量等于
的物质的量浓度之比为2∶1,则滴入的稀盐酸中的HCl的物质的量等于
您最近一年使用:0次
名校
解题方法
6 . 已知氯气与碱反应时,产物受温度的影响。实验室中利用如图装置(部分装置省略)制备KClO3和NaClO,并探究其氧化还原性质。
(1)仪器a的名称是:___________ 。
(2)装置D的离子方程式为___________ 。
(3)装置B中的试剂为___________ 。
(4)根据题目已知信息,氯气通入到一定温度的KOH溶液中,溶液中含Cl元素的离子且满足比例关系正确的有___________ (填标号)。
A.含有Cl-和ClO ;且c(Cl-):c(ClO
;且c(Cl-):c(ClO )=1:5
)=1:5
B.含有Cl-、ClO 和ClO-;且c(Cl-):c(ClO
和ClO-;且c(Cl-):c(ClO ):c(ClO-)=(5b+c):b:c
):c(ClO-)=(5b+c):b:c
C.含有ClO 和ClO- ;且c(ClO
和ClO- ;且c(ClO ):c(ClO-)=1:5
):c(ClO-)=1:5
(5)探究KClO3、NaClO的氧化能力 。
。
现象:1号试管溶液颜色不变,2号试管溶液变为棕色,1、2号试管均未检测到IO 。
。
结论:该条件下氧化能力KClO3___________ NaClO(填“大于”或“小于”)。
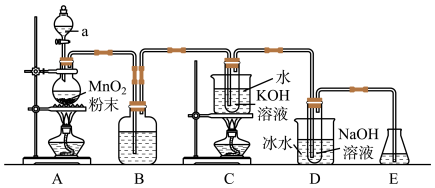
(1)仪器a的名称是:
(2)装置D的离子方程式为
(3)装置B中的试剂为
(4)根据题目已知信息,氯气通入到一定温度的KOH溶液中,溶液中含Cl元素的离子且满足比例关系正确的有
A.含有Cl-和ClO
 ;且c(Cl-):c(ClO
;且c(Cl-):c(ClO )=1:5
)=1:5 B.含有Cl-、ClO
 和ClO-;且c(Cl-):c(ClO
和ClO-;且c(Cl-):c(ClO ):c(ClO-)=(5b+c):b:c
):c(ClO-)=(5b+c):b:c C.含有ClO
 和ClO- ;且c(ClO
和ClO- ;且c(ClO ):c(ClO-)=1:5
):c(ClO-)=1:5(5)探究KClO3、NaClO的氧化能力
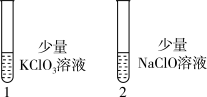
 。
。现象:1号试管溶液颜色不变,2号试管溶液变为棕色,1、2号试管均未检测到IO
 。
。结论:该条件下氧化能力KClO3
您最近一年使用:0次
名校
7 . 甲、乙、丙三种物质含有同种元素,它们之间存在如下转化关系: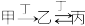 ,下列推断错误的是
,下列推断错误的是
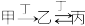 ,下列推断错误的是
,下列推断错误的是| A.若甲为炭,则丁可以是氧气 | B.若甲为铁,则丁可以是氯气 |
| C.若甲为氢氧化钠,则丁可以是二氧化硫 | D.若甲为氯化铝,则丁可以是氢氧化钠 |
您最近一年使用:0次
名校
8 . Cr2O 毒性较强,常用NaHSO3处理工业废水中的Cr2O
毒性较强,常用NaHSO3处理工业废水中的Cr2O ,反应的离子方程式为:H+ +Cr2O
,反应的离子方程式为:H+ +Cr2O +HSO
+HSO
 Cr3++SO
Cr3++SO +H2O(未配平),下列关于该反应的说法正确的是
+H2O(未配平),下列关于该反应的说法正确的是
 毒性较强,常用NaHSO3处理工业废水中的Cr2O
毒性较强,常用NaHSO3处理工业废水中的Cr2O ,反应的离子方程式为:H+ +Cr2O
,反应的离子方程式为:H+ +Cr2O +HSO
+HSO
 Cr3++SO
Cr3++SO +H2O(未配平),下列关于该反应的说法正确的是
+H2O(未配平),下列关于该反应的说法正确的是| A.氧化剂和还原剂的计量数之比为3:1 | B.Cr3+是氧化反应的产物 |
C. 发生还原反应 发生还原反应 | D.消耗5 molH+时转移6mol电子 |
您最近一年使用:0次
名校
解题方法
9 . 4种短周期主族元素X、Y、Z和Q的原子序数依次增大,相关信息如下表:
下列说法正确的是
| 元素 | 相关信息 |
| X | 最外层电子数等于次外层电子数 |
| Y | 与X在同一主族 |
| Z | 单质为淡黄色固体,难溶于水,微溶于酒精,易溶于二硫化碳 |
| Q | 同周期主族元素中原子半径最小 |
| A.X的金属性比Y强 |
| B.Y的原子半径是同周期中最大的 |
| C.Z的单质在空气燃烧和在充满氧气的集气瓶中燃烧产物相同 |
| D.Q的含氧酸与Z的含氧酸都可以混合,不发生反应 |
您最近一年使用:0次
名校
10 . 下列叙述错误的是
| A.1 mol SO2中含有2 mol氧原子和1 mol硫原子 |
| B.1 mol N2的质量为28g |
| C.0.1 mol H2O中含有的电子数目约为6.02×1023 |
| D.3.01×1023个CO2分子所占的体积约为11.2升 |
您最近一年使用:0次