1 . 硼元素在地壳中的含量仅为 ,但它却有着种类繁多的化合物。
,但它却有着种类繁多的化合物。
(1)基态 原子的电子排布式为
原子的电子排布式为___________ ;基态 原子的核外电子运动状态有
原子的核外电子运动状态有___________ 种。
(2)根据 的解离反应:
的解离反应: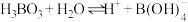 ,
,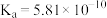 ,可判断
,可判断 是
是___________ 酸, 离子的VSEPR模型为
离子的VSEPR模型为___________ ,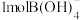 离子中含有
离子中含有___________  键。
键。
(3)分子式为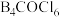 的化合物的结构如图,其中
的化合物的结构如图,其中 原子的杂化类型是
原子的杂化类型是___________ ,B-B-B键的键角___________ 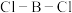 的键角(填“>”“<”或“=”)。
的键角(填“>”“<”或“=”)。

(4)在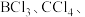 和
和 三种分子中,属于极性分子的是
三种分子中,属于极性分子的是___________ ,多原子分子中各原子若在同一平面,且有相互平行的 轨道,则
轨道,则 电子可在多个原子间运动,形成“离域
电子可在多个原子间运动,形成“离域 键”,上述三种分子中存在“离域
键”,上述三种分子中存在“离域 键”的是
键”的是___________ 。
 ,但它却有着种类繁多的化合物。
,但它却有着种类繁多的化合物。(1)基态
 原子的电子排布式为
原子的电子排布式为 原子的核外电子运动状态有
原子的核外电子运动状态有(2)根据
 的解离反应:
的解离反应: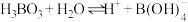 ,
,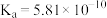 ,可判断
,可判断 是
是 离子的VSEPR模型为
离子的VSEPR模型为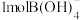 离子中含有
离子中含有 键。
键。(3)分子式为
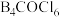 的化合物的结构如图,其中
的化合物的结构如图,其中 原子的杂化类型是
原子的杂化类型是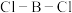 的键角(填“>”“<”或“=”)。
的键角(填“>”“<”或“=”)。
(4)在
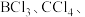 和
和 三种分子中,属于极性分子的是
三种分子中,属于极性分子的是 轨道,则
轨道,则 电子可在多个原子间运动,形成“离域
电子可在多个原子间运动,形成“离域 键”,上述三种分子中存在“离域
键”,上述三种分子中存在“离域 键”的是
键”的是
您最近一年使用:0次
名校
2 . 某温度下,由H2CO3与HCl或NaOH配制一组总含碳微粒浓度为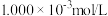 的混合溶液,混合体系中部分物种的浓度的负对数
的混合溶液,混合体系中部分物种的浓度的负对数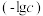 与pH关系如图所示。下列说法错误的是
与pH关系如图所示。下列说法错误的是

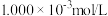 的混合溶液,混合体系中部分物种的浓度的负对数
的混合溶液,混合体系中部分物种的浓度的负对数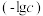 与pH关系如图所示。下列说法错误的是
与pH关系如图所示。下列说法错误的是
A.该溶液的温度为 |
B. 时,混合体系中浓度最高的含碳物种为 时,混合体系中浓度最高的含碳物种为 |
C.该条件下,H2CO3的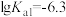 |
D. 的溶液中: 的溶液中: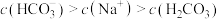 |
您最近一年使用:0次
2024-03-01更新
|
189次组卷
|
3卷引用:湖南省益阳市2023-2024学年高二上学期普通高中期末质量检测化学试题
解题方法
3 . 利用甲烷制取氢气等气体是科学家研究的热点课题。
(1)一定条件下, 分解反应
分解反应 的部分反应历程如下图所示。
的部分反应历程如下图所示。
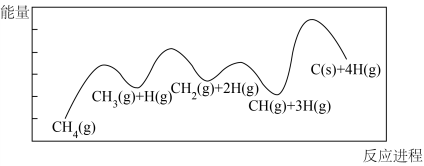
①该历程图表示___________ 步反应,其中正反应活化能最大步骤的反应方程式为___________ 。
② 分解反应
分解反应___________ 。
A.高温下能自发进行 B.低温下能自发进行
C.任何温度都能自发进行 D.任何温度都不能自发进行
(2)科学家提出以吸附性活性炭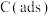 为催化剂,利用
为催化剂,利用 与
与 制备“合成气”(
制备“合成气”( 、
、 )。其反应历程分两步,反应历程的能量变化如下图:
)。其反应历程分两步,反应历程的能量变化如下图:
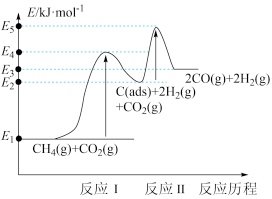
反应Ⅰ: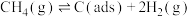 (慢反应)
(慢反应)
反应Ⅱ: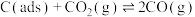 (快反应)
(快反应)
①加入活性炭C(ads)使该反应的活化能___________ (填“升高”“降低”或“不变”)。
② 与
与 制备“合成气”的反应为
制备“合成气”的反应为___________ 反应(填“放热”或“吸热”),其热化学方程式为___________ ( 用
用 表示),能量变化图中:
表示),能量变化图中:
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(1)一定条件下,
 分解反应
分解反应 的部分反应历程如下图所示。
的部分反应历程如下图所示。
①该历程图表示
②
 分解反应
分解反应A.高温下能自发进行 B.低温下能自发进行
C.任何温度都能自发进行 D.任何温度都不能自发进行
(2)科学家提出以吸附性活性炭
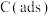 为催化剂,利用
为催化剂,利用 与
与 制备“合成气”(
制备“合成气”( 、
、 )。其反应历程分两步,反应历程的能量变化如下图:
)。其反应历程分两步,反应历程的能量变化如下图:
反应Ⅰ:
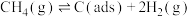 (慢反应)
(慢反应)反应Ⅱ:
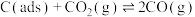 (快反应)
(快反应)①加入活性炭C(ads)使该反应的活化能
②
 与
与 制备“合成气”的反应为
制备“合成气”的反应为 用
用 表示),能量变化图中:
表示),能量变化图中:
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
您最近一年使用:0次
4 . 由 -羟基丁酸
-羟基丁酸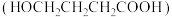 生成
生成 -丁内酯(
-丁内酯( )的反应为:HOCH2CH2CH2COOH
)的反应为:HOCH2CH2CH2COOH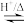
 +H2O
+H2O 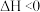 ,在
,在 时,溶液中
时,溶液中 -羟基丁酸的初始浓度为
-羟基丁酸的初始浓度为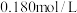 ,随着反应的进行,测得
,随着反应的进行,测得 丁内酯浓度随时间的变化如表所示。
丁内酯浓度随时间的变化如表所示。
(1)在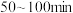 内,以
内,以 -丁内酯的浓度变化表示的反应速率为
-丁内酯的浓度变化表示的反应速率为___________ mol∙L-1∙min-1。
(2)在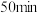 时,
时, -羟基丁酸的转化率为
-羟基丁酸的转化率为___________ (结果保留一位小数)。
(3)该反应达到平衡后,升高温度,平衡___________ 移动(填“正向”“不”或“逆向”)。
(4)保持其它条件不变,增大溶液中 -羟基丁酸的初始浓度,其平衡转化率将
-羟基丁酸的初始浓度,其平衡转化率将___________ (填“增大”“减小”或“不变”)。
(5)关于该反应的下列说法正确的是___________(填序号)。
(6) 时,该反应的平衡常数
时,该反应的平衡常数
___________ 。相同温度下,某溶液中发生上述反应,当 -丁内酯的浓度为
-丁内酯的浓度为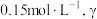 -羟基丁酸的浓度为
-羟基丁酸的浓度为 时,反应
时,反应___________ (填“正向进行”“逆向进行”或“已平衡”)。
 -羟基丁酸
-羟基丁酸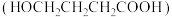 生成
生成 -丁内酯(
-丁内酯( )的反应为:HOCH2CH2CH2COOH
)的反应为:HOCH2CH2CH2COOH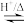
 +H2O
+H2O 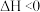 ,在
,在 时,溶液中
时,溶液中 -羟基丁酸的初始浓度为
-羟基丁酸的初始浓度为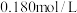 ,随着反应的进行,测得
,随着反应的进行,测得 丁内酯浓度随时间的变化如表所示。
丁内酯浓度随时间的变化如表所示。 | 21 | 50 | 80 | 100 | 120 | 160 | 220 |  |
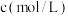 | 0.024 | 0.050 | 0.071 | 0.081 | 0.090 | 0.104 | 0.116 | 0.132 |
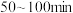 内,以
内,以 -丁内酯的浓度变化表示的反应速率为
-丁内酯的浓度变化表示的反应速率为(2)在
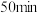 时,
时, -羟基丁酸的转化率为
-羟基丁酸的转化率为(3)该反应达到平衡后,升高温度,平衡
(4)保持其它条件不变,增大溶液中
 -羟基丁酸的初始浓度,其平衡转化率将
-羟基丁酸的初始浓度,其平衡转化率将(5)关于该反应的下列说法正确的是___________(填序号)。
| A.达到平衡后,升高温度正反应速率减小,逆反应速率增大 |
B.当 -羟基丁酸的正反应速率与 -羟基丁酸的正反应速率与 -丁内酯的逆反应速率相等时,说明达到了平衡 -丁内酯的逆反应速率相等时,说明达到了平衡 |
C.当 -羟基丁酸和 -羟基丁酸和 -丁内酯的浓度相等时,说明达到了平衡 -丁内酯的浓度相等时,说明达到了平衡 |
D.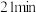 时的逆反应速率小于 时的逆反应速率小于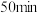 时的正反应速率 时的正反应速率 |
 时,该反应的平衡常数
时,该反应的平衡常数
 -丁内酯的浓度为
-丁内酯的浓度为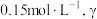 -羟基丁酸的浓度为
-羟基丁酸的浓度为 时,反应
时,反应
您最近一年使用:0次
5 . 下列图示或化学用语表示正确的是
| A | B | C | D |
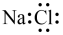 | 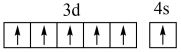 | 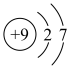 |  |
| NaCl的电子式 | 基态Cr原子的价层电子轨道表示式 |  的离子结构示意图 的离子结构示意图 | 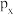 轨道的电子云轮廓图 轨道的电子云轮廓图 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是


A.图中 和 和 可分别表示 可分别表示 温度下 温度下 饱和溶液中 饱和溶液中 与 与 的浓度 的浓度 |
B.图中各点对应的 的关系为 的关系为 |
C.向 点的溶液中加入少量 点的溶液中加入少量 固体,溶液组成由 固体,溶液组成由 沿 沿 线向 线向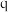 方向移动 方向移动 |
D.温度降低时,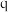 点的饱和溶液的组成由 点的饱和溶液的组成由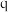 沿 沿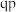 线向 线向 方向移动 方向移动 |
您最近一年使用:0次
7 . 下列说法正确的是
A.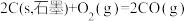 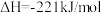 ,则石墨的燃烧热为 ,则石墨的燃烧热为 |
B.已知 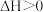 则金刚石比石墨稳定 则金刚石比石墨稳定 |
C.已知稀溶液中,  ,则稀醋酸与稀氢氧化钠溶液反应生成1mol水时放热57.3kJ ,则稀醋酸与稀氢氧化钠溶液反应生成1mol水时放热57.3kJ |
D.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 相同 相同 |
您最近一年使用:0次
解题方法
8 . Ⅰ.化学电源在生产生活中有着广泛的应用。
(1)下列化学方程式表示的化学反应能够设计成原电池的是___________
(2)为了探究化学反应中的能量变化,某同学用相同的 棒和相同浓度、相同体积的稀
棒和相同浓度、相同体积的稀 溶液,设计了两个实验(如下图)。有关实验现象,下列说法正确的是___________
溶液,设计了两个实验(如下图)。有关实验现象,下列说法正确的是___________

Ⅱ.以氨气替代氢气研发氨燃料电池是当前科研的一个热点。
(3)氨燃料电池使用的电解质溶液是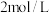 的
的 溶液,电池反应为:
溶液,电池反应为: ,该电池负极的电极反应为:
,该电池负极的电极反应为:___________ ,当反应消耗 时,从理论上计算,外电路中通过电子的电量为
时,从理论上计算,外电路中通过电子的电量为___________ (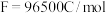 )。
)。
(4)用上述氨燃料电池接如图A、B两极(C、D、E、F都是惰性电极)。电源接通后,F电极附近溶液呈红色。
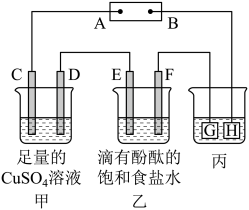
①甲池中C电极为___________ 极,乙池中发生的离子反应方程式为___________ 。
②丙装置是验证外加电流法对钢铁设备的保护(电解液为盐酸酸化的氯化钠溶液),钢铁应该接在___________ 处(填G或H)。为了证明铁能否被保护,可先取少量电解后的溶液于试管中,再向试管中加入___________ (填化学式)溶液,观察是否产生特征蓝色沉淀。
(1)下列化学方程式表示的化学反应能够设计成原电池的是___________
A.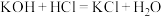 | B. |
C.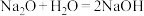 | D. |
(2)为了探究化学反应中的能量变化,某同学用相同的
 棒和相同浓度、相同体积的稀
棒和相同浓度、相同体积的稀 溶液,设计了两个实验(如下图)。有关实验现象,下列说法正确的是___________
溶液,设计了两个实验(如下图)。有关实验现象,下列说法正确的是___________
| A.消耗相同质量的Zn,图Ⅰ中产生的热能大于图Ⅱ |
| B.消耗相同质量的Zn,图Ⅰ中产生的热能等于图Ⅱ |
| C.图Ⅰ和图Ⅱ的锌棒表面均有大量气泡产生 |
| D.图Ⅱ中产生气体的速率比Ⅰ慢 |
Ⅱ.以氨气替代氢气研发氨燃料电池是当前科研的一个热点。
(3)氨燃料电池使用的电解质溶液是
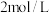 的
的 溶液,电池反应为:
溶液,电池反应为: ,该电池负极的电极反应为:
,该电池负极的电极反应为: 时,从理论上计算,外电路中通过电子的电量为
时,从理论上计算,外电路中通过电子的电量为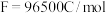 )。
)。(4)用上述氨燃料电池接如图A、B两极(C、D、E、F都是惰性电极)。电源接通后,F电极附近溶液呈红色。

①甲池中C电极为
②丙装置是验证外加电流法对钢铁设备的保护(电解液为盐酸酸化的氯化钠溶液),钢铁应该接在
您最近一年使用:0次
解题方法
9 . 2022年诺贝尔化学奖授予了对点击化学和生物正交化学做出贡献的三位科学家。我国科学家在寻找新的点击反应砌块的过程中,意外发现一种安全、高效的合成化合物,其结构如图所示,其中X、Y、Z和W是原子序数依次增大的短周期元素,Y与W是同一主族元素,X与Y为相邻元素,下列说法正确的是
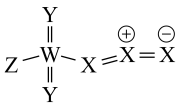
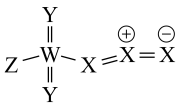
A.原子半径: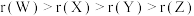 |
B.简单氢化物的沸点: |
C.电解 的简单氢化物水溶液可制得 的简单氢化物水溶液可制得 和 和 |
| D.同周期主族元素中第一电离能大于X的元素有2种 |
您最近一年使用:0次
10 . 在 时,向20mL浓度为0.05mol/L的H2SO4溶液(忽略反应导致溶液的体积变化)中通入NH3,使溶液中
时,向20mL浓度为0.05mol/L的H2SO4溶液(忽略反应导致溶液的体积变化)中通入NH3,使溶液中 ,则此时溶液的pH为
,则此时溶液的pH为
 时,向20mL浓度为0.05mol/L的H2SO4溶液(忽略反应导致溶液的体积变化)中通入NH3,使溶液中
时,向20mL浓度为0.05mol/L的H2SO4溶液(忽略反应导致溶液的体积变化)中通入NH3,使溶液中 ,则此时溶液的pH为
,则此时溶液的pH为| A.5 | B.6 | C.7 | D.8 |
您最近一年使用:0次



