名校
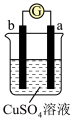
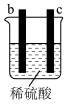
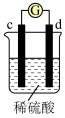
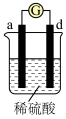
1 . 有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
由此可判断这四种金属的活动性顺序是
| 实验装置 |
|
|
| 部分实验现象 | a极质量减小,b极质量增加 | b极有气体产生,c极无变化 |
| 实验装置 |
|
|
| 部分实验现象 | d极溶解,c极有气体产生 | 电流计指示在导线中电流从a极流向d极 |
A. | B. |
C. | D. |
您最近一年使用:0次
2024-04-21更新
|
209次组卷
|
6卷引用:湖南省邵东市第一中学2022-2023学年高一上学期期末测试化学试题
湖南省邵东市第一中学2022-2023学年高一上学期期末测试化学试题(已下线)专题02 化学反应与能量变化-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)宁夏石嘴山市第三中学2023-2024学年高一下学期3月月考化学试题河南省信阳高级中学2023-2024学年高一下学期4月月考化学试题广西来宾市忻城县高级中学2023-2024学年高一下学期期中考试化学试卷云南省下关第一中学2023-2024学年高一下学期5月期中考试化学试题
名校
解题方法
2 . 回答下列问题
(1)已知:
则2H2(g)+O2(g) =2H2O(g) ΔH=___________ kJ·mol-1。
(2)消除汽车尾气中的NO、CO,有利于减少PM2.5的排放。已知如下信息:

①N2(g)+O2(g) =2NO(g) ΔH1=___________
②2CO(g)+O2(g) = 2CO2(g) ΔH2=-565 kJ·mol-1
在催化剂作用下NO和CO转化为无毒气体,写出反应的热化学方程式:___________ 。
(3)CO和H2是工业上最常用的合成气,该合成气的制备方法很多,它们也能合成许多重要的有机物。制备该合成气的一种方法是以CH4和H2O为原料,有关反应的能量变化如图所示。
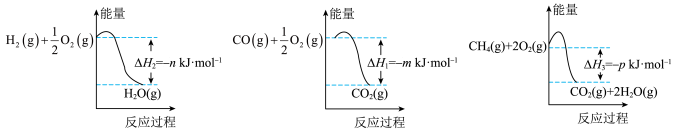
CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为___________ 。
(4)下图是锌锰干电池基本构造图,
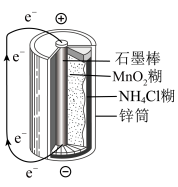
该电池的负极材料是___________ ,工作时NH 在正极放电产生两种气体,其中一种气体分子是含10e-的微粒,正极的电极反应式是
在正极放电产生两种气体,其中一种气体分子是含10e-的微粒,正极的电极反应式是___________ ;电路中每通过0.2 mol e-,负极质量减少___________ 。
(1)已知:
| 化学键 | H-H | O=O | O-H |
| 键能(kJ·mol-1) | 436 | 496 | 463 |
(2)消除汽车尾气中的NO、CO,有利于减少PM2.5的排放。已知如下信息:

①N2(g)+O2(g) =2NO(g) ΔH1=
②2CO(g)+O2(g) = 2CO2(g) ΔH2=-565 kJ·mol-1
在催化剂作用下NO和CO转化为无毒气体,写出反应的热化学方程式:
(3)CO和H2是工业上最常用的合成气,该合成气的制备方法很多,它们也能合成许多重要的有机物。制备该合成气的一种方法是以CH4和H2O为原料,有关反应的能量变化如图所示。

CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为
(4)下图是锌锰干电池基本构造图,

该电池的负极材料是
 在正极放电产生两种气体,其中一种气体分子是含10e-的微粒,正极的电极反应式是
在正极放电产生两种气体,其中一种气体分子是含10e-的微粒,正极的电极反应式是
您最近一年使用:0次
名校
解题方法
3 . 下列有关实验的操作、现象和实验结论错误
| 操作 | 现象 | 实验结论 | |
| A | 将SO2通入酸性KMnO4溶液 | 溶液褪色 | SO2具有还原性 |
| B | 石蜡油加强热,将产生的气体通入Br2的CCl4溶液 | 溶液红棕色变无色 | 气体中含有不饱和烃 |
| C | 向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水 | 溶液显红色 | 该溶液中一定含Fe2+ |
| D | 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的Cu(OH)2悬浊液 | 无砖红色沉淀生成 | 蔗糖未发生水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 下列离子方程式书写正确的是
A. 溶于水: 溶于水: |
B. 与稀 与稀 反应: 反应: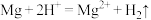 |
C. 溶液腐蚀覆铜板: 溶液腐蚀覆铜板: |
| D.向FeCl3溶液中滴加氨水:Fe3++3OH-=Fe(OH)3↓ |
您最近一年使用:0次
名校
解题方法
5 . 关于下列各装置图的叙述中,正确的是
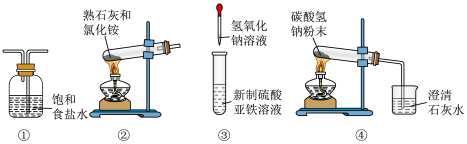

| A.装置①是洗气装置,除去氯气中的氯化氢 |
| B.实验室用装置②制取氨气 |
| C.装置③可用于制备氢氧化亚铁并观察其颜色 |
| D.装置④可验证碳酸氢钠受热分解 |
您最近一年使用:0次
6 . 乙烯是重要有机化工原料。结合以下路线回答: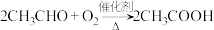 ;其中F为高分子化合物
;其中F为高分子化合物
(1)物质B所含官能团的名称为___________ ;
(2)D的结构简式为___________ ;
(3)反应①、⑥所涉及的反应类型是___________ 、___________ ;
(4)写出反应④的化学方程式为___________ ;
(5)写出反应⑦的化学方程式为___________ ;
(6)关于CH2=CH2的说法正确的是___________;
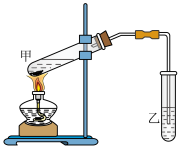
(7)在实验室里可以用如图所示的装置来制取G,乙中所盛的试剂为___________ ,该装置图中有一个明显的错误是___________ 。
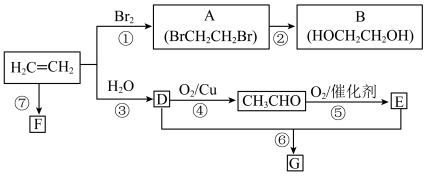
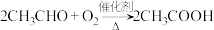 ;其中F为高分子化合物
;其中F为高分子化合物(1)物质B所含官能团的名称为
(2)D的结构简式为
(3)反应①、⑥所涉及的反应类型是
(4)写出反应④的化学方程式为
(5)写出反应⑦的化学方程式为
(6)关于CH2=CH2的说法正确的是___________;
| A.易溶于水 | B.是平面结构的分子 |
| C.能被高锰酸钾氧化 | D.在一定条件下能发生加聚反应 |
(7)在实验室里可以用如图所示的装置来制取G,乙中所盛的试剂为
您最近一年使用:0次
名校
解题方法
7 . I.汽车尾气中含有CO、NO等有害气体,某新型催化剂能促使NO、CO转化为两种无毒气体。T ℃时,将0.8 mol NO和0.8 mol CO充入容积为2 L的密闭容器中,模拟汽车尾气转化,容器中NO的物质的量随时间变化如图所示。___________ 。
(2)反应开始至10 min,v(NO)=___________ mol/(L·min)。
(3)下列说法正确的是___________ 。
a.新型催化剂可以加快NO、CO的转化
b.该反应进行到10 min时达到化学平衡状态
c.平衡时CO的浓度是0.4 mol/L
Ⅱ.在恒温下,将4mol的H2(g)和2mol的CO(g)充入1L恒容的密闭容器中发生如下反应:CO(g) + 2H2(g) CH3OH(g)。下图是CO(g)和 CH3OH(g)的浓度随时间变化的关系图,
CH3OH(g)。下图是CO(g)和 CH3OH(g)的浓度随时间变化的关系图,
(4)0-5min内,H2 (g)的平均反应速率是___________ mol/(L·min)。
(5)12min时,v正___________ v逆(填“>”“<”或“=”)。
(6)设起始压强为P,平衡时压强为P0,则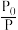 的值为
的值为___________ 。
(7)根据反应原理下列描述能说明反应达到最大限度的是___________。
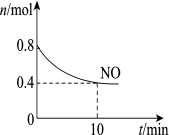
(2)反应开始至10 min,v(NO)=
(3)下列说法正确的是
a.新型催化剂可以加快NO、CO的转化
b.该反应进行到10 min时达到化学平衡状态
c.平衡时CO的浓度是0.4 mol/L
Ⅱ.在恒温下,将4mol的H2(g)和2mol的CO(g)充入1L恒容的密闭容器中发生如下反应:CO(g) + 2H2(g)
 CH3OH(g)。下图是CO(g)和 CH3OH(g)的浓度随时间变化的关系图,
CH3OH(g)。下图是CO(g)和 CH3OH(g)的浓度随时间变化的关系图,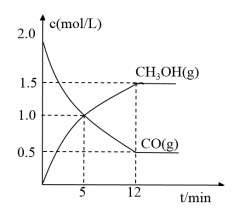
(4)0-5min内,H2 (g)的平均反应速率是
(5)12min时,v正
(6)设起始压强为P,平衡时压强为P0,则
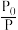 的值为
的值为(7)根据反应原理下列描述能说明反应达到最大限度的是___________。
| A.CO(g)、H2(g)、CH3OH(g)的物质的量比为1∶2∶1 |
| B.混合气体的压强不随时间的变化而改变 |
| C.单位时间内每消耗2amolH2(g),同时生成amolCH3OH(g) |
| D.反应速率:v(H2)=2v(CO) |
您最近一年使用:0次
2024-03-17更新
|
1151次组卷
|
3卷引用:湖南省邵阳市绥宁县第一中2022-2023学年高一下学期期末考试化学试题
湖南省邵阳市绥宁县第一中2022-2023学年高一下学期期末考试化学试题(已下线)重难点04 化学反应速率及平衡图像问题的分析-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)名校期末好题汇编-化学反应与能量(非选择题)
名校
解题方法
8 . 氮、硫的氧化物都会引起环境问题,越来越引起人们的重视。
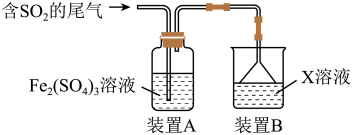
Ⅰ.某兴趣小组用Fe2(SO4)3溶液吸收含SO2的尾气(SO2的体积分数约为10%,其余为空气),实验装置如图所示:___________ 。
(2)反应后,若要检验装置A中Fe3+是否过量,可用试剂为___________ ;若要检验SO2是否过量,可用试剂为___________ 。
(3)装置B中所用X溶液常为碱溶液,其作用是___________ 。
(4)若实验测得反应后的装置A中不含有SO2,为测定其中所含FeSO4的物质的量浓度,现进行如下实验:取20.00 mL装置A中溶液,向其中逐滴加入0.100 0 mol/L Ce(SO4)2溶液,发生反应Fe2++Ce4+= Ce3++Fe3+,当反应恰好完全时,共消耗Ce(SO4)2溶液18.00 mL。则FeSO4的物质的量浓度为___________ 。
Ⅱ.工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
(5)水吸收法。结合化学方程式说明用水吸收NO2的缺陷___________ 。
(6)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学方程式:___________ 。
Ⅰ.某兴趣小组用Fe2(SO4)3溶液吸收含SO2的尾气(SO2的体积分数约为10%,其余为空气),实验装置如图所示:
(2)反应后,若要检验装置A中Fe3+是否过量,可用试剂为
(3)装置B中所用X溶液常为碱溶液,其作用是
(4)若实验测得反应后的装置A中不含有SO2,为测定其中所含FeSO4的物质的量浓度,现进行如下实验:取20.00 mL装置A中溶液,向其中逐滴加入0.100 0 mol/L Ce(SO4)2溶液,发生反应Fe2++Ce4+= Ce3++Fe3+,当反应恰好完全时,共消耗Ce(SO4)2溶液18.00 mL。则FeSO4的物质的量浓度为
Ⅱ.工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
(5)水吸收法。结合化学方程式说明用水吸收NO2的缺陷
(6)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学方程式:
您最近一年使用:0次
9 . NA为阿伏加德罗常数的值。下列说法正确的是
| A.1.7 g NH3中含有的质子数约为6.02×1023 |
| B.1 mol N2与3 mol H2反应生成的NH3分子数为2NA |
| C.标准状况下,2.24 L CCl4含有的共价键数为0.4NA |
D.0.1 mol/L NH4Cl溶液中的NH 数约为0.1NA 数约为0.1NA |
您最近一年使用:0次
2024-03-17更新
|
394次组卷
|
3卷引用:湖南省邵阳市绥宁县第一中2022-2023学年高一下学期期末考试化学试题
名校
10 . 化学与生活密切相关,下列叙述正确的是
| A.天然气、沼气和太阳能分别属于化石能源、可再生能源和二次能源 |
| B.高纯度的硅单质广泛用于制作光导纤维,光导纤维遇碱会“断路” |
| C.绿色化学的核心是应用化学原理对环境污染进行治理 |
| D.食品中添加适量的二氧化硫可以起到漂白、防腐和抗氧化等作用 |
您最近一年使用:0次