氮、硫的氧化物都会引起环境问题,越来越引起人们的重视。
Ⅰ.某兴趣小组用Fe2(SO4)3溶液吸收含SO2的尾气(SO2的体积分数约为10%,其余为空气),实验装置如图所示:
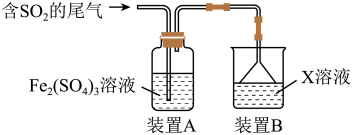
(1)装置A中SO2与Fe2(SO4)3溶液反应生成FeSO4,写出该反应的化学方程式:___________ 。
(2)反应后,若要检验装置A中Fe3+是否过量,可用试剂为___________ ;若要检验SO2是否过量,可用试剂为___________ 。
(3)装置B中所用X溶液常为碱溶液,其作用是___________ 。
(4)若实验测得反应后的装置A中不含有SO2,为测定其中所含FeSO4的物质的量浓度,现进行如下实验:取20.00 mL装置A中溶液,向其中逐滴加入0.100 0 mol/L Ce(SO4)2溶液,发生反应Fe2++Ce4+= Ce3++Fe3+,当反应恰好完全时,共消耗Ce(SO4)2溶液18.00 mL。则FeSO4的物质的量浓度为___________ 。
Ⅱ.工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
(5)水吸收法。结合化学方程式说明用水吸收NO2的缺陷___________ 。
(6)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学方程式:___________ 。
Ⅰ.某兴趣小组用Fe2(SO4)3溶液吸收含SO2的尾气(SO2的体积分数约为10%,其余为空气),实验装置如图所示:

(1)装置A中SO2与Fe2(SO4)3溶液反应生成FeSO4,写出该反应的化学方程式:
(2)反应后,若要检验装置A中Fe3+是否过量,可用试剂为
(3)装置B中所用X溶液常为碱溶液,其作用是
(4)若实验测得反应后的装置A中不含有SO2,为测定其中所含FeSO4的物质的量浓度,现进行如下实验:取20.00 mL装置A中溶液,向其中逐滴加入0.100 0 mol/L Ce(SO4)2溶液,发生反应Fe2++Ce4+= Ce3++Fe3+,当反应恰好完全时,共消耗Ce(SO4)2溶液18.00 mL。则FeSO4的物质的量浓度为
Ⅱ.工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
(5)水吸收法。结合化学方程式说明用水吸收NO2的缺陷
(6)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学方程式:
更新时间:2024-03-30 16:17:57
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】中国疾控中心指出,消毒是疫情防控的重要措施。含氯消毒剂是一种高效、安全的杀菌消毒剂。
(1)84消毒液是一种家庭常用消毒剂,但与洁厕灵(主要成分为盐酸)混合使用,混合时会产生黄绿色的有毒气体,其反应的离子方程式为___________ 。
(2) 是国际上公认的高效、安全的杀菌消毒剂。工业制备
是国际上公认的高效、安全的杀菌消毒剂。工业制备 的反应原理为:
的反应原理为: ,X的化学式为
,X的化学式为______ ,每生成1mol ,反应中转移电子
,反应中转移电子______ mol。在进行饮用水消毒时, 可转化为
可转化为 ,1mol
,1mol 与
与_______ g(保留两位小数)NaClO氧化消毒能力相当(用得电子数目多少衡量氧化消毒能力强弱)。
(1)84消毒液是一种家庭常用消毒剂,但与洁厕灵(主要成分为盐酸)混合使用,混合时会产生黄绿色的有毒气体,其反应的离子方程式为
(2)
 是国际上公认的高效、安全的杀菌消毒剂。工业制备
是国际上公认的高效、安全的杀菌消毒剂。工业制备 的反应原理为:
的反应原理为: ,X的化学式为
,X的化学式为 ,反应中转移电子
,反应中转移电子 可转化为
可转化为 ,1mol
,1mol 与
与
您最近一年使用:0次
【推荐2】氧化剂和还原剂在生产生活中广泛使用。
(1)高锰酸钾和氢溴酸溶液可以发生如下反应:2KMnO4+16HBr=5Br2+2MnBr2+2KBr+8H2O。若有0.8mol还原剂被氧化,则转移的电子数是________ 。
(2)人体内所含铁元素以Fe2+和Fe3+的形式存在。市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为____ ,但Fe2+在酸性条件下很容易被空气中的氧气氧化,写出该反应的离子方程式__________ 。
(3)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。
①H3PO2中P元素的化合价为__________ 。
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂物质的量之比为4∶1,则氧化产物为_________ 。
(1)高锰酸钾和氢溴酸溶液可以发生如下反应:2KMnO4+16HBr=5Br2+2MnBr2+2KBr+8H2O。若有0.8mol还原剂被氧化,则转移的电子数是
(2)人体内所含铁元素以Fe2+和Fe3+的形式存在。市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为
(3)H3PO2和NaH2PO2均可将溶液中的Ag+还原为Ag,从而可用于化学镀银。
①H3PO2中P元素的化合价为
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂物质的量之比为4∶1,则氧化产物为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】KMnO4是一种典型的强氧化剂。完成下列填空:
Ⅰ.在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
① MnO4-+ Cu2S + H+→ Cu2+ + SO2↑ + Mn2+ + H2O (未配平)
② MnO4-+ CuS + H+ → Cu2+ + SO2↑ + Mn2++ H2O (未配平)
(1)下列关于反应①的说法中错误的是_________ (选填编号)。
a.被氧化的元素是Cu和S b.氧化剂与还原剂的物质的量之比为8:5
c.还原性的强弱关系是: Mn2+<Cu2S d.每生成2.24 L(标况) SO2,转移0.6mol电子
(2)配平并标出反应②中电子转移的方向和数目 :_____
MnO4-+ CuS + H+ → Cu2+ + SO2↑ + Mn2++ H2O
(3)若将H2O2加入KMnO4有反应:2KMnO4+7H2O2+3H2SO4= K2SO4+2MnSO4+6O2↑+10H2O,则被1molKMnO4氧化的H2O2是_________ mol。
II.已知在碱性条件下:MnO4-+e-—→MnO42- (绿色)
(4) 将KMnO4溶液滴入NaOH溶液中微热,得到透明的绿色溶液,并且有气泡生成,写出反应的离子方程式_____________ 。
Ⅰ.在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
① MnO4-+ Cu2S + H+→ Cu2+ + SO2↑ + Mn2+ + H2O (未配平)
② MnO4-+ CuS + H+ → Cu2+ + SO2↑ + Mn2++ H2O (未配平)
(1)下列关于反应①的说法中错误的是
a.被氧化的元素是Cu和S b.氧化剂与还原剂的物质的量之比为8:5
c.还原性的强弱关系是: Mn2+<Cu2S d.每生成2.24 L(标况) SO2,转移0.6mol电子
(2)配平
MnO4-+ CuS + H+ → Cu2+ + SO2↑ + Mn2++ H2O
(3)若将H2O2加入KMnO4有反应:2KMnO4+7H2O2+3H2SO4= K2SO4+2MnSO4+6O2↑+10H2O,则被1molKMnO4氧化的H2O2是
II.已知在碱性条件下:MnO4-+e-—→MnO42- (绿色)
(4) 将KMnO4溶液滴入NaOH溶液中微热,得到透明的绿色溶液,并且有气泡生成,写出反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】写出下列所对应的离子或化学方程式
(1)写出用氯化铁溶液蚀刻印刷电路板发生反应的离子方程式:___________ 。
(2)向FeSO4溶液中滴加少量酸性KMnO4溶液,若溶液紫红色褪去,证明Fe2+具有还原性。反应原理用离子方程式表示为___________ 。
(3)写出泡沫灭火器的工作原理(AlCl3与NaHCO3反应):___________ 。
(4)写出Na2O2与CO2的反应,并标出双线桥___________ 。
(1)写出用氯化铁溶液蚀刻印刷电路板发生反应的离子方程式:
(2)向FeSO4溶液中滴加少量酸性KMnO4溶液,若溶液紫红色褪去,证明Fe2+具有还原性。反应原理用离子方程式表示为
(3)写出泡沫灭火器的工作原理(AlCl3与NaHCO3反应):
(4)写出Na2O2与CO2的反应,并标出双线桥
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】高纯超细氧化铝粉是一种新型无机功能材料,以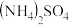 和
和 为原料制备复盐硫酸铝铵晶体[
为原料制备复盐硫酸铝铵晶体[ ],将硫酸铝铵晶体热分解可制得高纯超细氧化铝粉,其流程如下:
],将硫酸铝铵晶体热分解可制得高纯超细氧化铝粉,其流程如下:

回答下列问题:
(1)操作①需加入适量稀硫酸,其目的是_______ ,采用的纯化方法为_______ 。
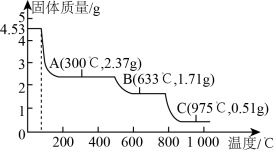
(2)取 加热分解,加热过程中固体质量随温度的变化如图所示。硫酸铝铵晶体在633℃、975℃分解生成的固体分别为
加热分解,加热过程中固体质量随温度的变化如图所示。硫酸铝铵晶体在633℃、975℃分解生成的固体分别为_______ 、_______ 。(填化学式)
(3)实验室以 和
和 为原料,在一定条件下反应生成制备纳米
为原料,在一定条件下反应生成制备纳米 的前驱体
的前驱体 沉淀,同时生成
沉淀,同时生成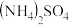 、
、 和
和 。
。 高温分解即得超细氧化铝粉。反应生成
高温分解即得超细氧化铝粉。反应生成 沉淀的化学方程式为
沉淀的化学方程式为_______ 。
(4)为了测定高纯超细氧化铝粉中 的质量分数,可用EDTA标准溶液滴定。取0.2035g高纯超细氧化铝粉溶于盐酸,加入过量的30.00mL0.1600
的质量分数,可用EDTA标准溶液滴定。取0.2035g高纯超细氧化铝粉溶于盐酸,加入过量的30.00mL0.1600 EDTA标准溶液并加热煮沸,充分反应后,再用
EDTA标准溶液并加热煮沸,充分反应后,再用 标准溶液滴定过量的EDTA至终点,消耗
标准溶液滴定过量的EDTA至终点,消耗 标准溶液。已知
标准溶液。已知 、
、 与EDTA反应的化学计量数之比均为1:1。
与EDTA反应的化学计量数之比均为1:1。
①加入过量的EDTA标准溶液并加热煮沸,其原因是_______ 。
②高纯超细氧化铝粉中, 的质量分数为
的质量分数为_______ %(保留1位小数)。
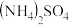 和
和 为原料制备复盐硫酸铝铵晶体[
为原料制备复盐硫酸铝铵晶体[ ],将硫酸铝铵晶体热分解可制得高纯超细氧化铝粉,其流程如下:
],将硫酸铝铵晶体热分解可制得高纯超细氧化铝粉,其流程如下:
回答下列问题:
(1)操作①需加入适量稀硫酸,其目的是
(2)取
 加热分解,加热过程中固体质量随温度的变化如图所示。硫酸铝铵晶体在633℃、975℃分解生成的固体分别为
加热分解,加热过程中固体质量随温度的变化如图所示。硫酸铝铵晶体在633℃、975℃分解生成的固体分别为
(3)实验室以
 和
和 为原料,在一定条件下反应生成制备纳米
为原料,在一定条件下反应生成制备纳米 的前驱体
的前驱体 沉淀,同时生成
沉淀,同时生成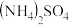 、
、 和
和 。
。 高温分解即得超细氧化铝粉。反应生成
高温分解即得超细氧化铝粉。反应生成 沉淀的化学方程式为
沉淀的化学方程式为(4)为了测定高纯超细氧化铝粉中
 的质量分数,可用EDTA标准溶液滴定。取0.2035g高纯超细氧化铝粉溶于盐酸,加入过量的30.00mL0.1600
的质量分数,可用EDTA标准溶液滴定。取0.2035g高纯超细氧化铝粉溶于盐酸,加入过量的30.00mL0.1600 EDTA标准溶液并加热煮沸,充分反应后,再用
EDTA标准溶液并加热煮沸,充分反应后,再用 标准溶液滴定过量的EDTA至终点,消耗
标准溶液滴定过量的EDTA至终点,消耗 标准溶液。已知
标准溶液。已知 、
、 与EDTA反应的化学计量数之比均为1:1。
与EDTA反应的化学计量数之比均为1:1。①加入过量的EDTA标准溶液并加热煮沸,其原因是
②高纯超细氧化铝粉中,
 的质量分数为
的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知:①MnO4- + e→ MnO42-(绿色) (强碱性条件)
②MnO4- + 8H+ + 5e → Mn2+(无色)+ 4H2O (强酸性条件)
(1)在KOH溶液中,KMnO4 与 K2SO3溶液发生反应,还原剂为_______________ ,还原产物为___________ 。
(2)将KMnO4溶液滴入NaOH溶液微热,得到透明的绿色溶液,写出反应的离子方程式______ 。
(3)用酸性KMnO4溶液与亚铁盐的反应证明Fe2+具有还原性、MnO4-具有氧化性,最合适的亚铁盐是___________ ,可用来酸化KMnO4溶液的试剂是_______ (均选填编号)。
a.FeSO4 b.FeCl2 c.Fe(NO3)2 d.盐酸 e.硝酸 f.稀硫酸
(4)向20 mL浓度为0.02 mol/L的KMnO4溶液中滴加FeSO4溶液,使MnO4-全部转化为Mn2+,则反应前需向KMnO4溶液加入c(H+) = 1 mol/L的酸不少于____________ mL。
②MnO4- + 8H+ + 5e → Mn2+(无色)+ 4H2O (强酸性条件)
(1)在KOH溶液中,KMnO4 与 K2SO3溶液发生反应,还原剂为
(2)将KMnO4溶液滴入NaOH溶液微热,得到透明的绿色溶液,写出反应的离子方程式
(3)用酸性KMnO4溶液与亚铁盐的反应证明Fe2+具有还原性、MnO4-具有氧化性,最合适的亚铁盐是
a.FeSO4 b.FeCl2 c.Fe(NO3)2 d.盐酸 e.硝酸 f.稀硫酸
(4)向20 mL浓度为0.02 mol/L的KMnO4溶液中滴加FeSO4溶液,使MnO4-全部转化为Mn2+,则反应前需向KMnO4溶液加入c(H+) = 1 mol/L的酸不少于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下图是氮元素的各种价态与物质类别的对应关系:
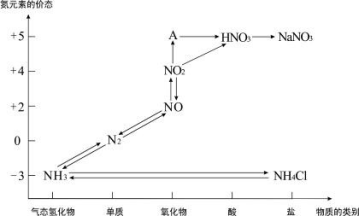
(1)根据 A 对应的化合价和物质类别,A 的摩尔质量是______ g·mol-1,从氮元素的 化合价能否发生变化的角度判断,图中既有 氧化性又有还原性的化合物有_____________ 。
(2)汽车尾气中含有 CO 和 NOx 等多种有 害气体,若在汽车的排气管上安装一种催化 转化装置,可使 CO 与 NO 反应,生成两种 无毒气体,则该反应的化学方程式为________________________________________ 。

(1)根据 A 对应的化合价和物质类别,A 的摩尔质量是
(2)汽车尾气中含有 CO 和 NOx 等多种有 害气体,若在汽车的排气管上安装一种催化 转化装置,可使 CO 与 NO 反应,生成两种 无毒气体,则该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】“环境是民生,青山是美丽,蓝天也是幸福”。对生态环境污染问题,我们必须正视问题、着力解决问题。
Ⅰ.随着我国汽车年销量的大幅增加,空气环境受到了很大的污染。汽车尾气净化装置“催化转化器”是防止尾气(含一氧化碳、氮氧化物等气体)污染的有效方法,能使尾气中的一氧化碳和氮氧化物发生反应生成可参与大气生态循环的无毒气体。
(1)汽车尾气中易造成光化学烟雾的物质是______ 。
a.氮氧化物 b.二氧化碳 c.一氧化碳
(2)汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示:______ 。
(3)可利用CH4等气体除去烟气中的氮氧化物,生成物为可参与大气循环的气体,请写出CH4与NO反应的化学方程式______ 。
(4)采用NaOH溶液可以吸收废气中的氮氧化物,反应的化学方程式如下: 。若反应时消耗了10L
。若反应时消耗了10L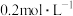 的NaOH溶液,则反应中转移电子的物质的量
的NaOH溶液,则反应中转移电子的物质的量______ mol。
Ⅱ.硫有多种化合物,如H2S、SO2等,它们对环境均有一定的影响,含硫化合物的综合利用既可以消除污染,又可以带来一定的经济效益。
(5)煤液化过程中产生的H2S可生产硫酸,部分过程如图所示:______ 。
(6)有学者提出利用Fe3+、Fe2+等离子的作用,在常温下将SO2氧化成 而实现SO2的回收利用,写出Fe3+将SO2氧化成
而实现SO2的回收利用,写出Fe3+将SO2氧化成 反应的离子方程式
反应的离子方程式______ 。
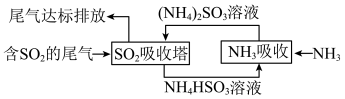
(7)某企业利用下列流程综合处理工厂排放的含;SO2的烟气,以减少其对环境造成的污染。“SO2吸收塔”中发生反应的化学方程式为______ ,该流程中可循环利用的物质为______ (填化学式)。
Ⅰ.随着我国汽车年销量的大幅增加,空气环境受到了很大的污染。汽车尾气净化装置“催化转化器”是防止尾气(含一氧化碳、氮氧化物等气体)污染的有效方法,能使尾气中的一氧化碳和氮氧化物发生反应生成可参与大气生态循环的无毒气体。
(1)汽车尾气中易造成光化学烟雾的物质是
a.氮氧化物 b.二氧化碳 c.一氧化碳
(2)汽车尾气装置里,气体在催化剂表面吸附与解吸作用的过程如图所示:
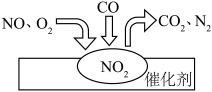
(3)可利用CH4等气体除去烟气中的氮氧化物,生成物为可参与大气循环的气体,请写出CH4与NO反应的化学方程式
(4)采用NaOH溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
 。若反应时消耗了10L
。若反应时消耗了10L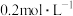 的NaOH溶液,则反应中转移电子的物质的量
的NaOH溶液,则反应中转移电子的物质的量Ⅱ.硫有多种化合物,如H2S、SO2等,它们对环境均有一定的影响,含硫化合物的综合利用既可以消除污染,又可以带来一定的经济效益。
(5)煤液化过程中产生的H2S可生产硫酸,部分过程如图所示:

(6)有学者提出利用Fe3+、Fe2+等离子的作用,在常温下将SO2氧化成
 而实现SO2的回收利用,写出Fe3+将SO2氧化成
而实现SO2的回收利用,写出Fe3+将SO2氧化成 反应的离子方程式
反应的离子方程式(7)某企业利用下列流程综合处理工厂排放的含;SO2的烟气,以减少其对环境造成的污染。“SO2吸收塔”中发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)镁称为“国防金属”,常用作还原剂和脱氧剂,二氧化碳常被用作灭火剂,但是当把点燃的镁条伸入盛有CO2的集气瓶中时,镁条却能继续燃烧。请写出化学方程式____________ 。
(2)下图变化是工业制硝酸的主要途径NH3→NO→NO2→HNO3请写出NH3→NO的化学方程式___________________ 。硝酸生产过程排放出来的NO是大气污染物之一。目前有一种治理方法,是在400℃左右且有催化剂存在的情况下,用氨把NO还原成无色无毒气体直接排放到空气中,化学方程式为______________ 。
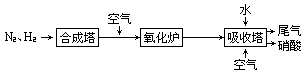
(2)下图变化是工业制硝酸的主要途径NH3→NO→NO2→HNO3请写出NH3→NO的化学方程式

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】硫及其化合物在工业上有广泛的用途。回答下列问题:
(1)硫是一种黄色晶体,化学性质比较活泼,能与许多金属单质反应,硫与铜在加热条件下反应的产物为_______ 。
(2)不同价态含硫物质在一定条件下能够相互转化,标准状况下11.2 LH2S与足量SO2反应,转移的电子数为_______ ,H2S分子中化学键的类型为_______ (填 “离子键”、“极性共价键”或“非极性共价键”)。
(3)黄铁矿(FeS2)是工业上制硫酸的重要原料,在氧气中煅烧生成Fe2O3和SO2,其煅烧的化学方程式为_______ 。
(4)在实验室中,几位同学围绕浓硫酸的化学性质进行了如下实验探究:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀;然后再加入适量浓硫酸,迅速搅拌。
①可以观察到的现象为_______ 。
②上述实验现象表明浓硫酸具有_______ (填字母)。
a.酸性 b.吸水性 c.脱水性 d.强氧化性
(5)二氧化硫及其在大气中发生反应后的生成物溶于水会形成酸雨。简述证明酸雨中含有硫酸根的实验操作步骤:_______ 。
(6)某工厂每天燃烧含硫质量分数为0.64%的煤100 t,如果煤中的硫全部转化为SO2,且产生的SO2全部用来生产硫酸,理论上每年(按365天计)可得到98%的浓硫酸的质量为_______ 。
(1)硫是一种黄色晶体,化学性质比较活泼,能与许多金属单质反应,硫与铜在加热条件下反应的产物为
(2)不同价态含硫物质在一定条件下能够相互转化,标准状况下11.2 LH2S与足量SO2反应,转移的电子数为
(3)黄铁矿(FeS2)是工业上制硫酸的重要原料,在氧气中煅烧生成Fe2O3和SO2,其煅烧的化学方程式为
(4)在实验室中,几位同学围绕浓硫酸的化学性质进行了如下实验探究:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀;然后再加入适量浓硫酸,迅速搅拌。
①可以观察到的现象为
②上述实验现象表明浓硫酸具有
a.酸性 b.吸水性 c.脱水性 d.强氧化性
(5)二氧化硫及其在大气中发生反应后的生成物溶于水会形成酸雨。简述证明酸雨中含有硫酸根的实验操作步骤:
(6)某工厂每天燃烧含硫质量分数为0.64%的煤100 t,如果煤中的硫全部转化为SO2,且产生的SO2全部用来生产硫酸,理论上每年(按365天计)可得到98%的浓硫酸的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
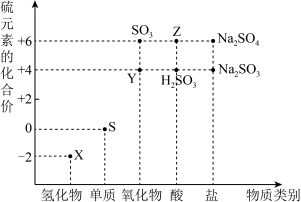
【推荐2】如图是硫元素的“价—类”二维图:___________ 。
(2) 的浓溶液与铝单质在加热条件下可以发生化学反应生成
的浓溶液与铝单质在加热条件下可以发生化学反应生成 ,该反应的化学方程式为
,该反应的化学方程式为___________ ,可用___________ 法收集 。
。
A.向上排空气 B.向下排空气 C.排饱和食盐水 D.排饱和 溶液
溶液
(3) 和
和 均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。用离子方程式解释原因
均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。用离子方程式解释原因___________ 。
(2)
 的浓溶液与铝单质在加热条件下可以发生化学反应生成
的浓溶液与铝单质在加热条件下可以发生化学反应生成 ,该反应的化学方程式为
,该反应的化学方程式为 。
。A.向上排空气 B.向下排空气 C.排饱和食盐水 D.排饱和
 溶液
溶液(3)
 和
和 均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。用离子方程式解释原因
均能使品红溶液褪色,但两种气体按一定比例同时通入品红溶液中无明显现象。用离子方程式解释原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】依据信息书写下列反应的方程式
(1)SO2是一种酸性氧化物,可制取Na2SO3,从括号内所给试剂(NaCl溶液、NaOH溶液、Na2SO4溶液)中选择合适的,完成这一反应,写出该反应的化学方程式:______ 。
(2)锶(Sr)原子的结构示意图如图所示: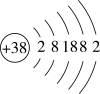 ,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:
,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:______ 。
(3)MnO2可经过如图所示的转化制取MnCO3。已知“反应Ⅱ”为复分解反应。

①写出“反应Ⅰ”的化学方程式:______ 。
②写出“反应Ⅱ”的离子方程式:______ 。
(1)SO2是一种酸性氧化物,可制取Na2SO3,从括号内所给试剂(NaCl溶液、NaOH溶液、Na2SO4溶液)中选择合适的,完成这一反应,写出该反应的化学方程式:
(2)锶(Sr)原子的结构示意图如图所示:
 ,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:
,锶能与水发生剧烈反应生成碱和氢气,写出单质锶与水反应的化学方程式:(3)MnO2可经过如图所示的转化制取MnCO3。已知“反应Ⅱ”为复分解反应。

①写出“反应Ⅰ”的化学方程式:
②写出“反应Ⅱ”的离子方程式:
您最近一年使用:0次



