1 . 一定温度时,向容积为2L的密闭容器中充入一定量的SO2和O2,发生反应:2SO2(g)+O2(g) 2SO3(g) △H=-196kJ·mol-1,一段时间后达到平衡,反应过程中测定的部分数据见下表:
2SO3(g) △H=-196kJ·mol-1,一段时间后达到平衡,反应过程中测定的部分数据见下表:
下列说法不正确的是
 2SO3(g) △H=-196kJ·mol-1,一段时间后达到平衡,反应过程中测定的部分数据见下表:
2SO3(g) △H=-196kJ·mol-1,一段时间后达到平衡,反应过程中测定的部分数据见下表:反应时间/min | n(SO2)/mol | n(O2)/mol |
0 | 2 | 1 |
5 | 1.2 |
|
10 |
| 0.4 |
15 | 0.8 |
|
| A.△H的大小与平衡移动与否无关 |
| B.相同温度下,起始时向容器中充入1.5mol SO3,达平衡时SO3的转化率为40% |
| C.保持温度不变,向平衡后的容器中再充入0.2mol SO2和0.2mol SO3时,v(正)>v(逆) |
| D.其他条件不变,若起始时向容器中充入2mol SO3,达平衡时吸收78.4kJ的热量 |
您最近一年使用:0次
2 . 回答下列问题:
(1)反应A(g)+B(g) C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
C(g) +D(g)过程中的能量变化如图所示,回答下列问题。______ 热反应(填“吸”、“放”)。
②在反应体系中加入催化剂,反应速率增大,E3_______ ,E2_______ (填“增大”、“减小”或“不变”)。
③当反应达到平衡时,升高温度,A的转化率_______ ( 填 “增大”、“减小”或“不变” )。
(2)一定条件下,一氧化碳与氢气反应可以合成甲醇。已知:
CH3OH(g)+1.5O2(g)=CO2(g)+2H2O(l) △H1=a kJ•mol﹣1
CO(g)+0.5O2(g)=CO2(g) △H2=b kJ•mol﹣1
H2(g)+0.5O2(g)=H2O(l) △H3=c kJ•mol﹣1
则CO(g)+2H2(g) CH3OH(g) △H=
CH3OH(g) △H=____________ kJ•mol﹣1 (用a、b、c表示)。
(3)一定压强下,在容积为2L的密闭容器中充入1mol CO与2mol H2,在催化剂作用下发生反应:CO(g)+2H2(g) CH3OH(g) △H,平衡转化率与温度、压强的关系如图所示。
CH3OH(g) △H,平衡转化率与温度、压强的关系如图所示。______ 0 (填“>”、“<”或“=”) ②p2_____ p1(填“>”、“<”或“=”);
(1)反应A(g)+B(g)
 C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
C(g) +D(g)过程中的能量变化如图所示,回答下列问题。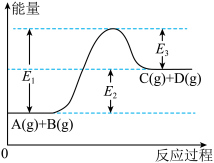
②在反应体系中加入催化剂,反应速率增大,E3
③当反应达到平衡时,升高温度,A的转化率
(2)一定条件下,一氧化碳与氢气反应可以合成甲醇。已知:
CH3OH(g)+1.5O2(g)=CO2(g)+2H2O(l) △H1=a kJ•mol﹣1
CO(g)+0.5O2(g)=CO2(g) △H2=b kJ•mol﹣1
H2(g)+0.5O2(g)=H2O(l) △H3=c kJ•mol﹣1
则CO(g)+2H2(g)
 CH3OH(g) △H=
CH3OH(g) △H=(3)一定压强下,在容积为2L的密闭容器中充入1mol CO与2mol H2,在催化剂作用下发生反应:CO(g)+2H2(g)
 CH3OH(g) △H,平衡转化率与温度、压强的关系如图所示。
CH3OH(g) △H,平衡转化率与温度、压强的关系如图所示。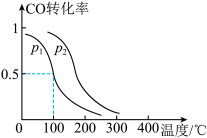
您最近一年使用:0次
3 . 回答下列问题:
(1)25℃时,CH3COOH的电离平衡常数为:K=1.8×10-5,H3PO3的电离平衡常数为:K1=8.3×10-3、K2=5.6×10-6;则:
①写出CH3COOH的电离方程式:___________
②25℃时,0.02mol/L的CH3COOH溶液的电离度约为______ %。
③往Na2HPO3溶液中滴加足量CH3COOH溶液的离子反应方程式为:____________
(2)①某课外活动小组为了探究BaSO4的溶解度,分别将足量BaSO4加入下列物质中:
a.5 mL水 b.40mL 0. 2 mol·L-1的Ba(OH)2溶液
c.20mL 0.5 mol·L-1的Na2SO4溶液 d.40mL 0.1 mol·L-1的H2SO4溶液中
溶解BaSO4后形成的溶液中,Ba2+的浓度由大到小的顺序为_____ (填字母)。
A.b>a>c>d B.b>a>d>c C.a>d>c>b D.a>b>d>c
②已知298K时,Ksp(BaSO4)=1.1×10-10,此时,溶液b中加入BaSO4固体后,c( )为
)为______________ mol·L-1。
(3)新型高效的乙烷燃料电池采用铂为电极材料,两电极上分别通入C2H6和O2 ,电解质溶液为KOH溶液。
①请写出乙烷燃料电池的负极反应式:_______________ 。
②利用此乙烷燃料电池给铅蓄电池充电,若充电过程中有3.0g乙烷完全反应,且不考虑能量损耗,则此充电过程消耗的O2在标况下的体积为_________ L(保留3位有效数字)、铅蓄电池的阳极质量减小________ g(保留3位有效数字)。
(1)25℃时,CH3COOH的电离平衡常数为:K=1.8×10-5,H3PO3的电离平衡常数为:K1=8.3×10-3、K2=5.6×10-6;则:
①写出CH3COOH的电离方程式:
②25℃时,0.02mol/L的CH3COOH溶液的电离度约为
③往Na2HPO3溶液中滴加足量CH3COOH溶液的离子反应方程式为:
(2)①某课外活动小组为了探究BaSO4的溶解度,分别将足量BaSO4加入下列物质中:
a.5 mL水 b.40mL 0. 2 mol·L-1的Ba(OH)2溶液
c.20mL 0.5 mol·L-1的Na2SO4溶液 d.40mL 0.1 mol·L-1的H2SO4溶液中
溶解BaSO4后形成的溶液中,Ba2+的浓度由大到小的顺序为
A.b>a>c>d B.b>a>d>c C.a>d>c>b D.a>b>d>c
②已知298K时,Ksp(BaSO4)=1.1×10-10,此时,溶液b中加入BaSO4固体后,c(
 )为
)为(3)新型高效的乙烷燃料电池采用铂为电极材料,两电极上分别通入C2H6和O2 ,电解质溶液为KOH溶液。
①请写出乙烷燃料电池的负极反应式:
②利用此乙烷燃料电池给铅蓄电池充电,若充电过程中有3.0g乙烷完全反应,且不考虑能量损耗,则此充电过程消耗的O2在标况下的体积为
您最近一年使用:0次
4 . 根据题意,完成下列填空:
(1)某温度时,测得0.1 mol·L-1的NaOH溶液的pH为13,则该温度下水的离子积常数KW=_______ 。
(2)浓度为0.1moL/L的二元弱酸H2S的水溶液中, H2S电离产生的离子有_______ 种(填数字),这几种离子中,浓度大小处于第二位的是_______ (填离子符号)。
(3)250C时,两种酸的电离平衡常数如下表所示。
①表中所列的二种酸中,酸性较弱的是_______ (写化学式)。
②向10mL0.1mol/L的H2R溶液中滴加10mL0.1mol/L的NaOH溶液充分反应后,混合溶液呈_______ 性(填酸性、碱性或中性),理由是(简略写出可做为判断理由的计算过程)______________ 。
(4)纯碱溶液呈碱性是因为它能与水发生水解反应,促进水的电离,但该溶液中由水电离产生的氢离子和氢氧根一定相等,请依此规律完善纯碱溶液中氢氧根浓度和其它相关粒子的相等关系式,即c(OH-)=_____________ 。
(1)某温度时,测得0.1 mol·L-1的NaOH溶液的pH为13,则该温度下水的离子积常数KW=
(2)浓度为0.1moL/L的二元弱酸H2S的水溶液中, H2S电离产生的离子有
(3)250C时,两种酸的电离平衡常数如下表所示。
| 化学式 | H2R | HClO |
| 电离平衡常数 | K1(H2R)=5×10-7,K2(H2R)=2×10-10 | 3.0×10-8 |
②向10mL0.1mol/L的H2R溶液中滴加10mL0.1mol/L的NaOH溶液充分反应后,混合溶液呈
(4)纯碱溶液呈碱性是因为它能与水发生水解反应,促进水的电离,但该溶液中由水电离产生的氢离子和氢氧根一定相等,请依此规律完善纯碱溶液中氢氧根浓度和其它相关粒子的相等关系式,即c(OH-)=
您最近一年使用:0次
5 . 根据能量不同能层又可分为不同的能级,分别用s、p、d、f等字母表示,以下能级符号正确的是
| A.1p | B.2d | C.3f | D.4s |
您最近一年使用:0次
6 . 每一种化学仪器都有它的用途,下列仪器可用来加热的是
| A.量筒 | B.试管 |
| C.滴定管 | D.胶头滴管 |
您最近一年使用:0次
7 . 黑木耳富含蛋白质、铁、具有还原性的维生素C等,每100 g黑木耳含铁量高达185 mg。
I.为了确定黑木耳中含有铁元素,甲同学设计实验方案如下。____________ 。
(2)步骤④检验Fe3+所用试剂是_____________ (填化学式)溶液。
(3)已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,则滤液A中大量含有的阳离子 的离子符号为____________ 。
II.紫色的KMnO4溶液在酸性条件下具有强氧化性,其还原产物是无色的Mn2+。本实验用KMnO4酸性溶液来测定黑木耳中铁元素的含量,乙同学设计实验方案如下。_______ (填序号)。
a.Na b.Cu c.Fe
(5)步骤⑥的离子方程式为_______________ 。
(6)若乙同学实验操作规范,但测得含铁量远远偏高,其可能的原因是_______________ 。
I.为了确定黑木耳中含有铁元素,甲同学设计实验方案如下。
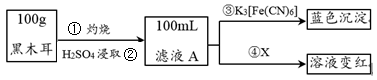
(2)步骤④检验Fe3+所用试剂是
(3)已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,则滤液A中大量含有的
II.紫色的KMnO4溶液在酸性条件下具有强氧化性,其还原产物是无色的Mn2+。本实验用KMnO4酸性溶液来测定黑木耳中铁元素的含量,乙同学设计实验方案如下。
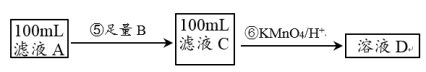
a.Na b.Cu c.Fe
(5)步骤⑥的离子方程式为
(6)若乙同学实验操作规范,但测得含铁量远远偏高,其可能的原因是
您最近一年使用:0次
8 . 下表列出了①~⑥六种元素在周期表中的位置:
按要求回答下列问题:
(1)元素②的最高正化合价是___________ 。
(2)元素⑤在周期表中的位置是___________ 。
(3)元素②和元素③的非金属性强弱关系是②___________ ③ (选填“>”或“<”);表中所列六种元素的单质,常温下为有色气体的是___________ (填化学式)。
(4)① ~⑥六种元素中原子半径最大的是___________ (填元素符号)。
(5)元素③与元素④能形成原子个数比为1:1的化合物 Y,Y 在常温下为_____ 色固态,常用与呼吸面具中做供氧剂。写出Y与水反应的化学方程式:___________ 。
| 族 周期 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ||||||
3 | ④ | ⑤ | ⑥ | |||||
(1)元素②的最高正化合价是
(2)元素⑤在周期表中的位置是
(3)元素②和元素③的非金属性强弱关系是②
(4)① ~⑥六种元素中原子半径最大的是
(5)元素③与元素④能形成原子个数比为1:1的化合物 Y,Y 在常温下为
您最近一年使用:0次
解题方法
9 . 回答下列问题。
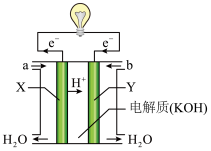
(1)如图为氢氧燃料电池的构造示意图。________ 口通入;电池工作时, 向
向________ 极移动。
②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质可以传导 ,则电池工作时负极电极反应式为
,则电池工作时负极电极反应式为________ 。
(2)银锌电池总反应为: 。则负极电极反应式:
。则负极电极反应式:________ 。正极电极反应式:________ 。
(3)铅酸蓄电池反应为 。用铅酸蓄电池电化学降解法处理酸性硝酸盐污水。
。用铅酸蓄电池电化学降解法处理酸性硝酸盐污水。
①铅酸蓄电池的负极材料________ (填“Pb”或“PbO2”)极。
②放电时负极电极反应式为:________ 。充电时的阳极反应式:________________ 。
(1)如图为氢氧燃料电池的构造示意图。
 向
向②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质可以传导
 ,则电池工作时负极电极反应式为
,则电池工作时负极电极反应式为(2)银锌电池总反应为:
 。则负极电极反应式:
。则负极电极反应式:(3)铅酸蓄电池反应为
 。用铅酸蓄电池电化学降解法处理酸性硝酸盐污水。
。用铅酸蓄电池电化学降解法处理酸性硝酸盐污水。①铅酸蓄电池的负极材料
②放电时负极电极反应式为:
您最近一年使用:0次
解题方法
10 . 燃煤会产生CO2、CO、SO2等大气污染物。燃煤脱硫的相关反应的热化学方程式如下:
Ⅰ.
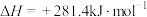
Ⅱ.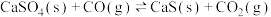
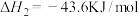
(1)一定温度下,向某恒容密闭容器中加入CaSO4(s)和1molCO,若只发生反应Ⅰ,下列能说明该反应已达到平衡状态的是________ (填字母)。
a.容器内的压强不发生变化 b.
c.容器内气体的密度不发生变化 d.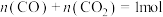
(2)一定温度下,体积为1L的容器中加入CaSO4(s)和1molCO,若只发生反应Ⅱ,测得CO2的物质的量随时间变化如图中曲线A所示:
________ 。
②曲线B表示过程与曲线A相比,改变的反应条件可能为________ (答出一条即可)。
③若要提高反应体系中CO2的体积分数,可采取的措施为________ 。
(3)以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.

Ⅱ.

Ⅲ.

回答下列问题:

________ kJmol-1。
Ⅰ.

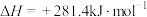
Ⅱ.
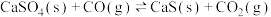
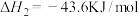
(1)一定温度下,向某恒容密闭容器中加入CaSO4(s)和1molCO,若只发生反应Ⅰ,下列能说明该反应已达到平衡状态的是
a.容器内的压强不发生变化 b.

c.容器内气体的密度不发生变化 d.
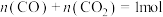
(2)一定温度下,体积为1L的容器中加入CaSO4(s)和1molCO,若只发生反应Ⅱ,测得CO2的物质的量随时间变化如图中曲线A所示:
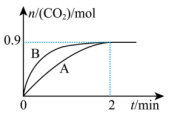

②曲线B表示过程与曲线A相比,改变的反应条件可能为
③若要提高反应体系中CO2的体积分数,可采取的措施为
(3)以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.


Ⅱ.


Ⅲ.


回答下列问题:

您最近一年使用:0次



