解题方法
1 . 下图是部分短周期元素原子半径与原子序数的关系图。下列说法正确的是
A. 两种元素只形成一种化合物 两种元素只形成一种化合物 |
B. 与 与 形成的化合物是共价化合物 形成的化合物是共价化合物 |
C.最高价氧化物对应的水化物的碱性: |
D. 元素气态氢化物的稳定性: 元素气态氢化物的稳定性: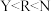 |
您最近半年使用:0次
名校
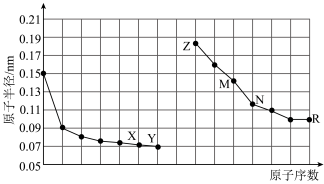
2 . 有7种短周期元素,原子半径及主要化合价如表,下列说法正确的是
元素代号 | X | Y | Z | M | W | Q | R |
原子半径/nm | 0.186 | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 | 0.032 |
主要化合价 | +1 | +3 | +6,-2 | +7,-1 | +5,-3 | -2 | +1 |
| A.Z在第三周期ⅣA族 |
B.离子半径: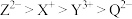 |
| C.Z、W、Q、R四种元素形成的化合物不可能是盐 |
| D.M元素的非金属性比Z强 |
您最近半年使用:0次
名校
3 . A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E的化合物焰色反应是黄色,F与G位置相邻,G是同周期元素中原子半径最小的元素。
请用化学用语回答:
(1)B的最高价氧化物的电子式是___________ 。
(2)用电子式表示E2F的形成过程___________ 。
(3)E、F、G三种元素所形成的简单离子,半径由大到小的顺序是___________ 。(用离子符号表示)
(4)下列实验操作对应的实验现象中,不正确的是___________ (填字母)。
(5)写出A与C形成的10电子分子中的化学键有___________ ,该物质的水溶液常用于检验输送G的单质的管道是否漏气,若漏气就会产生白烟,发生反应的化学方程式为___________ 。
请用化学用语回答:
(1)B的最高价氧化物的电子式是
(2)用电子式表示E2F的形成过程
(3)E、F、G三种元素所形成的简单离子,半径由大到小的顺序是
(4)下列实验操作对应的实验现象中,不正确的是
| 选项 | 实验操作 | 实验现象 |
| a | 将E单质投入到CuSO4溶液中 | 生成大量红色固体 |
| b | 向AlCl3溶液中通入过量C的气态氢化物 | 先生成白色沉淀,然后沉淀溶解 |
| c | 将G的单质通入到NaBr溶液中充分反应后,加入四氯化碳,振荡,静置 | 分两层,下层溶液变为橙红色 |
| d | 将B的最高价氧化物通入到Na2SiO3溶液中 | 生成白色沉淀 |
您最近半年使用:0次
名校
解题方法
4 . 现有部分元素的性质与原子(或分子)结构如下表(T、X、Y、Z都为前20号元素),请回答:
(1)画出元素T的二价阴离子的结构示意图______
(2)上述元素中,非金属性最强的元素在元素周期表中的位置______ ;表中T、X、Y元素的简单氢化物的稳定性由强到弱的顺序为______ (用化学式表示)。
(3)写出X单质与Z的最高价氧化物对应的水化物反应的化学方程式______
(4)镓(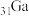 )的化合物砷化镓(GaAs)具有耐高温、耐高电压等特性,可作为第三代半导体材料。废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出
)的化合物砷化镓(GaAs)具有耐高温、耐高电压等特性,可作为第三代半导体材料。废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出 气体,同时生成
气体,同时生成 和
和 。写出该反应的化学方程式
。写出该反应的化学方程式______ 。
元素编号 | 元素性质与原子(或分子)结构 |
T | 其二价阴离子核外电子数为18 |
X | 第三周期非金属性最强的元素 |
Y | L层比K层多5个电子 |
Z | 位于第4周期,内层电子数是最外层电子数的9倍 |
(2)上述元素中,非金属性最强的元素在元素周期表中的位置
(3)写出X单质与Z的最高价氧化物对应的水化物反应的化学方程式
(4)镓(
 )的化合物砷化镓(GaAs)具有耐高温、耐高电压等特性,可作为第三代半导体材料。废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出
)的化合物砷化镓(GaAs)具有耐高温、耐高电压等特性,可作为第三代半导体材料。废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出 气体,同时生成
气体,同时生成 和
和 。写出该反应的化学方程式
。写出该反应的化学方程式
您最近半年使用:0次
名校
5 . 短周期元素W、X、Y、Z的原子序数依次增大,X与W、Z相邻,且X、Z同主族,W、X、Y、Z的最外层电子数之和为18,Y的金属性是短周期元素中最强的。下列说法正确的是
A.简单离子半径: | B.简单氢化物的还原性: |
| C.Y、Z形成的化合物中有共价键 | D.W的氧化物的水化物均为强酸 |
您最近半年使用:0次
7日内更新
|
170次组卷
|
2卷引用:四川省绵阳南山中学2024届高三下学期三诊热身考试理综-化学试题
名校
解题方法
6 . 六种短周期主族元素的原子半径和主要化合价如图所示。已知: 、
、 的简单阳离子都是10电子粒子。回答下列问题:
的简单阳离子都是10电子粒子。回答下列问题: 位于第
位于第___________ 周期___________ 族。
(2) 的简单阳离子的结构示意图为
的简单阳离子的结构示意图为___________ 。
(3)上述元素的最高价氧化物对应水化物中,碱性最强的是___________ (填化学式,下同),酸性最强的是___________ 。
(4)在 、
、 、
、 的简单氢化物中,最稳定的是
的简单氢化物中,最稳定的是___________ (填结构式)
(5) 、
、 、
、 三种元素组成一种具有强还原性的化合物,它在水溶液中与过量的
三种元素组成一种具有强还原性的化合物,它在水溶液中与过量的 单质反应的离子方程式为
单质反应的离子方程式为___________ 。
(6)设计简单实验证明 的金属性比
的金属性比 的强:
的强:___________ 。
 、
、 的简单阳离子都是10电子粒子。回答下列问题:
的简单阳离子都是10电子粒子。回答下列问题: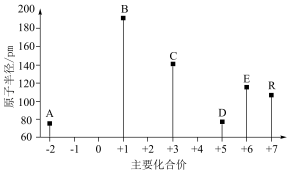
 位于第
位于第(2)
 的简单阳离子的结构示意图为
的简单阳离子的结构示意图为(3)上述元素的最高价氧化物对应水化物中,碱性最强的是
(4)在
 、
、 、
、 的简单氢化物中,最稳定的是
的简单氢化物中,最稳定的是(5)
 、
、 、
、 三种元素组成一种具有强还原性的化合物,它在水溶液中与过量的
三种元素组成一种具有强还原性的化合物,它在水溶液中与过量的 单质反应的离子方程式为
单质反应的离子方程式为(6)设计简单实验证明
 的金属性比
的金属性比 的强:
的强:
您最近半年使用:0次
7 . 根据表中短周期元素的有关信息判断,下列说法错误的是
元素编号 | E | F | G | H | I | J | K | L |
原子半径/nm | 0.037 | 0.074 | 0.082 | 0.099 | 0.102 | 0.143 | 0.160 | 0.186 |
| 最高化合价或最低化合价 |
|
|
|
|
|
|
|
|
| A.电负性大小:F>H>I |
| B.简单离子半径:K>F>L |
| C.第一电离能:K>J>L |
| D.L、K、J的最高价氧化物对应水化物碱性逐渐减弱 |
您最近半年使用:0次
名校
8 . 下表是部分前18号元素的原子半径及主要化合价。下列说法正确的是
| 元素 |  |  |  |  |  |  |
| 原子半径(nm) |  |  |  | 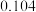 | 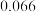 | 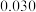 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 | +1 |
| A.从化合价看出,在周期表中位于同一周期的元素为U、L、M、R |
| B.T和U形成的两种化合物中,阴、阳离子个数比相同 |
| C.M与T、U元素组成的化合物既能与强酸反应又能与强碱反应 |
| D.L的最高价氧化物的水化物是强碱 |
您最近半年使用:0次
名校
9 . 如图是部分短周期元素原子半径与原子序数的关系图。下列说法正确的是
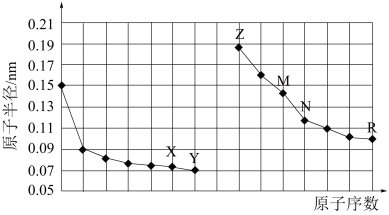

A.最高正化合价: |
B.最高价氧化物对应水化物的碱性, |
C.N的氧化物既可以和盐酸反应,也可以和 溶液反应 溶液反应 |
D.简单离子半径: |
您最近半年使用:0次
名校
解题方法
10 . 现有a、b、c、d、e、f、g七种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列信息,回答有关问题:
(1)常温下,气态 分子其系统命名为
分子其系统命名为_______ 。
(2)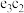 的电子式为
的电子式为_______ (用元素符号表示)。
(3)d元素的原子核外共有_______ 种不同空间运动状态的电子。
(4)已知A: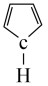 和B:
和B: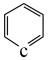 中所有原子均共面(c为题干中c元素),A物质中c原子的杂化类型为
中所有原子均共面(c为题干中c元素),A物质中c原子的杂化类型为_______ ,其中c原子较易形成配位键的是_______ (填“A或B”)。
(5)d、e、f三种元素的简单离子半径由大到小的顺序是_______ (用离子符号表示)。
(6)其中五种元素形成的一种1:1型离子化合物中,阴离子呈正四面体结构,则其阴离子化学式为_______ ;阳离子中含有的中性分子结构部分如图所示,阳离子中存在的化学键类型有_______ (填序号)。
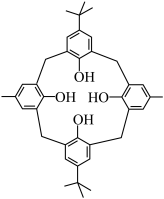
A.共价键 B.配位键 C.离子键 D.金属键
| a元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| b形成化合物种类最多的元素 |
| c元素基态原子的核外p电子数比s电子数少1 |
| d元素基态原子的核外p轨道中有两个未成对电子 |
e元素的气态基态原子的第一至第四电离能分别是: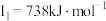  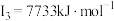 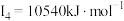 |
| f元素的主族序数比周期数大3 |
| g元素位于元素周期表中的第11列 |
(1)常温下,气态
 分子其系统命名为
分子其系统命名为(2)
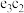 的电子式为
的电子式为(3)d元素的原子核外共有
(4)已知A:
 和B:
和B: 中所有原子均共面(c为题干中c元素),A物质中c原子的杂化类型为
中所有原子均共面(c为题干中c元素),A物质中c原子的杂化类型为(5)d、e、f三种元素的简单离子半径由大到小的顺序是
(6)其中五种元素形成的一种1:1型离子化合物中,阴离子呈正四面体结构,则其阴离子化学式为

A.共价键 B.配位键 C.离子键 D.金属键
您最近半年使用:0次








