1 . 下列实验操作正确且能达到实验目的的是
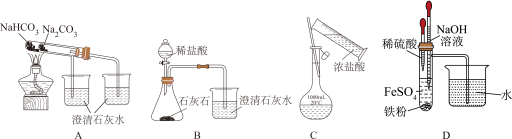
| A.验证碳酸钠和碳酸氢钠的稳定性 |
B.用装置比较 、C元素的非金属性 、C元素的非金属性 |
| C.用装置配制一定物质的量浓度的稀盐酸 |
| D.制备氢氧化亚铁并能较长时间看见白色沉淀 |
您最近一年使用:0次
解题方法
2 . 在一定的温度和压强下,将按一定比例混合的 和
和 通过装有催化剂的反应器可得到甲烷。
通过装有催化剂的反应器可得到甲烷。
已知: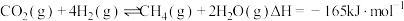 ;
;
 。
。
催化剂选择是 甲烷化技术的核心。在两种不同催化剂作用下反应相同时间,测
甲烷化技术的核心。在两种不同催化剂作用下反应相同时间,测 转化率和生成
转化率和生成 选择性随温度变化的影响如下图所示:
选择性随温度变化的影响如下图所示: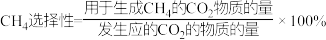 。下列有关说法正确的是
。下列有关说法正确的是
 和
和 通过装有催化剂的反应器可得到甲烷。
通过装有催化剂的反应器可得到甲烷。已知:
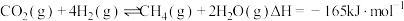 ;
; 。
。催化剂选择是
 甲烷化技术的核心。在两种不同催化剂作用下反应相同时间,测
甲烷化技术的核心。在两种不同催化剂作用下反应相同时间,测 转化率和生成
转化率和生成 选择性随温度变化的影响如下图所示:
选择性随温度变化的影响如下图所示: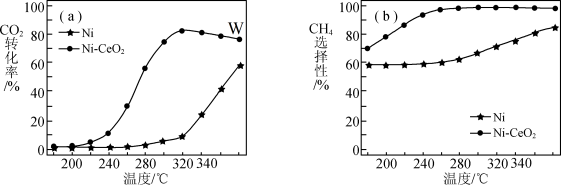
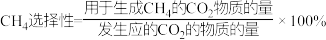 。下列有关说法正确的是
。下列有关说法正确的是A.反应 在高温下有自发进行的倾向 在高温下有自发进行的倾向 |
B.在 间,以 间,以 为催化剂,升高温度 为催化剂,升高温度 的选择性明显增大 的选择性明显增大 |
C.高于 后,以 后,以 为催化剂, 为催化剂, 转化率上升的原因是平衡正向移动 转化率上升的原因是平衡正向移动 |
D.选择合适的催化剂、合适的温度有利于提高 的选择性 的选择性 |
您最近一年使用:0次
解题方法
3 . 优氯净[化学式为 ,常温下为白色固体,在冷水中溶解度较小]是一种高效杀菌剂。实验室利用
,常温下为白色固体,在冷水中溶解度较小]是一种高效杀菌剂。实验室利用 溶液和氰尿酸固体[化学式为
溶液和氰尿酸固体[化学式为 ,弱酸,微溶于水,溶于强碱溶液]制备优氯净,实验装置如下图所示(部分夹持装置略):
,弱酸,微溶于水,溶于强碱溶液]制备优氯净,实验装置如下图所示(部分夹持装置略): 中会生成
中会生成 和
和 。
。
② 。
。
回答下列问题:
(1)仪器 的名称为
的名称为_______ ,装置 的作用为
的作用为_______ 。
(2)除了用装置 制取氯气,还可以用
制取氯气,还可以用 和浓盐酸在常温下反应生成
和浓盐酸在常温下反应生成 和两种盐,写出该反应的化学方程式:
和两种盐,写出该反应的化学方程式:_______ 。
(3)装置D的作用是_______ 。
(4)装置C进行控温水浴的目的是_____ ,若温度过高C中发生反应的化学方程式为____ 。
(5)通过下列实验,可以测定优氯净样品中有效氯的含量(样品中有效氯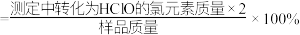 )。
)。
反应原理: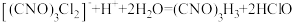 ;
;
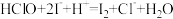 ;
;
 。
。
实验步骤:准确称取 样品,用容量瓶配成
样品,用容量瓶配成 溶液;取
溶液;取 上述溶液于锥形瓶中,加入适量稀硫酸和过量
上述溶液于锥形瓶中,加入适量稀硫酸和过量 溶液,充分反应。生成的
溶液,充分反应。生成的 恰好消耗
恰好消耗 标准溶液。
标准溶液。
则该样品中有效氯的百分含量为_______  (保留三位有效数字)。
(保留三位有效数字)。
 ,常温下为白色固体,在冷水中溶解度较小]是一种高效杀菌剂。实验室利用
,常温下为白色固体,在冷水中溶解度较小]是一种高效杀菌剂。实验室利用 溶液和氰尿酸固体[化学式为
溶液和氰尿酸固体[化学式为 ,弱酸,微溶于水,溶于强碱溶液]制备优氯净,实验装置如下图所示(部分夹持装置略):
,弱酸,微溶于水,溶于强碱溶液]制备优氯净,实验装置如下图所示(部分夹持装置略):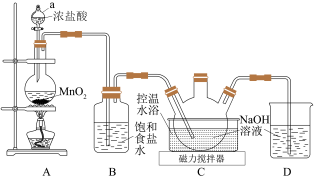
 中会生成
中会生成 和
和 。
。②
 。
。回答下列问题:
(1)仪器
 的名称为
的名称为 的作用为
的作用为(2)除了用装置
 制取氯气,还可以用
制取氯气,还可以用 和浓盐酸在常温下反应生成
和浓盐酸在常温下反应生成 和两种盐,写出该反应的化学方程式:
和两种盐,写出该反应的化学方程式:(3)装置D的作用是
(4)装置C进行控温水浴的目的是
(5)通过下列实验,可以测定优氯净样品中有效氯的含量(样品中有效氯
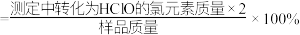 )。
)。反应原理:
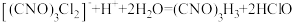 ;
;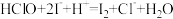 ;
; 。
。实验步骤:准确称取
 样品,用容量瓶配成
样品,用容量瓶配成 溶液;取
溶液;取 上述溶液于锥形瓶中,加入适量稀硫酸和过量
上述溶液于锥形瓶中,加入适量稀硫酸和过量 溶液,充分反应。生成的
溶液,充分反应。生成的 恰好消耗
恰好消耗 标准溶液。
标准溶液。则该样品中有效氯的百分含量为
 (保留三位有效数字)。
(保留三位有效数字)。
您最近一年使用:0次
解题方法
4 . 从砷化镓废料(主要成分为 、含
、含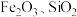 和
和 等杂质)中回收镓和砷的工艺流程如图所示:
等杂质)中回收镓和砷的工艺流程如图所示: 是两性氢氧化物。
是两性氢氧化物。 时,
时, 的溶度积
的溶度积 ,电离常数
,电离常数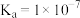 。
。
回答下列问题:
(1)“浆化”过程将砷化镓废料转变为悬浊液,目的是_______ 。
(2)“碱浸1”过程,砷化镓转化为 和
和 ,该反应的离子方程式:
,该反应的离子方程式:_______ 。
(3)为提高镓的回收率,加硫酸调 的最大值是
的最大值是_______ (溶液中含镓元素的微粒的浓度不大于 时,认为该微粒沉淀完全)。
时,认为该微粒沉淀完全)。
(4)“电解”是指用传统的方法将 溶解到
溶解到 溶液中,电解得到金属镓。电解时,
溶液中,电解得到金属镓。电解时,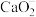 在阴极放电的电极反应式:
在阴极放电的电极反应式:_______ 。
(5)向“调 ”后得到的滤液中加入足量
”后得到的滤液中加入足量 溶液,使
溶液,使 大于12,经
大于12,经____ 、降温结晶、过滤、洗涤、____ 后得到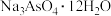 。
。
(6)某同学为了探究可逆反应: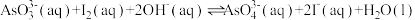 设计如图1所示装置。实验操作及现象:按图1装置加入试剂并连接装置,电流由
设计如图1所示装置。实验操作及现象:按图1装置加入试剂并连接装置,电流由 流向
流向 。当不产生电流时,向图1装置左边烧杯中加入一定量
。当不产生电流时,向图1装置左边烧杯中加入一定量 盐酸,发现又产生电流,实验中电流与时间的关系如图2所示:
盐酸,发现又产生电流,实验中电流与时间的关系如图2所示:_______ 。
a.实验开始时,电子由 经盐桥流向
经盐桥流向
b.图2中, 点时反应达到化学平衡状态
点时反应达到化学平衡状态
c.向左边烧杯中加入盐酸后,平衡逆向移动
d.若将所加的盐酸换成氢氧化钠溶液,平衡逆向移动,电流增大
 、含
、含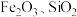 和
和 等杂质)中回收镓和砷的工艺流程如图所示:
等杂质)中回收镓和砷的工艺流程如图所示: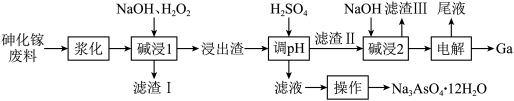
 是两性氢氧化物。
是两性氢氧化物。 时,
时, 的溶度积
的溶度积 ,电离常数
,电离常数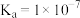 。
。回答下列问题:
(1)“浆化”过程将砷化镓废料转变为悬浊液,目的是
(2)“碱浸1”过程,砷化镓转化为
 和
和 ,该反应的离子方程式:
,该反应的离子方程式:(3)为提高镓的回收率,加硫酸调
 的最大值是
的最大值是 时,认为该微粒沉淀完全)。
时,认为该微粒沉淀完全)。(4)“电解”是指用传统的方法将
 溶解到
溶解到 溶液中,电解得到金属镓。电解时,
溶液中,电解得到金属镓。电解时,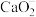 在阴极放电的电极反应式:
在阴极放电的电极反应式:(5)向“调
 ”后得到的滤液中加入足量
”后得到的滤液中加入足量 溶液,使
溶液,使 大于12,经
大于12,经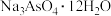 。
。(6)某同学为了探究可逆反应:
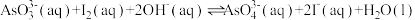 设计如图1所示装置。实验操作及现象:按图1装置加入试剂并连接装置,电流由
设计如图1所示装置。实验操作及现象:按图1装置加入试剂并连接装置,电流由 流向
流向 。当不产生电流时,向图1装置左边烧杯中加入一定量
。当不产生电流时,向图1装置左边烧杯中加入一定量 盐酸,发现又产生电流,实验中电流与时间的关系如图2所示:
盐酸,发现又产生电流,实验中电流与时间的关系如图2所示: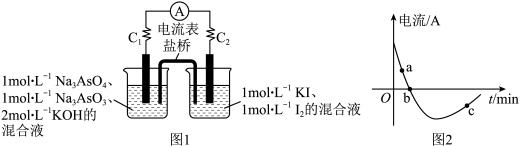
a.实验开始时,电子由
 经盐桥流向
经盐桥流向
b.图2中,
 点时反应达到化学平衡状态
点时反应达到化学平衡状态c.向左边烧杯中加入盐酸后,平衡逆向移动
d.若将所加的盐酸换成氢氧化钠溶液,平衡逆向移动,电流增大
您最近一年使用:0次
5 . 锌是一种应用广泛的金属,工业上以菱锌矿(主要成分是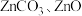 ,含少量
,含少量 和
和 )制备锌单质的流程如下:
)制备锌单质的流程如下: 是两性氢氧化物。下列说法错误的是
是两性氢氧化物。下列说法错误的是
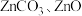 ,含少量
,含少量 和
和 )制备锌单质的流程如下:
)制备锌单质的流程如下: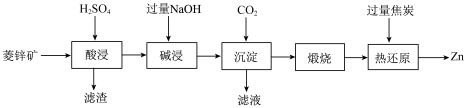
 是两性氢氧化物。下列说法错误的是
是两性氢氧化物。下列说法错误的是| A.硫酸根离子的VSEPR模型为正四面体 |
| B.“酸浸”过程中加入食盐可增加滤渣的量 |
C.“沉淀”过程中,消耗 与 与 的物质的量之比为 的物质的量之比为 |
D.“热还原”过程中,发生主要反应的化学方程式为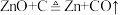 |
您最近一年使用:0次
6 . 消毒剂在生产生活中有重要应用,氯气可以制备多种含氯消毒剂,常见的含氯消毒剂有:次氯酸、漂白粉、漂白液、 等。
等。
(1)图是实验室制取氯气后进行性质实验的一部分,将氯气依次通过盛有干燥有色布条的广口瓶和盛有湿润有色布条的广口瓶。为防止氯气尾气污染空气,可用_____ 溶液吸收多余的氯气,发生反应的离子方程式为_____ 。 工业上将氯气通入石灰乳
工业上将氯气通入石灰乳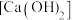 制取漂白粉,漂白粉溶于水后,受空气中的
制取漂白粉,漂白粉溶于水后,受空气中的 作用,产生有漂白、杀菌作用的次氯酸,产生次氯酸的化学方程式为
作用,产生有漂白、杀菌作用的次氯酸,产生次氯酸的化学方程式为_____ 。
 长期露置于空气中的漂白粉,加稀盐酸后产生的气体是
长期露置于空气中的漂白粉,加稀盐酸后产生的气体是_____ (填字母) 。
。
A .
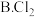

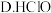
③ 是一种强氧化剂,其水溶液也是一种广谱杀菌剂,可用“有效氯含量”来衡量其消毒能力,“有效氯含量”定义是:每克含氯消毒剂的氧化能力相当于多少克
是一种强氧化剂,其水溶液也是一种广谱杀菌剂,可用“有效氯含量”来衡量其消毒能力,“有效氯含量”定义是:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。
的氧化能力。 的有效氯含量为
的有效氯含量为_____  。(计算结果保留两位小数)
。(计算结果保留两位小数)
 等。
等。(1)图是实验室制取氯气后进行性质实验的一部分,将氯气依次通过盛有干燥有色布条的广口瓶和盛有湿润有色布条的广口瓶。为防止氯气尾气污染空气,可用
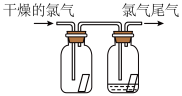
 工业上将氯气通入石灰乳
工业上将氯气通入石灰乳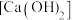 制取漂白粉,漂白粉溶于水后,受空气中的
制取漂白粉,漂白粉溶于水后,受空气中的 作用,产生有漂白、杀菌作用的次氯酸,产生次氯酸的化学方程式为
作用,产生有漂白、杀菌作用的次氯酸,产生次氯酸的化学方程式为 长期露置于空气中的漂白粉,加稀盐酸后产生的气体是
长期露置于空气中的漂白粉,加稀盐酸后产生的气体是 。
。A .

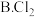

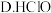
③
 是一种强氧化剂,其水溶液也是一种广谱杀菌剂,可用“有效氯含量”来衡量其消毒能力,“有效氯含量”定义是:每克含氯消毒剂的氧化能力相当于多少克
是一种强氧化剂,其水溶液也是一种广谱杀菌剂,可用“有效氯含量”来衡量其消毒能力,“有效氯含量”定义是:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。
的氧化能力。 的有效氯含量为
的有效氯含量为 。(计算结果保留两位小数)
。(计算结果保留两位小数)
您最近一年使用:0次
7 . 实验室需用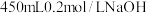 溶液,请同学们结合配制过程回答下列问题:
溶液,请同学们结合配制过程回答下列问题:___________ 。
 温度
温度  浓度
浓度  容量
容量  压强
压强  刻度线
刻度线  酸(碱)式
酸(碱)式
(2)配制过程中不需要使用的化学仪器有___________ (填字母)。
A.烧杯 B. 容量瓶 C.漏斗 D.胶头滴管 E.玻璃棒
容量瓶 C.漏斗 D.胶头滴管 E.玻璃棒
(3)用托盘天平称取氢氧化钠,其质量为___________  。
。
(4)如果实验过程中定容时俯视,会使配制出的 溶液浓度
溶液浓度___________ (填“偏高”、“偏低”或“不变”)。
(5)实验室也可以通过稀释浓溶液进行配制,现用密度为1.4g/cm3质量分数为40%的浓 溶液来配制450mL1mol/L的稀
溶液来配制450mL1mol/L的稀 溶液,请根据计算结果,量取浓氢氧化钠溶液体积的量筒规格为___________。
溶液,请根据计算结果,量取浓氢氧化钠溶液体积的量筒规格为___________。
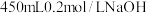 溶液,请同学们结合配制过程回答下列问题:
溶液,请同学们结合配制过程回答下列问题:
 温度
温度  浓度
浓度  容量
容量  压强
压强  刻度线
刻度线  酸(碱)式
酸(碱)式(2)配制过程中不需要使用的化学仪器有
A.烧杯 B.
 容量瓶 C.漏斗 D.胶头滴管 E.玻璃棒
容量瓶 C.漏斗 D.胶头滴管 E.玻璃棒(3)用托盘天平称取氢氧化钠,其质量为
 。
。(4)如果实验过程中定容时俯视,会使配制出的
 溶液浓度
溶液浓度(5)实验室也可以通过稀释浓溶液进行配制,现用密度为1.4g/cm3质量分数为40%的浓
 溶液来配制450mL1mol/L的稀
溶液来配制450mL1mol/L的稀 溶液,请根据计算结果,量取浓氢氧化钠溶液体积的量筒规格为___________。
溶液,请根据计算结果,量取浓氢氧化钠溶液体积的量筒规格为___________。| A.10mL | B.25mL | C.50mL | D.100mL |
您最近一年使用:0次
8 . 已知 、
、 、
、 、
、 、
、 、
、 、
、 为中学化学中常见的化合物,其中
为中学化学中常见的化合物,其中 是淡黄色固体,
是淡黄色固体, 是无色液体,
是无色液体, 为红褐色固体。常温下甲、乙、丙为单质气体,丙呈黄绿色;丁、戊为常见金属单质,其中戊是当前用量最大的金属。它们之间的转化关系如图所示
为红褐色固体。常温下甲、乙、丙为单质气体,丙呈黄绿色;丁、戊为常见金属单质,其中戊是当前用量最大的金属。它们之间的转化关系如图所示 有的反应部分产物已经略去
有的反应部分产物已经略去 。回答下列问题:
。回答下列问题:_____ 氢氧化物(填酸性、碱性或两性),写出 的化学式:
的化学式:_____ 。
(2)写出反应②的离子方程式:_____ 。
(3)检验 中阳离子常用的试剂是(若需要多种试剂,请按使用的先后顺序填写):
中阳离子常用的试剂是(若需要多种试剂,请按使用的先后顺序填写):_____ 。
(4)写出F转化成G的化学方程式:_____ 。
 、
、 、
、 、
、 、
、 、
、 、
、 为中学化学中常见的化合物,其中
为中学化学中常见的化合物,其中 是淡黄色固体,
是淡黄色固体, 是无色液体,
是无色液体, 为红褐色固体。常温下甲、乙、丙为单质气体,丙呈黄绿色;丁、戊为常见金属单质,其中戊是当前用量最大的金属。它们之间的转化关系如图所示
为红褐色固体。常温下甲、乙、丙为单质气体,丙呈黄绿色;丁、戊为常见金属单质,其中戊是当前用量最大的金属。它们之间的转化关系如图所示 有的反应部分产物已经略去
有的反应部分产物已经略去 。回答下列问题:
。回答下列问题: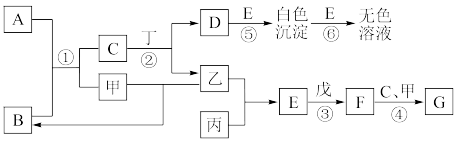
 的化学式:
的化学式:(2)写出反应②的离子方程式:
(3)检验
 中阳离子常用的试剂是(若需要多种试剂,请按使用的先后顺序填写):
中阳离子常用的试剂是(若需要多种试剂,请按使用的先后顺序填写):(4)写出F转化成G的化学方程式:
您最近一年使用:0次
9 . 下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回答问题:
(1)①的元素符号是_____ ;④在元素周期表中的位置是_____ ;
(2)②和⑤两种元素的非金属性强弱关系是②_____ ⑤(填“>”“<”或“=”);
(3)③和⑤形成的化合物中含有的化学键是_____ (填“离子键”或“共价键”);
(4)④和⑤的最高价氧化物对应的水化物反应的离子方程式为_____ 。
| IA | 0 | ||||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |||
| 2 | ① | ② | |||||||
| 3 | ③ | ④ | ⑤ | Ar |
(2)②和⑤两种元素的非金属性强弱关系是②
(3)③和⑤形成的化合物中含有的化学键是
(4)④和⑤的最高价氧化物对应的水化物反应的离子方程式为
您最近一年使用:0次
10 . 物质的用途与其性质密切相关,现有下列五种物质:A.14C B.FeCl3 C.Fe2O3 D.MnO2 E.Na2CO3,请根据题意选择恰当的选项用字母填空。
(1)可作为“腐蚀液”的溶质,将覆铜板上不需要的铜腐蚀的是_____ ;
(2)常用作油漆、涂料、油墨和橡胶的红色颜料的是_____ ;
(3)属于软锰矿主要成分的是_____ ;
(4)可用于考古,测定文物年代的是_____ ;
(5)俗名纯碱,可以用作食用碱或工业用碱的是_____ ;
(1)可作为“腐蚀液”的溶质,将覆铜板上不需要的铜腐蚀的是
(2)常用作油漆、涂料、油墨和橡胶的红色颜料的是
(3)属于软锰矿主要成分的是
(4)可用于考古,测定文物年代的是
(5)俗名纯碱,可以用作食用碱或工业用碱的是
您最近一年使用:0次



