名校
1 . 根据所学知识,回答下列问题。
(1)已知反应: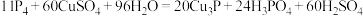 在该反应中,氧化剂是
在该反应中,氧化剂是_______ (填化学式),被氧化的元素是_______ (填元素符号)。
(2)下列状态的物质,既属于电解质又能导电的是_______。(填标号)
(3) 是人体必需的微量元素,其中
是人体必需的微量元素,其中 的中子数是
的中子数是_______ ,其氢化物 的结构式为
的结构式为_______ 。
(4)写出炽热的碳与浓硫酸反应的化学方程式_______ 。
(5)已知反应: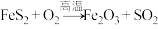 (未配平),若生成标准状况下
(未配平),若生成标准状况下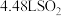 ,则转移的电子数为
,则转移的电子数为_______ 。
(6)往碘化钾溶液中通入少量 ,所发生的离子方程式
,所发生的离子方程式_______ 。
(1)已知反应:
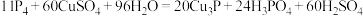 在该反应中,氧化剂是
在该反应中,氧化剂是(2)下列状态的物质,既属于电解质又能导电的是_______。(填标号)
| A.氯化镁晶体 | B.氯化钠溶液 | C.液态氯化氢 | D.熔融氢氧化钾 |
 是人体必需的微量元素,其中
是人体必需的微量元素,其中 的中子数是
的中子数是 的结构式为
的结构式为(4)写出炽热的碳与浓硫酸反应的化学方程式
(5)已知反应:
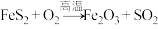 (未配平),若生成标准状况下
(未配平),若生成标准状况下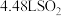 ,则转移的电子数为
,则转移的电子数为(6)往碘化钾溶液中通入少量
 ,所发生的离子方程式
,所发生的离子方程式
您最近一年使用:0次
2 . 铁与空气接触时会形成氧化物,如一块低碳钢可以被三种氧化物膜所覆盖与金属接触的一侧是FeO,与空气接触的一侧是 ,而中间则是
,而中间则是 。
。
(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的___________ (填化学式)。
(2) 的一种用途是
的一种用途是___________ 。(填“用作油漆、涂料 ”或“磁电机”);
(3)FeO可作化妆品中的色素,它还能进行一系列转化: 。
。
① 时应加入的试剂是
时应加入的试剂是___________ (填“H2SO4”或“Na2SO4”)。
②“速力菲”(主要有效成分是 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入___________ (填“KSCN”或“K2SO4”),若出现___________ (填“红色”或“浅绿色”)现象,则证明该药物已变质。
③在 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成___________ (填“红褐色”或“黄色”),其中沉淀颜色发生变化的化学方程式为___________ 。
 ,而中间则是
,而中间则是 。
。(1)中国古代“四大发明”之一最早的指南针“司南”,其具有磁性作用是因为主要含有上述物质中的
(2)
 的一种用途是
的一种用途是(3)FeO可作化妆品中的色素,它还能进行一系列转化:
 。
。①
 时应加入的试剂是
时应加入的试剂是②“速力菲”(主要有效成分是
 )是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入
)是一种常见的补铁药物,欲验证该药物超过保质期后已变质,具体操作为:首先除去药物表面包装的糖衣,再将药物粉碎、加水溶解静置、取少许溶液于试管中,向其中加入③在
 中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
中滴加NaOH溶液的实验现象是先产生白色絮状沉淀,然后迅速变成灰绿色,最终变成
您最近一年使用:0次
3 . 钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在_______ 中。
(2)除去碳酸钠固体中碳酸氢钠的方法是______________ 。
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入_______ (填“铁粉”或“铜粉”)。
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:_______________ 。
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于__________ (填“碱性”或“两性”)氧化物。
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在
(2)除去碳酸钠固体中碳酸氢钠的方法是
(3)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入
(4)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的离子方程式:
(5)铝制餐具不宜用来蒸煮或长时间存放酸性或碱性食物,是因为Al和Al2O3均能与酸、碱反应。则Al2O3属于
您最近一年使用:0次
4 . 回答下列问题:
(1)反应A(g)+B(g) C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
C(g) +D(g)过程中的能量变化如图所示,回答下列问题。______ 热反应(填“吸”、“放”)。
②在反应体系中加入催化剂,反应速率增大,E3_______ ,E2_______ (填“增大”、“减小”或“不变”)。
③当反应达到平衡时,升高温度,A的转化率_______ ( 填 “增大”、“减小”或“不变” )。
(2)一定条件下,一氧化碳与氢气反应可以合成甲醇。已知:
CH3OH(g)+1.5O2(g)=CO2(g)+2H2O(l) △H1=a kJ•mol﹣1
CO(g)+0.5O2(g)=CO2(g) △H2=b kJ•mol﹣1
H2(g)+0.5O2(g)=H2O(l) △H3=c kJ•mol﹣1
则CO(g)+2H2(g) CH3OH(g) △H=
CH3OH(g) △H=____________ kJ•mol﹣1 (用a、b、c表示)。
(3)一定压强下,在容积为2L的密闭容器中充入1mol CO与2mol H2,在催化剂作用下发生反应:CO(g)+2H2(g) CH3OH(g) △H,平衡转化率与温度、压强的关系如图所示。
CH3OH(g) △H,平衡转化率与温度、压强的关系如图所示。______ 0 (填“>”、“<”或“=”) ②p2_____ p1(填“>”、“<”或“=”);
(1)反应A(g)+B(g)
 C(g) +D(g)过程中的能量变化如图所示,回答下列问题。
C(g) +D(g)过程中的能量变化如图所示,回答下列问题。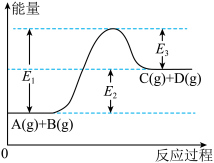
②在反应体系中加入催化剂,反应速率增大,E3
③当反应达到平衡时,升高温度,A的转化率
(2)一定条件下,一氧化碳与氢气反应可以合成甲醇。已知:
CH3OH(g)+1.5O2(g)=CO2(g)+2H2O(l) △H1=a kJ•mol﹣1
CO(g)+0.5O2(g)=CO2(g) △H2=b kJ•mol﹣1
H2(g)+0.5O2(g)=H2O(l) △H3=c kJ•mol﹣1
则CO(g)+2H2(g)
 CH3OH(g) △H=
CH3OH(g) △H=(3)一定压强下,在容积为2L的密闭容器中充入1mol CO与2mol H2,在催化剂作用下发生反应:CO(g)+2H2(g)
 CH3OH(g) △H,平衡转化率与温度、压强的关系如图所示。
CH3OH(g) △H,平衡转化率与温度、压强的关系如图所示。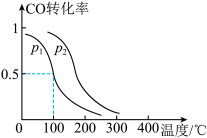
您最近一年使用:0次
解题方法
5 . 生活离不开化学,生活中有许多中学化学常见的物质,它们的主要成分如下表:
回答下列问题:
(1) 中所含化学键类型为
中所含化学键类型为___________ (填“离子键”或“共价键”)。
(2)明矾可用来制备氢氧化铝,请选择与之反应的最佳试剂:___________ (填“氨水”或“氢氧化钠溶液”)。
(3) 的电离方程式为
的电离方程式为___________ 。
(4) 溶液中混有少量
溶液中混有少量 ,可加适量的
,可加适量的 溶液除杂,离子方程式为
溶液除杂,离子方程式为___________ , 固体中若含有少量
固体中若含有少量 固体,可采取的除杂方法为
固体,可采取的除杂方法为___________ 。
(5)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:___________ 。
(6) 属于
属于___________ 电解质(填“强”、“弱”或“非”)。
| 商品 | 食盐 | 明矾 | 84消毒液 |
| 主要成分 | ① | ② | ③ |
| 商品 | 发酵粉 | 白醋 | 洁厕灵 |
| 主要成分 | ④ | ⑤ | ⑥ |
(1)
 中所含化学键类型为
中所含化学键类型为(2)明矾可用来制备氢氧化铝,请选择与之反应的最佳试剂:
(3)
 的电离方程式为
的电离方程式为(4)
 溶液中混有少量
溶液中混有少量 ,可加适量的
,可加适量的 溶液除杂,离子方程式为
溶液除杂,离子方程式为 固体中若含有少量
固体中若含有少量 固体,可采取的除杂方法为
固体,可采取的除杂方法为(5)84消毒液和洁厕灵不能混合使用,用离子方程式表示其理由:
(6)
 属于
属于
您最近一年使用:0次
6 . Ⅰ.某无色透明溶液中可能大量存在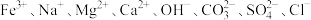 中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
①向第一份溶液中滴入几滴酚酞试液,溶液变红;
②向第二份溶液中加入过量 溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
③向第三份溶液中先加入 溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
已知: 可与水作用,产生较多的
可与水作用,产生较多的 ,使溶液呈碱性;
,使溶液呈碱性; 溶于稀硝酸。
溶于稀硝酸。
(1)根据上述实验现象可知,原溶液中一定存在的离子是_______ ,一定不存在的离子是_______ ,不能确定是否存在的离子是_______ 。
Ⅱ.次磷酸 是一种精细的磷化工产品,它是一元弱酸,具有较强的还原性,可将溶液中的
是一种精细的磷化工产品,它是一元弱酸,具有较强的还原性,可将溶液中的 还原为银单质,从而用于化学镀银。
还原为银单质,从而用于化学镀银。 的工业制法是将白磷与
的工业制法是将白磷与 溶液反应生成
溶液反应生成 气体和
气体和 ,后者再与
,后者再与 反应生成
反应生成 。
。
(2)写出白磷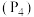 与
与 溶液反应的化学方程式:
溶液反应的化学方程式:_______ ,反应中每消耗 ,转移的电子数为
,转移的电子数为_______ 。
(3)写出 与足量
与足量 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 。
(4)工业上利用 进行化学镀银的反应中,当氧化剂与还原剂物质的量之比为4∶1时,则氧化产物中
进行化学镀银的反应中,当氧化剂与还原剂物质的量之比为4∶1时,则氧化产物中 元素的化合价为
元素的化合价为_______ 。
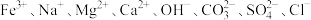 中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:
中的几种,为确定溶液中的离子组成,取三份少量溶液于试管中,进行了如下实验:①向第一份溶液中滴入几滴酚酞试液,溶液变红;
②向第二份溶液中加入过量
 溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;
溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气泡冒出;③向第三份溶液中先加入
 溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。已知:
 可与水作用,产生较多的
可与水作用,产生较多的 ,使溶液呈碱性;
,使溶液呈碱性; 溶于稀硝酸。
溶于稀硝酸。(1)根据上述实验现象可知,原溶液中一定存在的离子是
Ⅱ.次磷酸
 是一种精细的磷化工产品,它是一元弱酸,具有较强的还原性,可将溶液中的
是一种精细的磷化工产品,它是一元弱酸,具有较强的还原性,可将溶液中的 还原为银单质,从而用于化学镀银。
还原为银单质,从而用于化学镀银。 的工业制法是将白磷与
的工业制法是将白磷与 溶液反应生成
溶液反应生成 气体和
气体和 ,后者再与
,后者再与 反应生成
反应生成 。
。(2)写出白磷
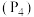 与
与 溶液反应的化学方程式:
溶液反应的化学方程式: ,转移的电子数为
,转移的电子数为(3)写出
 与足量
与足量 溶液反应的离子方程式:
溶液反应的离子方程式:(4)工业上利用
 进行化学镀银的反应中,当氧化剂与还原剂物质的量之比为4∶1时,则氧化产物中
进行化学镀银的反应中,当氧化剂与还原剂物质的量之比为4∶1时,则氧化产物中 元素的化合价为
元素的化合价为
您最近一年使用:0次
名校
解题方法
7 . 回答下列问题
(1)已知:
则2H2(g)+O2(g) =2H2O(g) ΔH=___________ kJ·mol-1。
(2)消除汽车尾气中的NO、CO,有利于减少PM2.5的排放。已知如下信息:

①N2(g)+O2(g) =2NO(g) ΔH1=___________
②2CO(g)+O2(g) = 2CO2(g) ΔH2=-565 kJ·mol-1
在催化剂作用下NO和CO转化为无毒气体,写出反应的热化学方程式:___________ 。
(3)CO和H2是工业上最常用的合成气,该合成气的制备方法很多,它们也能合成许多重要的有机物。制备该合成气的一种方法是以CH4和H2O为原料,有关反应的能量变化如图所示。
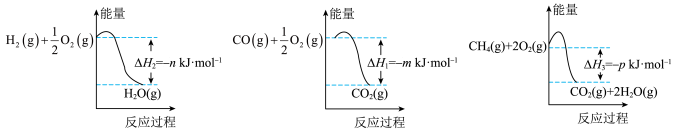
CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为___________ 。
(4)下图是锌锰干电池基本构造图,
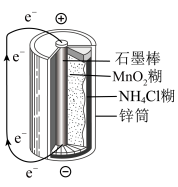
该电池的负极材料是___________ ,工作时NH 在正极放电产生两种气体,其中一种气体分子是含10e-的微粒,正极的电极反应式是
在正极放电产生两种气体,其中一种气体分子是含10e-的微粒,正极的电极反应式是___________ ;电路中每通过0.2 mol e-,负极质量减少___________ 。
(1)已知:
| 化学键 | H-H | O=O | O-H |
| 键能(kJ·mol-1) | 436 | 496 | 463 |
(2)消除汽车尾气中的NO、CO,有利于减少PM2.5的排放。已知如下信息:

①N2(g)+O2(g) =2NO(g) ΔH1=
②2CO(g)+O2(g) = 2CO2(g) ΔH2=-565 kJ·mol-1
在催化剂作用下NO和CO转化为无毒气体,写出反应的热化学方程式:
(3)CO和H2是工业上最常用的合成气,该合成气的制备方法很多,它们也能合成许多重要的有机物。制备该合成气的一种方法是以CH4和H2O为原料,有关反应的能量变化如图所示。

CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式为
(4)下图是锌锰干电池基本构造图,

该电池的负极材料是
 在正极放电产生两种气体,其中一种气体分子是含10e-的微粒,正极的电极反应式是
在正极放电产生两种气体,其中一种气体分子是含10e-的微粒,正极的电极反应式是
您最近一年使用:0次
名校
解题方法
8 . 氮、硫的氧化物都会引起环境问题,越来越引起人们的重视。
Ⅰ.某兴趣小组用Fe2(SO4)3溶液吸收含SO2的尾气(SO2的体积分数约为10%,其余为空气),实验装置如图所示:___________ 。
(2)反应后,若要检验装置A中Fe3+是否过量,可用试剂为___________ ;若要检验SO2是否过量,可用试剂为___________ 。
(3)装置B中所用X溶液常为碱溶液,其作用是___________ 。
(4)若实验测得反应后的装置A中不含有SO2,为测定其中所含FeSO4的物质的量浓度,现进行如下实验:取20.00 mL装置A中溶液,向其中逐滴加入0.100 0 mol/L Ce(SO4)2溶液,发生反应Fe2++Ce4+= Ce3++Fe3+,当反应恰好完全时,共消耗Ce(SO4)2溶液18.00 mL。则FeSO4的物质的量浓度为___________ 。
Ⅱ.工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
(5)水吸收法。结合化学方程式说明用水吸收NO2的缺陷___________ 。
(6)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学方程式:___________ 。
Ⅰ.某兴趣小组用Fe2(SO4)3溶液吸收含SO2的尾气(SO2的体积分数约为10%,其余为空气),实验装置如图所示:
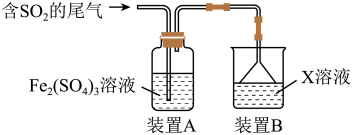
(2)反应后,若要检验装置A中Fe3+是否过量,可用试剂为
(3)装置B中所用X溶液常为碱溶液,其作用是
(4)若实验测得反应后的装置A中不含有SO2,为测定其中所含FeSO4的物质的量浓度,现进行如下实验:取20.00 mL装置A中溶液,向其中逐滴加入0.100 0 mol/L Ce(SO4)2溶液,发生反应Fe2++Ce4+= Ce3++Fe3+,当反应恰好完全时,共消耗Ce(SO4)2溶液18.00 mL。则FeSO4的物质的量浓度为
Ⅱ.工业制硝酸时尾气中含有NO、NO2,可用以下方法吸收:
(5)水吸收法。结合化学方程式说明用水吸收NO2的缺陷
(6)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学方程式:
您最近一年使用:0次
解题方法
9 . 按要求完成下列问题
(1)用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为___________ 。
(2)请写出氢氧化铁胶体制备的原理___________ (用化学方程式表示)。
(3)区分 Fe(OH)3胶体和FeCl3溶液的方法___________ 。
(4)写出H2SO4电离方程式:___________ 。
(5) 在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。在该反应中:Fe2O3发生了
在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。在该反应中:Fe2O3发生了___________ 反应(填“氧化”或“还原”),___________ 是还原剂。
(1)用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为
(2)请写出氢氧化铁胶体制备的原理
(3)区分 Fe(OH)3胶体和FeCl3溶液的方法
(4)写出H2SO4电离方程式:
(5)
 在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。在该反应中:Fe2O3发生了
在化学上被称为“铝热反应”,人们可利用该反应来焊接铁轨。在该反应中:Fe2O3发生了
您最近一年使用:0次
名校
10 . 新型冠状病毒肺炎爆发以来,各类杀菌消毒剂逐渐被人们所认识和使用。下列是常见的几种消毒剂:
①“84”消毒液(有效成分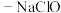 );②
);② (在水中一部分可以电离出正、负离子);③漂白粉;④
(在水中一部分可以电离出正、负离子);③漂白粉;④ ;⑤
;⑤ ;⑥碘酒;⑦75%酒精;⑧过氧乙酸
;⑥碘酒;⑦75%酒精;⑧过氧乙酸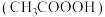 ;⑨高铁酸钠
;⑨高铁酸钠 。
。
回答下列问题:
(1)上述杀菌消毒剂_____ (填序号)属于电解质,_____ (填序号)属于非电解质。 在有催化剂条件下分解的化学方程式为
在有催化剂条件下分解的化学方程式为_____ 。
(2)巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。原因是 与
与 反应产生
反应产生 促进藻类快速生长,
促进藻类快速生长, 在该反应中做
在该反应中做_____ (填“氧化剂”或“还原剂”)。该反应说明氧化性:
_____ 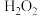 (填“
(填“ ”或“
”或“ ”)。
”)。
(3)若混合使用“洁网灵”(盐酸是成分之一)与84消毒液会产生氯气。原因是_____ (用离子方程式表示)。
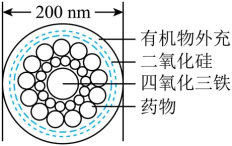
(4)如图是中国科学院上海硅酸盐研究所研发的“纳米药物分子运输车”,可提高肿瘤的治疗效果。以下说法不正确的是_____。
①“84”消毒液(有效成分
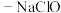 );②
);② (在水中一部分可以电离出正、负离子);③漂白粉;④
(在水中一部分可以电离出正、负离子);③漂白粉;④ ;⑤
;⑤ ;⑥碘酒;⑦75%酒精;⑧过氧乙酸
;⑥碘酒;⑦75%酒精;⑧过氧乙酸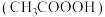 ;⑨高铁酸钠
;⑨高铁酸钠 。
。回答下列问题:
(1)上述杀菌消毒剂
 在有催化剂条件下分解的化学方程式为
在有催化剂条件下分解的化学方程式为(2)巴西奥运会期间,由于工作人员将“84”消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。原因是
 与
与 反应产生
反应产生 促进藻类快速生长,
促进藻类快速生长, 在该反应中做
在该反应中做
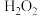 (填“
(填“ ”或“
”或“ ”)。
”)。(3)若混合使用“洁网灵”(盐酸是成分之一)与84消毒液会产生氯气。原因是
(4)如图是中国科学院上海硅酸盐研究所研发的“纳米药物分子运输车”,可提高肿瘤的治疗效果。以下说法不正确的是_____。

| A.有机物外充可以选择葡萄糖等亲生物化合物 |
| B.该“纳米药物分子车”属于混合物 |
| C.该“纳米药物分子车”分散于水后能够透过半透膜 |
| D.该“纳米药物分子车”中的二氧化硅和四氧化三铁属于氧化物 |
您最近一年使用:0次



