解题方法
1 . 某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径≤2.5um的悬浮颗粒物,已知1μm=1×10-6m),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系___________ (填“属于"或“不属于)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
根据表中数据判断待测试样为___________ (填“酸”或“碱”)性。
(3)洗涤含SO2的烟气,以下物质可作洗涤剂的是___________ (填字母)
a.Ca(OH)2 b.CaCl2 c.Na2CO3 d.NaHSO3
(4)硫酸生产及煤燃烧产生的废气SO2等会对大气造成污染。
①为防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产品用于制造石膏。脱硫反应的化学方程式为___________ 。
②某硫酸化工厂,使用一种含杂质为25%的黄铁矿石(FeS2)为原料。若取2吨该矿石,可制得98%的浓硫酸___________ 吨(假设生产过程中96%SO2转化为SO3)。
(1)PM2.5分散在空气中形成的分散系
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | NH | SO | NO | Cl- |
| 浓度/mol/L | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(3)洗涤含SO2的烟气,以下物质可作洗涤剂的是
a.Ca(OH)2 b.CaCl2 c.Na2CO3 d.NaHSO3
(4)硫酸生产及煤燃烧产生的废气SO2等会对大气造成污染。
①为防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产品用于制造石膏。脱硫反应的化学方程式为
②某硫酸化工厂,使用一种含杂质为25%的黄铁矿石(FeS2)为原料。若取2吨该矿石,可制得98%的浓硫酸
您最近一年使用:0次
解题方法
2 . 按要求回答下列问题:
(1)现有8种物质:A.稀硫酸;B.Fe2(SO4)3溶液;C.CO;D.熔融的NaNO3;E.SO2;F.Fe(OH)3胶体;G.NH4NO3固体;H.Na2CO3溶液。
①能导电的电解质有___________ (填字母,下同),属于酸性氧化物的有___________ 。
②Fe2(SO4)3溶于水的电离方程式为___________ 。
③写出实验室制取Fe(OH)3胶体的离子方程式:___________ 。
④写出H与足量A反应的离子方程式:___________ 。
(2)①甲烷(甲烷中C的化合价为-4)在厌氧氧化菌的作用下,可以和氢氧化铁发生如下反应,配平该离子方程式:___________ 。

②该反应中的还原剂为___________ (填化学式),被还原的物质与被氧化的物质的物质的量之比为___________ 。
(3)无氧条件下加热蓝铁矿(无杂质),发生反应的化学方程式为 ,蓝铁矿的质量由10.04g减小到7.16g,则n=
,蓝铁矿的质量由10.04g减小到7.16g,则n=___________ 。
(1)现有8种物质:A.稀硫酸;B.Fe2(SO4)3溶液;C.CO;D.熔融的NaNO3;E.SO2;F.Fe(OH)3胶体;G.NH4NO3固体;H.Na2CO3溶液。
①能导电的电解质有
②Fe2(SO4)3溶于水的电离方程式为
③写出实验室制取Fe(OH)3胶体的离子方程式:
④写出H与足量A反应的离子方程式:
(2)①甲烷(甲烷中C的化合价为-4)在厌氧氧化菌的作用下,可以和氢氧化铁发生如下反应,配平该离子方程式:

②该反应中的还原剂为
(3)无氧条件下加热蓝铁矿(无杂质),发生反应的化学方程式为
 ,蓝铁矿的质量由10.04g减小到7.16g,则n=
,蓝铁矿的质量由10.04g减小到7.16g,则n=
您最近一年使用:0次
3 . 回答下列问题。
(1)现有6种物质①MgCl2 ②HCl ③SO2 ④K2CO3 ⑤CaO ⑥NaHSO4 ⑦N2。请根据下列标准,对上述物质进行分类(填序号):
①属于共价化合物是___________ 。
②只含离子键的化合物是___________ 。
③含共价键的离子化合物是___________ 。
④如果将NaHSO4溶于水,破坏了NaHSO4中化学键的类型为___________ 。
(2)现有下列9种微粒: 、
、 、
、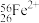 、
、 、
、 、
、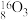 。
。
形成上述6种微粒的核素有___________ 种、元素有___________ 种。
(3)已知有下列物质:①Al ②HCl气体 ③ ④KCl ⑤熔融NaOH,其中能导电的是
④KCl ⑤熔融NaOH,其中能导电的是___________ (填标号,下同);属于电解质的是___________ ;
(1)现有6种物质①MgCl2 ②HCl ③SO2 ④K2CO3 ⑤CaO ⑥NaHSO4 ⑦N2。请根据下列标准,对上述物质进行分类(填序号):
①属于共价化合物是
②只含离子键的化合物是
③含共价键的离子化合物是
④如果将NaHSO4溶于水,破坏了NaHSO4中化学键的类型为
(2)现有下列9种微粒:
 、
、 、
、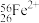 、
、 、
、 、
、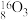 。
。形成上述6种微粒的核素有
(3)已知有下列物质:①Al ②HCl气体 ③
 ④KCl ⑤熔融NaOH,其中能导电的是
④KCl ⑤熔融NaOH,其中能导电的是
您最近一年使用:0次
解题方法
4 . 化学与生活息息相关。请回答下列问题。
(1)碳酸氢钠可单独用作蒸馒头的膨松剂,用化学方程式表示该膨松原理______ 。
(2)过氧化钠常用作呼吸面具和潜水艇里的氧气供给,用化学方程式表示____________ 。
(3)铀元素在核工业中具有重要作用,自然界中存在的铀矿石主要成分为二氧化铀(UO2)。工业上,可以用钾、钙、镁等金属与二氧化铀反应制得铀单质。若要获得等质量的铀单质,钾、钙、镁三种金属的物质的量之比为______ 。
(4)补铁口服液是常见的补铁剂,同时服用维生素C吸收效果更好,维生素C的作用为____________ 。
(5)工业上利用硫铁矿(80%FeS2)制备硫酸。
①FeS2中S的化合价为______ ,硫铁矿在氧气中焙烧产物为Fe2O3和SO2,写出该反应的化学方程式____________ 。
②不考虑生产过程中硫的损失,3吨该矿石可制得98%的浓硫酸______ 吨。
(1)碳酸氢钠可单独用作蒸馒头的膨松剂,用化学方程式表示该膨松原理
(2)过氧化钠常用作呼吸面具和潜水艇里的氧气供给,用化学方程式表示
(3)铀元素在核工业中具有重要作用,自然界中存在的铀矿石主要成分为二氧化铀(UO2)。工业上,可以用钾、钙、镁等金属与二氧化铀反应制得铀单质。若要获得等质量的铀单质,钾、钙、镁三种金属的物质的量之比为
(4)补铁口服液是常见的补铁剂,同时服用维生素C吸收效果更好,维生素C的作用为
(5)工业上利用硫铁矿(80%FeS2)制备硫酸。
①FeS2中S的化合价为
②不考虑生产过程中硫的损失,3吨该矿石可制得98%的浓硫酸
您最近一年使用:0次
名校
解题方法
5 . 2020年,比亚迪宣布推出基于磷酸铁锂技术的“刀片电池”,刀片电池能量密度大,安全性高。电池的正极活性材料是 。请回答下列问题
。请回答下列问题
(1)铁元素位于周期表第四周期第___________ 族;基态 的最外层电子排布式为
的最外层电子排布式为___________ 。
(2)正极材料 的阴离子
的阴离子 的空间结构为
的空间结构为___________ ,请写出一个与 为等电子体的分子
为等电子体的分子___________ 。
(3) 原子或离子外围有较多能量相近的空轨道,能与
原子或离子外围有较多能量相近的空轨道,能与 等形成配合物。
等形成配合物。
① 与
与 形成配位键时,提供孤电子对的原子是
形成配位键时,提供孤电子对的原子是___________ ,1mol[Fe(SCN)6]3-的 键数目为
键数目为___________ 。
②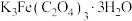 为可溶于水的晶体,某同学欲检验该晶体中
为可溶于水的晶体,某同学欲检验该晶体中 元素的价态,取少量晶体放入试管中,加蒸馏水使其充分溶解,再向试管中滴入几滴
元素的价态,取少量晶体放入试管中,加蒸馏水使其充分溶解,再向试管中滴入几滴 溶液。
溶液。
已知:i.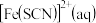 为血红色:
为血红色:
ii. 时,
时,
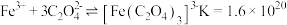
上述实验方案___________ (填“可行”或“不可行”),并解释其原因___________ 。
 。请回答下列问题
。请回答下列问题(1)铁元素位于周期表第四周期第
 的最外层电子排布式为
的最外层电子排布式为(2)正极材料
 的阴离子
的阴离子 的空间结构为
的空间结构为 为等电子体的分子
为等电子体的分子(3)
 原子或离子外围有较多能量相近的空轨道,能与
原子或离子外围有较多能量相近的空轨道,能与 等形成配合物。
等形成配合物。①
 与
与 形成配位键时,提供孤电子对的原子是
形成配位键时,提供孤电子对的原子是 键数目为
键数目为②
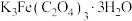 为可溶于水的晶体,某同学欲检验该晶体中
为可溶于水的晶体,某同学欲检验该晶体中 元素的价态,取少量晶体放入试管中,加蒸馏水使其充分溶解,再向试管中滴入几滴
元素的价态,取少量晶体放入试管中,加蒸馏水使其充分溶解,再向试管中滴入几滴 溶液。
溶液。已知:i.
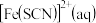 为血红色:
为血红色:ii.
 时,
时,
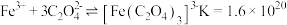
上述实验方案
您最近一年使用:0次
2024-03-13更新
|
372次组卷
|
2卷引用:山东省青岛第五十八中学2023-2024学年高二上学期期末化学试卷
解题方法
6 . 燃料电池的种类很多,氢氧燃料电池是目前最成熟的燃料电池,电解质可以是酸性的,也可以是碱性的。回答下列问题:
(1)氢氧燃料电池中,负极上通入的气体是______ ,电池总反应为______ 。
(2)若以稀硫酸作电解质溶液,电池工作时的负极反应为______ 。
(3)若以氢氧化钠溶液作电解质溶液,电池工作时的正极反应为______ 。
(1)氢氧燃料电池中,负极上通入的气体是
(2)若以稀硫酸作电解质溶液,电池工作时的负极反应为
(3)若以氢氧化钠溶液作电解质溶液,电池工作时的正极反应为
您最近一年使用:0次
7 . 海洋是个巨大的资源宝库,利用海水可以获得淡水、食盐、单质溴、单质镁等多种化学物质。结合有关过程回答下列问题:
(1)利用海水制备下列物质,不用通过化学反应过程就可以得到的是______。
(2)氯碱工业中电解饱和食盐水可以得到氢氧化钠、氯气和氢气,写出电解反应的化学方程式______ 。
(3)实验室中通常用浓盐酸和二氧化锰加热制备氯气,反应的化学方程式为______ 。用该种方法制备的氯气中含有杂质,为获得纯净干燥的氯气,可将气体依次通入盛有______ 和浓硫酸的洗气瓶中。
(4)海水中提取镁,先制备MgCl2再进一步获得单质镁,由MgCl2得到单质镁的化学方程式为______ 。
(1)利用海水制备下列物质,不用通过化学反应过程就可以得到的是______。
| A.氢氧化钠 | B.单质镁 | C.淡水 | D.单质溴 |
(3)实验室中通常用浓盐酸和二氧化锰加热制备氯气,反应的化学方程式为
(4)海水中提取镁,先制备MgCl2再进一步获得单质镁,由MgCl2得到单质镁的化学方程式为
您最近一年使用:0次
8 . 现有下列几种物质:
①Al2O3、②CuO、③NaHSO4、④FeCl3、⑤Cl2、⑥NaOH、⑦稀硫酸。回答下列问题:
(1)上述物质中属于碱性氧化物的是___________ (填序号,下同),属于两性氧化物的是___________ ,属于混合物的是___________ 。
(2)上述物质在水中能电离出三种离子的是___________ (填序号);写出④的电离方程式:___________ 。
(3)写出①与⑦反应的离子方程式:___________ 。
①Al2O3、②CuO、③NaHSO4、④FeCl3、⑤Cl2、⑥NaOH、⑦稀硫酸。回答下列问题:
(1)上述物质中属于碱性氧化物的是
(2)上述物质在水中能电离出三种离子的是
(3)写出①与⑦反应的离子方程式:
您最近一年使用:0次
9 . 回答下列问题。
(1)Na、Fe、Cl、Al是中学化学常见的元素。
①含上述某一种元素的常见化合物中,呈淡黄色的是___________ (填化学式)。
②焰色试验中,Na元素燃烧时的焰色为___________ 色,观察K元素燃烧时的焰色需要透过___________ 。
③实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是___________ ,反应的化学方程式为___________ 。
(2)饮用水质量是关系人类健康的重要问题。
氯气是最早用于饮用水消毒的物质,其消毒作用主要是氯气溶于水后生成了次氯酸,该反应的离子方程式为___________ 。
(1)Na、Fe、Cl、Al是中学化学常见的元素。
①含上述某一种元素的常见化合物中,呈淡黄色的是
②焰色试验中,Na元素燃烧时的焰色为
③实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是
(2)饮用水质量是关系人类健康的重要问题。
氯气是最早用于饮用水消毒的物质,其消毒作用主要是氯气溶于水后生成了次氯酸,该反应的离子方程式为
您最近一年使用:0次
10 . 电化学原理在电池制造、能量转换、物质合成等方面应用广泛。
(1)若用如图装置,依据反应Cu+2Fe3+=2Fe2++Cu2+设计原电池,则电极X应为___________ (填化学式),石墨电极的电极反应式为___________ 。将石墨换成铁电极后,电池总反应变为___________ 。

(2)燃料电池必须从电池外部源源不断地向电池提供天然气、甲烷、煤气等含氢化合物作为燃料。基于甲烷(CH4)-空气燃料电池,其工作原理如图,a、b均为惰性电极。a为___________ 极,正极的电极反应式为___________ 。当通入4.48L(标准状况下)甲烷气体时,测得电路中转移1.1mol电子,则甲烷的利用率为___________ 。(保留小数点后1位)。

(3)以如图所示装置模拟生产硫酸:

写出通入O2的电极的电极反应式___________ ,若此过程中转移了0.2mol电子,则质子膜两侧电解液的质量变化差(Δm左-Δm右)为___________ g(忽略气体的溶解)。
(4)一种可充电电池装置如图所示,充放电过程中,存在LiCoO2与Li1-xCoO2之间的转化。

①放电过程中Li+的移动方向___________ (填“A→B”或“B→A”);
②写出该电池放电时A极反应___________ ,充电时,阳极的电极反应式为___________ ;
③放电时,当电路中转移0.2NA电子时,A极质量减少___________ g。
(1)若用如图装置,依据反应Cu+2Fe3+=2Fe2++Cu2+设计原电池,则电极X应为

(2)燃料电池必须从电池外部源源不断地向电池提供天然气、甲烷、煤气等含氢化合物作为燃料。基于甲烷(CH4)-空气燃料电池,其工作原理如图,a、b均为惰性电极。a为

(3)以如图所示装置模拟生产硫酸:

写出通入O2的电极的电极反应式
(4)一种可充电电池装置如图所示,充放电过程中,存在LiCoO2与Li1-xCoO2之间的转化。

①放电过程中Li+的移动方向
②写出该电池放电时A极反应
③放电时,当电路中转移0.2NA电子时,A极质量减少
您最近一年使用:0次



