名校
1 . 科学家利用氧化锆锌作催化剂,在一定温度下将 和
和 转化为重要有机原料甲醇
转化为重要有机原料甲醇 ,其原理为:
,其原理为:
 。在容积为
。在容积为 的恒温密闭容器中,充入
的恒温密闭容器中,充入 和
和 发生上述反应。
发生上述反应。 和
和 的物质的量随时间变化如图所示。回答下列问题:
的物质的量随时间变化如图所示。回答下列问题:
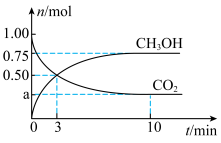
(1)图中
_____ ; 时,
时, 的转化率为
的转化率为_____ 。
(2)下列叙述正确的是_____ (填序号)。
a. 时
时 的生成速率等于其分解速率
的生成速率等于其分解速率
b.由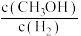 保持不变,可判断该反应达到平衡状态
保持不变,可判断该反应达到平衡状态
c.当 时,该反应一定达到平衡状态
时,该反应一定达到平衡状态
d.若改变催化剂,则反应达到平衡状态所需的时间一定小于
(3)该温度下达到平衡时,混合气体中 的体积分数为
的体积分数为_____ ,此时体系压强与开始时的压强之比为_____ 。
(4)其他条件不变时,下列措施不能使生成 的反应速率增大的是
的反应速率增大的是_____ (填序号)。
a.增大 的浓度
的浓度
b.将容器的容积变为
c.恒容条件下充入一定量
d.将恒温恒容容器改为绝热恒容容器
已知升高温度,平衡向吸热方向移动。降低温度,此反应再次达到平衡时体系中混合气体的平均摩尔质量_____ (填“增大”“减小”或“不变”)。
 和
和 转化为重要有机原料甲醇
转化为重要有机原料甲醇 ,其原理为:
,其原理为:
 。在容积为
。在容积为 的恒温密闭容器中,充入
的恒温密闭容器中,充入 和
和 发生上述反应。
发生上述反应。 和
和 的物质的量随时间变化如图所示。回答下列问题:
的物质的量随时间变化如图所示。回答下列问题:
(1)图中

 时,
时, 的转化率为
的转化率为(2)下列叙述正确的是
a.
 时
时 的生成速率等于其分解速率
的生成速率等于其分解速率b.由
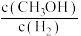 保持不变,可判断该反应达到平衡状态
保持不变,可判断该反应达到平衡状态c.当
 时,该反应一定达到平衡状态
时,该反应一定达到平衡状态d.若改变催化剂,则反应达到平衡状态所需的时间一定小于

(3)该温度下达到平衡时,混合气体中
 的体积分数为
的体积分数为(4)其他条件不变时,下列措施不能使生成
 的反应速率增大的是
的反应速率增大的是a.增大
 的浓度
的浓度b.将容器的容积变为

c.恒容条件下充入一定量

d.将恒温恒容容器改为绝热恒容容器
已知升高温度,平衡向吸热方向移动。降低温度,此反应再次达到平衡时体系中混合气体的平均摩尔质量
您最近一年使用:0次
2023-07-12更新
|
608次组卷
|
2卷引用:山东省潍坊市2022-2023学年高一下学期期末考试化学试题
2 . 向27.2gCu和Cu2O的固体混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成4.48LNO(标准状况)和Cu(NO3)2,在所得溶液中加入1.0mol•L-1的NaOH溶液1.0L,此时溶液中的溶质为NaNO3,铜离子已完全沉淀,沉淀质量为39.2g。(提示:Cu2O稀硝酸反应的方程式为:3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O)
(1)在上述Cu2O与硝酸的反应中,硝酸表现出的性质有______ 。
(2)计算原固体混合物Cu2O中Cu与的物质的量之比_____ 。
(3)计算原硝酸溶液的物质的量浓度_____ 。
(1)在上述Cu2O与硝酸的反应中,硝酸表现出的性质有
(2)计算原固体混合物Cu2O中Cu与的物质的量之比
(3)计算原硝酸溶液的物质的量浓度
您最近一年使用:0次
2023-05-05更新
|
794次组卷
|
3卷引用:山东新高考2022-2023学年高一上学期质量测评模拟演练化学试题
山东新高考2022-2023学年高一上学期质量测评模拟演练化学试题 浙江省长河中学2022-2023学年高一下学期期中考试化学试题 (已下线)【2023】【高一下】【期中考】【长河】【高中化学】【刘尼尼收集】
2023高三·全国·专题练习
3 . 已知 时某弱酸
时某弱酸 的电离常
的电离常 ,则
,则 时
时 的
的 溶液中
溶液中 浓度是
浓度是_______ 。
 时某弱酸
时某弱酸 的电离常
的电离常 ,则
,则 时
时 的
的 溶液中
溶液中 浓度是
浓度是
您最近一年使用:0次
名校
4 . 据部分键能数据,以及热化学方程式 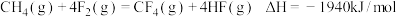 ,计算
,计算  键的键能为
键的键能为_______ 。
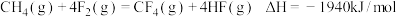 ,计算
,计算  键的键能为
键的键能为| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ/mol) | 414 | 489 | ? | 155 |
您最近一年使用:0次
2022-04-07更新
|
341次组卷
|
2卷引用:山东省济宁市特殊教育学校2023-2024学年高二上学期期末化学试卷
解题方法
5 .  可作为食盐中的补碘剂,可采用“电解法”制备。先将一定量的碘溶于过量氢氧化钾溶液,发生反应:
可作为食盐中的补碘剂,可采用“电解法”制备。先将一定量的碘溶于过量氢氧化钾溶液,发生反应: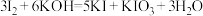 ,将反应后的溶液加入阳极区,阴极区加入氢氧化钾溶液,开始电解。装置如下图所示:
,将反应后的溶液加入阳极区,阴极区加入氢氧化钾溶液,开始电解。装置如下图所示:
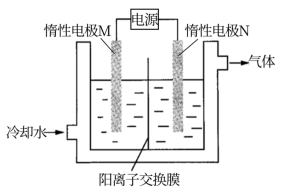
回答下列问题:
(1)惰性电极M为___________ (填“阳极”或“阴极”),其电极反应式为___________ 。
(2)若电解时用铅蓄电池做电源,当消耗2mol单质铅时,电解生成气体的物质的量是___________ mol。
(3)若电解结束时,阳极反应生成 ,则理论上消耗的
,则理论上消耗的 的物质的量为
的物质的量为___________ mol。
(4)常温下若有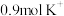 通过阳离子交换膜,阴极区KOH溶液pH由13升到14,则阴极区KOH溶液体积为
通过阳离子交换膜,阴极区KOH溶液pH由13升到14,则阴极区KOH溶液体积为___________ L(忽略溶液体积变化)。
(5)若电解池工作前,阳极室和阴极室中电解液质量相等,当转移___________ mol电子时,两侧电解液的质量差为308g。
 可作为食盐中的补碘剂,可采用“电解法”制备。先将一定量的碘溶于过量氢氧化钾溶液,发生反应:
可作为食盐中的补碘剂,可采用“电解法”制备。先将一定量的碘溶于过量氢氧化钾溶液,发生反应: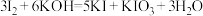 ,将反应后的溶液加入阳极区,阴极区加入氢氧化钾溶液,开始电解。装置如下图所示:
,将反应后的溶液加入阳极区,阴极区加入氢氧化钾溶液,开始电解。装置如下图所示:
回答下列问题:
(1)惰性电极M为
(2)若电解时用铅蓄电池做电源,当消耗2mol单质铅时,电解生成气体的物质的量是
(3)若电解结束时,阳极反应生成
 ,则理论上消耗的
,则理论上消耗的 的物质的量为
的物质的量为(4)常温下若有
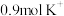 通过阳离子交换膜,阴极区KOH溶液pH由13升到14,则阴极区KOH溶液体积为
通过阳离子交换膜,阴极区KOH溶液pH由13升到14,则阴极区KOH溶液体积为(5)若电解池工作前,阳极室和阴极室中电解液质量相等,当转移
您最近一年使用:0次
解题方法
6 . 工业废气中CO的处理和合理利用,越来越受到关注。
(1)在两个固定容积为2L的恒容密闭容器中均充入2molCO和2molNO,在不同条件下发生反应2CO(g)+2NO(g) ⇌2CO2(g)+N2(g),实验测得反应体系的压强与时间t的变化曲线如图所示。
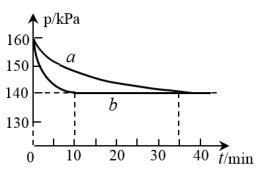
①与实验a相比,实验b采取的措施可能是_______ ,理由是_______ ;
②0~10min内,实验b对应条件下υ(NO)=_______ ;
③实验a条件下,反应的平衡常数Kc=_______ 。
(2)CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g) ⇌CH3OH(g) △H。已知:υ(正)=k(正)·x(CO)·x2(H2),υ(逆)=k(逆)·x(CH3OH),其中x为各组分的体积分数。在密闭容器中按物质的量之比为1∶2充入CO和H2,测得平衡混合气体中CO的平衡转化率随温度、压强的变化关系如图所示。
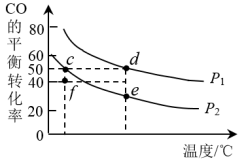
①P1_______ P2(填“>”“<”);升高温度,
_______ (填“增大”“减小”或“不变”);
②c、d、e三点平衡常数Kc、Kd、Ke三者之间的关系为_______ ,理由是_______ ;
③f点, =
=_______ (保留三位有效数字)。
(1)在两个固定容积为2L的恒容密闭容器中均充入2molCO和2molNO,在不同条件下发生反应2CO(g)+2NO(g) ⇌2CO2(g)+N2(g),实验测得反应体系的压强与时间t的变化曲线如图所示。

①与实验a相比,实验b采取的措施可能是
②0~10min内,实验b对应条件下υ(NO)=
③实验a条件下,反应的平衡常数Kc=
(2)CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g) ⇌CH3OH(g) △H。已知:υ(正)=k(正)·x(CO)·x2(H2),υ(逆)=k(逆)·x(CH3OH),其中x为各组分的体积分数。在密闭容器中按物质的量之比为1∶2充入CO和H2,测得平衡混合气体中CO的平衡转化率随温度、压强的变化关系如图所示。

①P1

②c、d、e三点平衡常数Kc、Kd、Ke三者之间的关系为
③f点,
 =
=
您最近一年使用:0次
解题方法
7 . 化学正在走向精准。当代化学的三大支柱是:理论、实验和计算。
Ⅰ.某溶液为硫酸和硝酸混合后的稀溶液,取200.00mL,该溶液加入过量锌粉充分反应。反应后溶液中只含有一种溶质,其浓度为 (溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。
(溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。______
Ⅱ.某硫铜矿的主要成分为 ,可用于冶炼金属铜,为测定矿石中
,可用于冶炼金属铜,为测定矿石中 的质量分数,进行如下实验(杂质不参加反应):
的质量分数,进行如下实验(杂质不参加反应):
步骤1:在1.00g试样中加入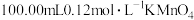 的酸性溶液,加热,硫元素全部转化为
的酸性溶液,加热,硫元素全部转化为 ,铜元素全部转化为
,铜元素全部转化为 ,滤去不溶性杂质。
,滤去不溶性杂质。
步骤2:收集步骤1所得滤液至250mL容量瓶中,定容。取25.00mL溶液,用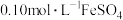 溶液与剩余
溶液与剩余 恰好反应,消耗10.00mL。列式计算
恰好反应,消耗10.00mL。列式计算 的质量分数
的质量分数______ 。
Ⅰ.某溶液为硫酸和硝酸混合后的稀溶液,取200.00mL,该溶液加入过量锌粉充分反应。反应后溶液中只含有一种溶质,其浓度为
 (溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。
(溶液体积不变),收集到无色气体6.72L(标准状况),请列式计算溶液中硫酸和硝酸的浓度比,及产生的氢气的体积(标准状况)。Ⅱ.某硫铜矿的主要成分为
 ,可用于冶炼金属铜,为测定矿石中
,可用于冶炼金属铜,为测定矿石中 的质量分数,进行如下实验(杂质不参加反应):
的质量分数,进行如下实验(杂质不参加反应):步骤1:在1.00g试样中加入
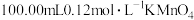 的酸性溶液,加热,硫元素全部转化为
的酸性溶液,加热,硫元素全部转化为 ,铜元素全部转化为
,铜元素全部转化为 ,滤去不溶性杂质。
,滤去不溶性杂质。步骤2:收集步骤1所得滤液至250mL容量瓶中,定容。取25.00mL溶液,用
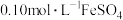 溶液与剩余
溶液与剩余 恰好反应,消耗10.00mL。列式计算
恰好反应,消耗10.00mL。列式计算 的质量分数
的质量分数
您最近一年使用:0次
8 . 实验室常常用氯化铵与足量熟石灰混合加热制取氨气。现欲制取4.48L(标准状况)氨气,至少需要称取氯化铵的质量是___________ 。
您最近一年使用:0次
2021-05-24更新
|
976次组卷
|
2卷引用:山东新高考2022-2023学年高一上学期质量测评模拟演练化学试题
9 . 氢气作为一种清洁能源,一直是能源研究的热点,工业上制取氢气有多种方法:
①C(s)+H2O(g)=CO(g)+H2(g) △H1=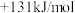
②CH4 (g)+CO2(g)=2CO(g)+2H2 (g) △H2=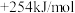
③CH4 (g)+H2O(g)=CO(g)+3H2 (g) △H3=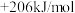
④CH3OH(1)=CO(g)+2H2 (g) △H4=
(1)根据以上数据,请写出CH4(g)分解生成C(s)和H2(g)的热化学方程式______ 。
(2)几种化学键的键能如下表所示:
根据以上有关反应的△H,计算 x=______ 。
(3)我国科学家通过计算机模拟,研究了在某催化剂表面上发生反应④的反应历程(吸附在催化剂表面的物质,用"*"标注)。甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式Ⅰ: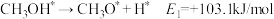
方式Ⅱ:
活化能E值推测,甲醇脱氢过程中主要历程的方式为______ (填"Ⅰ"或"Ⅱ")。计算机模拟的各步反应的能量变化示意图如下。

该历程中最大能垒(活化能)E正=______ kJ/mol,写出该步骤的化学方程式______ 。
①C(s)+H2O(g)=CO(g)+H2(g) △H1=
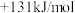
②CH4 (g)+CO2(g)=2CO(g)+2H2 (g) △H2=
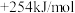
③CH4 (g)+H2O(g)=CO(g)+3H2 (g) △H3=
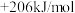
④CH3OH(1)=CO(g)+2H2 (g) △H4=

(1)根据以上数据,请写出CH4(g)分解生成C(s)和H2(g)的热化学方程式
(2)几种化学键的键能如下表所示:
| 化学键 | C=O | H—H | 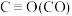 | C—H | O—H |
| 键能/kJ·mol-1 | 803 | 436 | x | 414 | 463 |
根据以上有关反应的△H,计算 x=
(3)我国科学家通过计算机模拟,研究了在某催化剂表面上发生反应④的反应历程(吸附在催化剂表面的物质,用"*"标注)。甲醇(CH3OH)脱氢反应的第一步历程,有两种可能方式:
方式Ⅰ:
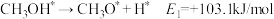
方式Ⅱ:

活化能E值推测,甲醇脱氢过程中主要历程的方式为

该历程中最大能垒(活化能)E正=
您最近一年使用:0次
10 . 电解质溶液中存在多种平衡体系,请根据相关信息回答下列问题。
(1)已知:常温下,FeS和CuS的溶度积分别为 ,
,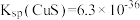 。
。
①向FeS悬浊液中滴加CuCl2溶液产生黑色沉淀,发生反应的离子方程式_____ 。
②在饱和FeS和CuS的混合溶液中
____ 。
③测得某矿物浸出液中 ,加入Na2S出现沉淀时,Na2S的浓度应大于
,加入Na2S出现沉淀时,Na2S的浓度应大于_____  。
。
(2)已知:常温下,HA的Ka=6.2×10-10。
①常温下,含等物质的量浓度的HA与NaA的混合溶液显_____ (填“酸”“碱”或“中”)性,c平(A-)_____ (填“>”“<”或“=”)c平(HA),该溶液中各离子浓度由大到小的顺序为______ 。
②常温下,若将c mol/L盐酸与0.6 mol/LKA溶液等体积混合后恰好得到中性溶液,则c=_____ mol/L (小数点后保留4位数字)。
(1)已知:常温下,FeS和CuS的溶度积分别为
 ,
,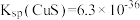 。
。①向FeS悬浊液中滴加CuCl2溶液产生黑色沉淀,发生反应的离子方程式
②在饱和FeS和CuS的混合溶液中

③测得某矿物浸出液中
 ,加入Na2S出现沉淀时,Na2S的浓度应大于
,加入Na2S出现沉淀时,Na2S的浓度应大于 。
。(2)已知:常温下,HA的Ka=6.2×10-10。
①常温下,含等物质的量浓度的HA与NaA的混合溶液显
②常温下,若将c mol/L盐酸与0.6 mol/LKA溶液等体积混合后恰好得到中性溶液,则c=
您最近一年使用:0次



