名校
1 . “84消毒液”能有效杀灭甲型H1N1病毒,某同学购买了一瓶84消毒液,该消毒液通常稀释到100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如图信息:
(1)该84消毒液NaClO物质的量浓度约为_______ (保留1位小数)。
(2)该同学参阅该84消毒液的配方,欲用NaClO固体配制480mL该种84消毒液。下列说法不正确的是_______ (填字母)。
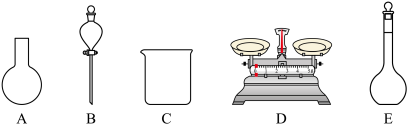
A.如图所示的仪器中,有三种是不需要的,还另需要一种玻璃仪器
B.使用前要检查容量瓶是否漏液
C.容量瓶上标有容积、温度和浓度
D.需要称量NaClO固体的质量为149.0g
E.容量瓶用蒸馏水洗净后,须烘干后再使用
(3)一瓶上述84消毒液理论上能吸收空气中_______ L的CO2(标准状况下)而变质。(已知:CO2+NaClO+H2O=NaHCO3+HClO)
(4)84消毒液与稀硫酸混合使用可增强消毒能力,请用化学方程式解释其原因_______ ,某消毒小组人员用18.4mol·L-1的浓硫酸配制500mL2.3mol·L-1的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为_______ mL。
(5)在配制过程中,下列操作中能使所配溶液的浓度偏高的有_______ (填代号)。
①用量筒量取98%的硫酸时俯视
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤定容时,俯视刻度线
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
| 84消毒液 (有效成分)NaClO (规格)1000mL (质量分数)25% (密度)1.19g/cm3 |
(1)该84消毒液NaClO物质的量浓度约为
(2)该同学参阅该84消毒液的配方,欲用NaClO固体配制480mL该种84消毒液。下列说法不正确的是

A.如图所示的仪器中,有三种是不需要的,还另需要一种玻璃仪器
B.使用前要检查容量瓶是否漏液
C.容量瓶上标有容积、温度和浓度
D.需要称量NaClO固体的质量为149.0g
E.容量瓶用蒸馏水洗净后,须烘干后再使用
(3)一瓶上述84消毒液理论上能吸收空气中
(4)84消毒液与稀硫酸混合使用可增强消毒能力,请用化学方程式解释其原因
(5)在配制过程中,下列操作中能使所配溶液的浓度偏高的有
①用量筒量取98%的硫酸时俯视
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤定容时,俯视刻度线
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
您最近一年使用:0次
2023-08-26更新
|
284次组卷
|
2卷引用:福建省福州市九师教学联盟2023-2024学年高一上学期期末学业联考化学试题
名校
2 . 完成下列问题
(Ⅰ)某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol/L、2.00 mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验HNO3的用量为25.0 mL。大理石用量为10.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填空:
(Ⅱ)把2.5 mol A和2.5 mol B混合放入2 L密闭容器里,发生反应: 3A(g)+B(g) xC(g)+2D(g),经5s后反应达到平衡。在此5 s内C的平均反应速率为0.2 mol/(L·s),同时生成1 mol D。试求:
xC(g)+2D(g),经5s后反应达到平衡。在此5 s内C的平均反应速率为0.2 mol/(L·s),同时生成1 mol D。试求:
(2)达到平衡时B的转化率为___________ 。
(3)x的值为___________ 。
(Ⅰ)某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol/L、2.00 mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验HNO3的用量为25.0 mL。大理石用量为10.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填空:
| 实验编号 | 温度/℃ | 大理石规格 | HNO3浓度(mol/L) | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究浓度对反应速率的影响 |
| ② | 25 | 粗颗粒 | (Ⅱ)实验①和③探究温度对反应速率的影响; | |
| ③ | 粗颗粒 | 2.00 | (Ⅲ)实验①和④探究 | |
| ④ | 25 | 细颗粒 | 2.00 |
(Ⅱ)把2.5 mol A和2.5 mol B混合放入2 L密闭容器里,发生反应: 3A(g)+B(g)
 xC(g)+2D(g),经5s后反应达到平衡。在此5 s内C的平均反应速率为0.2 mol/(L·s),同时生成1 mol D。试求:
xC(g)+2D(g),经5s后反应达到平衡。在此5 s内C的平均反应速率为0.2 mol/(L·s),同时生成1 mol D。试求:(2)达到平衡时B的转化率为
(3)x的值为
您最近一年使用:0次
解题方法
3 . 为测定某 溶液的浓度,取
溶液的浓度,取 待测液,向其中加入过量
待测液,向其中加入过量 溶液。充分反应后过滤、洗涤并干燥,得到
溶液。充分反应后过滤、洗涤并干燥,得到 沉淀的质量为
沉淀的质量为 ,反应的化学方程式为
,反应的化学方程式为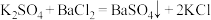 。求该溶液中
。求该溶液中 的物质的量浓度
的物质的量浓度_______ (请写出计算过程)。
 溶液的浓度,取
溶液的浓度,取 待测液,向其中加入过量
待测液,向其中加入过量 溶液。充分反应后过滤、洗涤并干燥,得到
溶液。充分反应后过滤、洗涤并干燥,得到 沉淀的质量为
沉淀的质量为 ,反应的化学方程式为
,反应的化学方程式为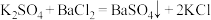 。求该溶液中
。求该溶液中 的物质的量浓度
的物质的量浓度
您最近一年使用:0次
4 . 已知可逆反应CO(g)+H2O(g) CO2(g)+H2(g),平衡常数为K。
CO2(g)+H2(g),平衡常数为K。
(1)557℃时,若起始浓度:CO为1mol·L-1,H2O为1.5mol·L-1,平衡时CO转化率为60%,则H2O的转化率为___________ ;K值为___________ 。
(2)557℃时,若起始浓度改为:CO为1mol·L-1,H2O为3mol·L-1,平衡时H2O的转化率为___________ 。
 CO2(g)+H2(g),平衡常数为K。
CO2(g)+H2(g),平衡常数为K。(1)557℃时,若起始浓度:CO为1mol·L-1,H2O为1.5mol·L-1,平衡时CO转化率为60%,则H2O的转化率为
(2)557℃时,若起始浓度改为:CO为1mol·L-1,H2O为3mol·L-1,平衡时H2O的转化率为
您最近一年使用:0次
2022-08-27更新
|
624次组卷
|
5卷引用:福建省莆田第十五中学2019-2020学年高二上学期期末考试化学试题
福建省莆田第十五中学2019-2020学年高二上学期期末考试化学试题河北省邯郸市魏县2022-2023学年高二上学期期末考试化学试题(已下线)2.2.2 化学平衡常数(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)2.2.1 化学平衡常数-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第09讲 化学平衡常数(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)
名校
解题方法
5 . 现有浓度均为0.1mol·L-1的下列溶液:①硫酸②醋酸③氢氧化钠④氯化铵⑤醋酸铵⑥硫酸氢铵⑦氨水。
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是____ (填序号)。
(2)④、⑤、⑥、⑦四种溶液中 浓度由大到小的顺序是
浓度由大到小的顺序是____ (填序号)。
(3)将③和④按体积比1:2混合后显碱性,混合液中各离子浓度由大到小的顺序是____ 。
(4)已知t℃,Kw=1×10-13,在t℃时将pH=11的NaOH溶液aL与pH=2的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=7,则a___ b(填“>”或“<”或“=”)。
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是
(2)④、⑤、⑥、⑦四种溶液中
 浓度由大到小的顺序是
浓度由大到小的顺序是(3)将③和④按体积比1:2混合后显碱性,混合液中各离子浓度由大到小的顺序是
(4)已知t℃,Kw=1×10-13,在t℃时将pH=11的NaOH溶液aL与pH=2的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=7,则a
您最近一年使用:0次
21-22高一·全国·课后作业
6 . 氯化钠是一种重要的化工原料,电解氯化钠溶液可制得氯气、氢氧化钠等物质,发生的化学反应如下:2NaCl + 2H2O Cl2 ↑+ H2 ↑+ 2NaOH。现取一定质量的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电。生成氯气的质量与时间的关系如图所示。请计算:
Cl2 ↑+ H2 ↑+ 2NaOH。现取一定质量的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电。生成氯气的质量与时间的关系如图所示。请计算:
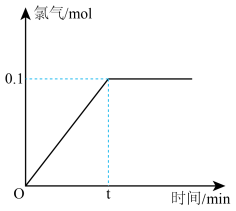
(1)参加反应的氯化钠是_______ 克?
(2)生成氢气_______ 克?生成NaOH_______ mol?
 Cl2 ↑+ H2 ↑+ 2NaOH。现取一定质量的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电。生成氯气的质量与时间的关系如图所示。请计算:
Cl2 ↑+ H2 ↑+ 2NaOH。现取一定质量的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电。生成氯气的质量与时间的关系如图所示。请计算:
(1)参加反应的氯化钠是
(2)生成氢气
您最近一年使用:0次
2021-07-27更新
|
494次组卷
|
6卷引用:福建省莆田第十五中学2021-2022学年高一上学期期末考试化学试题
福建省莆田第十五中学2021-2022学年高一上学期期末考试化学试题(已下线)1.2.1 物质的量(2)(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)(已下线)周末培优5 物质的量应用于化学方程式的计算专练-2021-2022学年高一化学课后培优练(人教版2019必修第一册)(已下线)第14讲 化学方程式的计算-【暑假自学课】2022年新高一化学暑假精品课(沪科版2020必修第一册)作业(八) 物质的量在化学反应中的应用(已下线)【定心卷】3.2.2 物质的量在化学方程式计算中的应用随堂练习-人教版2023-2024学年必修第一册
7 . 在汽车排气系统中安装三元催化转化器,可发生下列反应:2NO(g)+2CO(g)  2CO2(g)+N2(g)。在某恒容密闭容器中通入等物质的量的CO和NO,在不同温度(T)下发生上述反应时,c(CO)随时间(t)的变化曲线如图所示:
2CO2(g)+N2(g)。在某恒容密闭容器中通入等物质的量的CO和NO,在不同温度(T)下发生上述反应时,c(CO)随时间(t)的变化曲线如图所示:

(1)温度为 时,反应开始19s内的平均反应速率:v(N2)=
时,反应开始19s内的平均反应速率:v(N2)=___________
(2)温度为 时,平衡常数K=
时,平衡常数K=___________ (填计算结果的数值)
(3)温度为 时,反应达到平衡时
时,反应达到平衡时 的转化率为
的转化率为___________ 。
 2CO2(g)+N2(g)。在某恒容密闭容器中通入等物质的量的CO和NO,在不同温度(T)下发生上述反应时,c(CO)随时间(t)的变化曲线如图所示:
2CO2(g)+N2(g)。在某恒容密闭容器中通入等物质的量的CO和NO,在不同温度(T)下发生上述反应时,c(CO)随时间(t)的变化曲线如图所示:
(1)温度为
 时,反应开始19s内的平均反应速率:v(N2)=
时,反应开始19s内的平均反应速率:v(N2)=(2)温度为
 时,平衡常数K=
时,平衡常数K=(3)温度为
 时,反应达到平衡时
时,反应达到平衡时 的转化率为
的转化率为
您最近一年使用:0次
名校
解题方法
8 . 硫酸厂的烟道气会严重污染环境,保护环境、变废为宝成为了当今时代的主题。
(1)请写出采用石灰乳吸收少量SO2的化学方程式:_______
(2)某硫酸厂每天排放1.0×104 m3(标准状况)尾气,其中含0.2%(体积分数)的SO2。现用石灰乳进行处理,每天至少需要Ca(OH)2 的质量为_______ kg。(计算结果保留1位小数)
(3)工业上常用二氧化硫对溴单质进行精制,请写出SO2与Br2在酸性的水溶液中发生氧化还原的离子方程式_______
(1)请写出采用石灰乳吸收少量SO2的化学方程式:
(2)某硫酸厂每天排放1.0×104 m3(标准状况)尾气,其中含0.2%(体积分数)的SO2。现用石灰乳进行处理,每天至少需要Ca(OH)2 的质量为
(3)工业上常用二氧化硫对溴单质进行精制,请写出SO2与Br2在酸性的水溶液中发生氧化还原的离子方程式
您最近一年使用:0次
解题方法
9 . 加热条件下,用二氧化锰与足量的浓盐酸反应,制得氯气1.12L(标准状况)。(MnO2+4HCl(浓) MnCl2+2H2O+ Cl2↑)
MnCl2+2H2O+ Cl2↑)
(1)理论上需要消耗MnO2的质量是_____________ 。
(2)被氧化的HCl的物质的量是____________ 。
 MnCl2+2H2O+ Cl2↑)
MnCl2+2H2O+ Cl2↑)(1)理论上需要消耗MnO2的质量是
(2)被氧化的HCl的物质的量是
您最近一年使用:0次
解题方法
10 . 二氧化氯(ClO2)作为第四代消毒剂,已被世界卫生组织列为A1级高效安全灭菌消毒剂,我国从2000年起就逐渐用二氧化氯替代氯气对饮用水进行消毒。工业制取二氧化氯的化学方程式为:2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4。若有100mLNaClO3溶液完全反应,共消耗0.075molH2SO4。(写出计算过程)
(1)求生成ClO2的物质的量___ 。
(2)求NaClO3溶液的物质的量浓度___ 。
(1)求生成ClO2的物质的量
(2)求NaClO3溶液的物质的量浓度
您最近一年使用:0次



