“84消毒液”能有效杀灭甲型H1N1病毒,某同学购买了一瓶84消毒液,该消毒液通常稀释到100倍(体积比)使用。查阅相关资料和消毒液包装说明得到如图信息:
(1)该84消毒液NaClO物质的量浓度约为_______ (保留1位小数)。
(2)该同学参阅该84消毒液的配方,欲用NaClO固体配制480mL该种84消毒液。下列说法不正确的是_______ (填字母)。
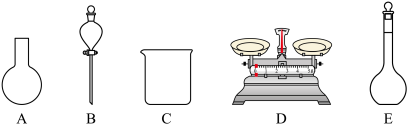
A.如图所示的仪器中,有三种是不需要的,还另需要一种玻璃仪器
B.使用前要检查容量瓶是否漏液
C.容量瓶上标有容积、温度和浓度
D.需要称量NaClO固体的质量为149.0g
E.容量瓶用蒸馏水洗净后,须烘干后再使用
(3)一瓶上述84消毒液理论上能吸收空气中_______ L的CO2(标准状况下)而变质。(已知:CO2+NaClO+H2O=NaHCO3+HClO)
(4)84消毒液与稀硫酸混合使用可增强消毒能力,请用化学方程式解释其原因_______ ,某消毒小组人员用18.4mol·L-1的浓硫酸配制500mL2.3mol·L-1的稀硫酸用于增强84消毒液的消毒能力,需取用浓硫酸的体积为_______ mL。
(5)在配制过程中,下列操作中能使所配溶液的浓度偏高的有_______ (填代号)。
①用量筒量取98%的硫酸时俯视
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤定容时,俯视刻度线
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
| 84消毒液 (有效成分)NaClO (规格)1000mL (质量分数)25% (密度)1.19g/cm3 |
(1)该84消毒液NaClO物质的量浓度约为
(2)该同学参阅该84消毒液的配方,欲用NaClO固体配制480mL该种84消毒液。下列说法不正确的是

A.如图所示的仪器中,有三种是不需要的,还另需要一种玻璃仪器
B.使用前要检查容量瓶是否漏液
C.容量瓶上标有容积、温度和浓度
D.需要称量NaClO固体的质量为149.0g
E.容量瓶用蒸馏水洗净后,须烘干后再使用
(3)一瓶上述84消毒液理论上能吸收空气中
(4)84消毒液与稀硫酸混合使用可增强消毒能力,请用化学方程式解释其原因
(5)在配制过程中,下列操作中能使所配溶液的浓度偏高的有
①用量筒量取98%的硫酸时俯视
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤定容时,俯视刻度线
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
更新时间:2023-08-26 06:50:29
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】将32.64 g铜与140 mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为11.2 L。请回答下列问题:
(1)写出铜与稀硝酸反应的离子方程式为___________ ,
(2) NO的体积为___________ L,
(3) 待产生的气体全部释放后,向溶液中加入V mL a mol/ L的NaOH溶液,恰好使溶液中Cu2+全部转化成沉淀,则原硝酸溶液的浓度为___________ mol /L。(用相应的数字和字母表示)
(1)写出铜与稀硝酸反应的离子方程式为
(2) NO的体积为
(3) 待产生的气体全部释放后,向溶液中加入V mL a mol/ L的NaOH溶液,恰好使溶液中Cu2+全部转化成沉淀,则原硝酸溶液的浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】有碳酸钠、碳酸氢钠的混合物38.0克,均分为两份,①一份将它们加热到质量不再减轻,冷却后称量为15.9克。②另一份溶于蒸馏水,滴加足量的氢氧化钡溶液至不再产生沉淀。求:
(1)原混合物中碳酸氢钠的质量有_______ 克。
(2)第二份溶液中滴加足量的氢氧化钡至不再产生沉淀,则沉淀的质量为_______ 克。
(1)原混合物中碳酸氢钠的质量有
(2)第二份溶液中滴加足量的氢氧化钡至不再产生沉淀,则沉淀的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】取Na2CO3和NaOH的混合液100mL,先向其中滴加Ba(OH)2溶液至不产生沉淀为止,再向其中滴加稀盐酸至沉淀消失,产生的沉淀的质量与消耗盐酸的体积如图所示:
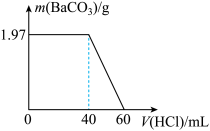
(1)原混合液中Na2CO3与NaOH的物质的量浓度比为___ 。
(2)稀盐酸的物质的量浓度为___ mol·L-1。

(1)原混合液中Na2CO3与NaOH的物质的量浓度比为
(2)稀盐酸的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】将12.6g无水亚硫酸钠固体加入100mL 8mol·L-1的硫酸中以制取SO2气体,反应完全后,若溶液中含+4价硫元素的物质的总浓度为0.2mol·L-1,假定溶液体积不变,忽略容器及导管中的气体体积,求:
(1)溶液中硫元素的质量_________ 。
(2)收集到SO2气体_________ 毫升(标准状况下)?
(1)溶液中硫元素的质量
(2)收集到SO2气体
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】某溶液含 Mg2+、Al3+,向其中滴加a mLC1mol·L—1NaOH之后,改成滴加C2mol·L—1H2SO4溶液,所得沉淀Y(mol)与所加试剂总体积V(mL)间的关系如下图所示。据此,回答下列问题:
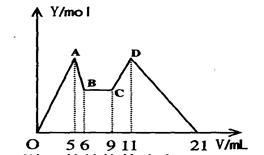
(1)C-D过程中的离子方程式________________________ ;
(2)n(Mg2+)/ n(Al3+) =______________ ;
(3)C1/C2=______________ ;
(4)所加入NaOH溶液的体积a=______________ mL。

(1)C-D过程中的离子方程式
(2)n(Mg2+)/ n(Al3+) =
(3)C1/C2=
(4)所加入NaOH溶液的体积a=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】(1)4gNaOH固体溶于一定量的水中,配成500mL溶液,该溶液的物质的量浓度为__ 。向该溶液中加入__ mL浓度为0.2mol/L的稀硫酸,恰好完全中和。若等量稀硫酸中撒入足量小苏打粉末,能够产生标准状况下的气体__ mL(不考虑气体的溶解)。
(2)在100g浓度为cmol/L、密度为ρg/cm3的硫酸中加入一定量的水稀释成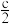 mol/L的硫酸,则加入水的体积
mol/L的硫酸,则加入水的体积__ 100mL(填“=”、“>”或“<”)。
(3)将4.6g钠单质投入__ g水中,形成每50个水分子中将有一个钠离子的溶液,该溶液的质量分数为__ %(保留两位小数)。
(2)在100g浓度为cmol/L、密度为ρg/cm3的硫酸中加入一定量的水稀释成
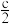 mol/L的硫酸,则加入水的体积
mol/L的硫酸,则加入水的体积(3)将4.6g钠单质投入
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)3.6gH2O的物质的量是____ mol,含有___ 个水分子,含有__ molH。
(2)标准状况下44.8LHCl气体的物质的量是____ mol,全部溶于水形成1L盐酸溶液,此盐酸的物质的量浓度是____ mol•L-1。
(3)3.01×1022个OH-的物质的量为___ mol,质量为___ g,含有质子的物质的量为___ mol,含有电子的物质的量为____ mol,这些OH-与____ molNH3的质量相同。
(4)用20gNaOH配成250mL溶液,它的物质的量浓度为___ mol•L-1。取出5mL该溶液,它的物质的量浓度为__ mol•L-1,再加水稀释至100mL,则稀释后溶液的物质的量浓度为___ mol•L-1。
(5)18.6gNa2R含0.6molNa+,则Na2R的摩尔质量为___ ,R的相对原子质量为___ 。
(2)标准状况下44.8LHCl气体的物质的量是
(3)3.01×1022个OH-的物质的量为
(4)用20gNaOH配成250mL溶液,它的物质的量浓度为
(5)18.6gNa2R含0.6molNa+,则Na2R的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】I.科学研究小组的同学为测定某Na2CO3和NaHCO3混合物中Na2CO3的质量分数,进行了下列相关实验。其实验流程如下:
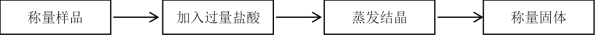
(1)该实验需要用到1.50 mol/L的稀盐酸500 mL,但实验室只有12.0 mol/L的浓盐酸。则配制稀盐酸所用浓盐酸_______ mL。
(2)若实验中测得样品质量为46.4 g,固体质量为40.95 g,请列式计算碳酸钠的质量分数_______ (保留3位有效数字)。
II.为测定某氯化亚铜样品中CuCl的含量,某同学设计如下实验:准确称取氯化亚铜样品m g,将其置于过量的FeCl3溶液中,待固体完全溶解后,加入适量稀硫酸,用a mol/L的K2Cr2O7溶液氧化反应生成的Fe2+,消耗K2Cr2O7溶液b mL,反应中 被还原为Cr3+。请列式计算样品中CuCl的质量分数
被还原为Cr3+。请列式计算样品中CuCl的质量分数_______ 。
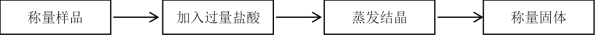
(1)该实验需要用到1.50 mol/L的稀盐酸500 mL,但实验室只有12.0 mol/L的浓盐酸。则配制稀盐酸所用浓盐酸
(2)若实验中测得样品质量为46.4 g,固体质量为40.95 g,请列式计算碳酸钠的质量分数
II.为测定某氯化亚铜样品中CuCl的含量,某同学设计如下实验:准确称取氯化亚铜样品m g,将其置于过量的FeCl3溶液中,待固体完全溶解后,加入适量稀硫酸,用a mol/L的K2Cr2O7溶液氧化反应生成的Fe2+,消耗K2Cr2O7溶液b mL,反应中
 被还原为Cr3+。请列式计算样品中CuCl的质量分数
被还原为Cr3+。请列式计算样品中CuCl的质量分数
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】根据所学知识回答下列问题:
(1)常温下铝具有较强的抗腐蚀性,主要原因是___________ 。
(2)标准状况下, 氨气与同条件下
氨气与同条件下___________ gH2S含有相同的氢原子数。
(3)标准状况下, 由
由 和
和 组成的混合气体的质量为12g,则
组成的混合气体的质量为12g,则 和
和 的物质的量之比是
的物质的量之比是___________ 。
(4)将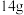 由
由 和
和 组成的混合物加入足量的水中充分反应后,生成标准状况下
组成的混合物加入足量的水中充分反应后,生成标准状况下 气体所得溶液的体积为
气体所得溶液的体积为 。则原混合物中
。则原混合物中 的物质的量为
的物质的量为___________  ;所得溶液中溶质的物质的量浓度为
;所得溶液中溶质的物质的量浓度为___________  。
。
(5)实验室籥配制 溶液,实际应称量绿矾(
溶液,实际应称量绿矾( )的质量为
)的质量为___________ g。配制时,其正确的操作顺序是___________ (填标号,每个标号只能用一次)。
①用 水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
②将准确称量的绿矾倒入烧杯中,再加适量水溶解
③将已冷却的溶液沿玻璃棒注入容量瓶中
④将容量瓶盖紧振荡,反复上下颠倒,摇匀
⑤改用胶头滴管加水,使溶液凹面恰好与刻度线相切
⑥继续往容量瓶内小心加水,直到液面接近刻度线下 处
处
(1)常温下铝具有较强的抗腐蚀性,主要原因是
(2)标准状况下,
 氨气与同条件下
氨气与同条件下(3)标准状况下,
 由
由 和
和 组成的混合气体的质量为12g,则
组成的混合气体的质量为12g,则 和
和 的物质的量之比是
的物质的量之比是(4)将
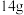 由
由 和
和 组成的混合物加入足量的水中充分反应后,生成标准状况下
组成的混合物加入足量的水中充分反应后,生成标准状况下 气体所得溶液的体积为
气体所得溶液的体积为 。则原混合物中
。则原混合物中 的物质的量为
的物质的量为 ;所得溶液中溶质的物质的量浓度为
;所得溶液中溶质的物质的量浓度为 。
。(5)实验室籥配制
 溶液,实际应称量绿矾(
溶液,实际应称量绿矾( )的质量为
)的质量为①用
 水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡②将准确称量的绿矾倒入烧杯中,再加适量水溶解
③将已冷却的溶液沿玻璃棒注入容量瓶中
④将容量瓶盖紧振荡,反复上下颠倒,摇匀
⑤改用胶头滴管加水,使溶液凹面恰好与刻度线相切
⑥继续往容量瓶内小心加水,直到液面接近刻度线下
 处
处
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】Ba2+是一种重金属离子,有一环境监测小组欲利用Na2S2O3、KI、K2Cr2O7等试剂测定某工厂废水中Ba2+的物质的量浓度。请回答下列问题:
(1)现需配制250 mL 0.100 mol·L-1的标准Na2S2O3溶液,所需要的玻璃仪器除量筒、250 mL容量瓶、玻璃棒外,还需要________ 。
(2)需准确称取Na2S2O3固体的质量为________ g。
(3)另取废水50.00 mL,控制适当的酸度,加入足量的K2Cr2O7溶液,得到BaCrO4沉淀;沉淀经洗涤、过滤后,用适量的稀盐酸溶解,此时CrO 全部转化为Cr2O
全部转化为Cr2O ;再加入过量KI溶液进行反应,然后在反应液中滴加上述标准Na2S2O3溶液,反应完全时,消耗
;再加入过量KI溶液进行反应,然后在反应液中滴加上述标准Na2S2O3溶液,反应完全时,消耗
Na2S2O3溶液36.00 mL,已知有关反应的离子方程式为①Cr2O +6I-+14H+=2Cr3++3I2+7H2O;②2S2O
+6I-+14H+=2Cr3++3I2+7H2O;②2S2O +I2=2I-+S4O
+I2=2I-+S4O ,则该工厂废水中Ba2+的物质的量浓度为
,则该工厂废水中Ba2+的物质的量浓度为________ 。
(1)现需配制250 mL 0.100 mol·L-1的标准Na2S2O3溶液,所需要的玻璃仪器除量筒、250 mL容量瓶、玻璃棒外,还需要
(2)需准确称取Na2S2O3固体的质量为
(3)另取废水50.00 mL,控制适当的酸度,加入足量的K2Cr2O7溶液,得到BaCrO4沉淀;沉淀经洗涤、过滤后,用适量的稀盐酸溶解,此时CrO
 全部转化为Cr2O
全部转化为Cr2O ;再加入过量KI溶液进行反应,然后在反应液中滴加上述标准Na2S2O3溶液,反应完全时,消耗
;再加入过量KI溶液进行反应,然后在反应液中滴加上述标准Na2S2O3溶液,反应完全时,消耗Na2S2O3溶液36.00 mL,已知有关反应的离子方程式为①Cr2O
 +6I-+14H+=2Cr3++3I2+7H2O;②2S2O
+6I-+14H+=2Cr3++3I2+7H2O;②2S2O +I2=2I-+S4O
+I2=2I-+S4O ,则该工厂废水中Ba2+的物质的量浓度为
,则该工厂废水中Ba2+的物质的量浓度为
您最近一年使用:0次