1 . 将35.8gNa2CO3和NaHCO3的固体混合物溶于足量水中,向其中逐滴加入1mol·L-1的盐酸至不再产生气体为止,测得共产生CO28.96L(标准状况)(气体溶解忽略不计)。回答下列问题:
(1)原混合物中Na2CO3为___________ g。
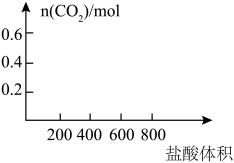
(2)若以滴加盐酸的体积为V(mL),产生气体的物质的量为n(mol),建立n=f(V)的函数关系,将V在不同取值范围时,n=f(V)的关系式填入下表并作图。
___________
(1)原混合物中Na2CO3为
(2)若以滴加盐酸的体积为V(mL),产生气体的物质的量为n(mol),建立n=f(V)的函数关系,将V在不同取值范围时,n=f(V)的关系式填入下表并作图。
| V的取值范围 | n=f(V) |
您最近一年使用:0次
2 . 在标准状况下,将336LHCl气体溶解于1L水中,所得盐酸溶液的密度为1.18g/cm3.试计算这种盐酸溶液中溶质的物质的量浓度为___________ 。
您最近一年使用:0次
名校
3 . 硝酸与金属的反应
①先将5.6克铁粉与200mL一定浓度的稀硝酸混合使其充分反应,固体完全溶解,并收集到气体VL(已折算为标准状况);
②往反应后的溶液中加入一定量铜粉,铜粉恰好完全溶解,且溶解过程中无气泡产生;
③继续往溶液中加入足量NaOH溶液并过滤,将滤渣充分加热后得共到12g固体X.
回答下列问题:
(1)①中产生的气体为______ ,其体积为______ (标况下),写出产生该气体的化学方程式______ 。
(2)铜粉的质量为______ 写出铜粉溶解的离子方程式______ 。
(3)固体X中主要成分的物质的量之比为______ 。
①先将5.6克铁粉与200mL一定浓度的稀硝酸混合使其充分反应,固体完全溶解,并收集到气体VL(已折算为标准状况);
②往反应后的溶液中加入一定量铜粉,铜粉恰好完全溶解,且溶解过程中无气泡产生;
③继续往溶液中加入足量NaOH溶液并过滤,将滤渣充分加热后得共到12g固体X.
回答下列问题:
(1)①中产生的气体为
(2)铜粉的质量为
(3)固体X中主要成分的物质的量之比为
您最近一年使用:0次
解题方法
4 . Ⅰ、
(1)室温下,试计算:
①pH=4的亚硫酸溶液中,c(H+)H2O=___________ 。
②pH=2的盐酸加水稀释到1000倍,溶液的pH=___________ 。
Ⅱ、某温度下的水溶液中,c(H+)=10-xmol·L-1,c(OH-)=10-ymol·L-1。x与y的关系如图所示:

(2)该温度下水的离子积为___________ (填具体数值);该温度___________ (填“高于”“低于”或“等于”)常温。
(3)该温度下0.01mol·L-1NaOH溶液的pH为___________ 。
(4)除了用pH外,科学家还建议用酸度(AG)来表示溶液的酸碱性:AG=lg 。则该温度下,0.01mol·L-1盐酸的酸度AG=
。则该温度下,0.01mol·L-1盐酸的酸度AG=___________ 。
(1)室温下,试计算:
①pH=4的亚硫酸溶液中,c(H+)H2O=
②pH=2的盐酸加水稀释到1000倍,溶液的pH=
Ⅱ、某温度下的水溶液中,c(H+)=10-xmol·L-1,c(OH-)=10-ymol·L-1。x与y的关系如图所示:

(2)该温度下水的离子积为
(3)该温度下0.01mol·L-1NaOH溶液的pH为
(4)除了用pH外,科学家还建议用酸度(AG)来表示溶液的酸碱性:AG=lg
 。则该温度下,0.01mol·L-1盐酸的酸度AG=
。则该温度下,0.01mol·L-1盐酸的酸度AG=
您最近一年使用:0次
5 . 制取SO2的方程式为: ,将12.6g Na2SO3与足量浓硫酸反应,求制得标准状况下SO2的体积
,将12.6g Na2SO3与足量浓硫酸反应,求制得标准状况下SO2的体积
您最近一年使用:0次
6 . 将10.6gNa2CO3粉末投入500mL一定浓度的硫酸溶液中,恰好完全反应。求:
(1)标准状况下收集到CO2气体体积为___________ 。
(2)硫酸溶液的物质的量浓度为___________ 。
(1)标准状况下收集到CO2气体体积为
(2)硫酸溶液的物质的量浓度为
您最近一年使用:0次
7 . 回答下列问题:
素材Ⅰ.“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为: ,结合素材回答问题(1)~(3):
,结合素材回答问题(1)~(3):
(1)该反应中 的摩尔质量是
的摩尔质量是________ 。
(2)28g铁粉中含有的Fe原子数是_______ 。
(3)若28g铁粉完全反应,析出Cu单质的物质的量为_______ 。
素材Ⅱ.宋代《洗冤集录》中记载有“银针探毒”,其原理是: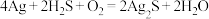 ,结合素材回答问题(4)~(5):
,结合素材回答问题(4)~(5):
(4)在相同条件下体积相同的 和
和 两种气体含有的原子数之比为
两种气体含有的原子数之比为_______ 。
(5)在0℃、101kPa条件下,11.2L氧气完全反应,消耗的 的体积是
的体积是_______ 。
素材Ⅲ.向空气中排放 会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
(6)该雨水中氢离子的浓度
________  。
。
素材Ⅰ.“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为:
 ,结合素材回答问题(1)~(3):
,结合素材回答问题(1)~(3):(1)该反应中
 的摩尔质量是
的摩尔质量是(2)28g铁粉中含有的Fe原子数是
(3)若28g铁粉完全反应,析出Cu单质的物质的量为
素材Ⅱ.宋代《洗冤集录》中记载有“银针探毒”,其原理是:
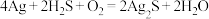 ,结合素材回答问题(4)~(5):
,结合素材回答问题(4)~(5):(4)在相同条件下体积相同的
 和
和 两种气体含有的原子数之比为
两种气体含有的原子数之比为(5)在0℃、101kPa条件下,11.2L氧气完全反应,消耗的
 的体积是
的体积是素材Ⅲ.向空气中排放
 会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:离子 |
|
|
|
|
|
浓度( | 0.06 | 0.08 | 0.02 | 0.04 | a |

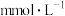 。
。
您最近一年使用:0次
名校
解题方法
8 . 填空
(1)0.3molD2O中所含中子数与_____ 克H2O分子中所含电子数相等。
(2)19g某二价金属氯化物(ACl2)中含有0.4molCl-,则ACl2的摩尔质量是_____ ;A的相对原子质量是_____ 。
(3)在无土栽培中,配制1L内含0.5mol 、0.64molCl-、0.56molK+、
、0.64molCl-、0.56molK+、_____ mol 的某中性营养液,若用KCl、NH4Cl、
的某中性营养液,若用KCl、NH4Cl、_____ 配制,则需这三种固体的物质的量分别为0.56mol、0.08mol、_____ mol。
(4)现有一定条件下CO2和H2O的混合气体37.5g,通过足量的Na2O2固体后,剩余的气体在标准状况的体积为11.2L,则:混合气体中CO2的物质的量为_____ mol,混合气体中H2O的质量为_____ g。
(5)Na2O和Na2O2的混合物14g和足量的水反应,得到300mL溶液,其中含溶质16g。原混合物中Na2O和Na2O2的质量分别多少_____ 。
(1)0.3molD2O中所含中子数与
(2)19g某二价金属氯化物(ACl2)中含有0.4molCl-,则ACl2的摩尔质量是
(3)在无土栽培中,配制1L内含0.5mol
 、0.64molCl-、0.56molK+、
、0.64molCl-、0.56molK+、 的某中性营养液,若用KCl、NH4Cl、
的某中性营养液,若用KCl、NH4Cl、(4)现有一定条件下CO2和H2O的混合气体37.5g,通过足量的Na2O2固体后,剩余的气体在标准状况的体积为11.2L,则:混合气体中CO2的物质的量为
(5)Na2O和Na2O2的混合物14g和足量的水反应,得到300mL溶液,其中含溶质16g。原混合物中Na2O和Na2O2的质量分别多少
您最近一年使用:0次
9 . 取1L的 和
和 混合物溶液与过量盐酸反应,生成2.016L
混合物溶液与过量盐酸反应,生成2.016L (标况下),然后加入足量的
(标况下),然后加入足量的 溶液,得到沉淀的质量为2.33g。
溶液,得到沉淀的质量为2.33g。
(1)计算混合物溶液中 的物质的量浓度
的物质的量浓度_______ 。
(2) 的物质的量为
的物质的量为_______ 。
 和
和 混合物溶液与过量盐酸反应,生成2.016L
混合物溶液与过量盐酸反应,生成2.016L (标况下),然后加入足量的
(标况下),然后加入足量的 溶液,得到沉淀的质量为2.33g。
溶液,得到沉淀的质量为2.33g。(1)计算混合物溶液中
 的物质的量浓度
的物质的量浓度(2)
 的物质的量为
的物质的量为
您最近一年使用:0次
名校
10 . 填空
(1)3.01×1023个H2O的物质的量为___________ mol,其中,所含电子的数目为___________ 。
(2)在同温同压下,等质量的CO和CO2,其体积之比为___________ 。
(3)33.3g某金属氯化物MCl2中含有0.6molCl-,则该氯化物的摩尔质量为___________ 。
(4)某硫酸铝溶液中所含铝离子浓度为3mol/L,则硫酸根离子浓度为___________ 。
(5)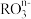 中,共有x个核外电子,R原子的质量数为A,则R原子核内含有的中子数目是
中,共有x个核外电子,R原子的质量数为A,则R原子核内含有的中子数目是___________ 。
(1)3.01×1023个H2O的物质的量为
(2)在同温同压下,等质量的CO和CO2,其体积之比为
(3)33.3g某金属氯化物MCl2中含有0.6molCl-,则该氯化物的摩尔质量为
(4)某硫酸铝溶液中所含铝离子浓度为3mol/L,则硫酸根离子浓度为
(5)
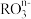 中,共有x个核外电子,R原子的质量数为A,则R原子核内含有的中子数目是
中,共有x个核外电子,R原子的质量数为A,则R原子核内含有的中子数目是
您最近一年使用:0次








