名校
1 . 填空
(1)3.01×1023个H2O的物质的量为___________ mol,其中,所含电子的数目为___________ 。
(2)在同温同压下,等质量的CO和CO2,其体积之比为___________ 。
(3)33.3g某金属氯化物MCl2中含有0.6molCl-,则该氯化物的摩尔质量为___________ 。
(4)某硫酸铝溶液中所含铝离子浓度为3mol/L,则硫酸根离子浓度为___________ 。
(5)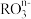 中,共有x个核外电子,R原子的质量数为A,则R原子核内含有的中子数目是
中,共有x个核外电子,R原子的质量数为A,则R原子核内含有的中子数目是___________ 。
(1)3.01×1023个H2O的物质的量为
(2)在同温同压下,等质量的CO和CO2,其体积之比为
(3)33.3g某金属氯化物MCl2中含有0.6molCl-,则该氯化物的摩尔质量为
(4)某硫酸铝溶液中所含铝离子浓度为3mol/L,则硫酸根离子浓度为
(5)
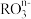 中,共有x个核外电子,R原子的质量数为A,则R原子核内含有的中子数目是
中,共有x个核外电子,R原子的质量数为A,则R原子核内含有的中子数目是
您最近一年使用:0次
解题方法
2 . 200ml 0.2mol/L的氢氧化钠溶液在标准状况下能吸收多少升的二氧化碳?___________
您最近一年使用:0次
解题方法
3 . 完成下列问题
(1)3.01×1023个氯气分子的物质的量是_______ ,质量为_______ ;
(2)1.5 mol Na2SO4·10H2O中所含的Na+的物质的量是_______ ,所含的SO 的物质的量是
的物质的量是_______ ,所含H2O的数目是_______ ;
(3)一定量的Na2CO3中,碳原子和氧原子的物质的量之比为_______ ;
(4)0.5 mol NaOH中含有电子的物质的量是_______ ,在_______ mol Na2CO3中所含Na+数目与上述0.5 mol NaOH所含Na+数目相等。
(5)12.4gNa2R含0.4molNa+,则Na2R的摩尔质量为_______ ,R的相对原子质量为_______ ,含R的质量为1.6g的Na2R,其物质的量为_______ ;
(6)标准状况下,1.92g某气体的体积为672mL,则此气体的相对分子质量为_______ ;
(7)在标准状况下,CO和CO2的混合气体共39.2L,质量为61g,则两种气体的物质的量之和为_______ mol,CO占总质量的_______ %(结果取整数)
(1)3.01×1023个氯气分子的物质的量是
(2)1.5 mol Na2SO4·10H2O中所含的Na+的物质的量是
 的物质的量是
的物质的量是(3)一定量的Na2CO3中,碳原子和氧原子的物质的量之比为
(4)0.5 mol NaOH中含有电子的物质的量是
(5)12.4gNa2R含0.4molNa+,则Na2R的摩尔质量为
(6)标准状况下,1.92g某气体的体积为672mL,则此气体的相对分子质量为
(7)在标准状况下,CO和CO2的混合气体共39.2L,质量为61g,则两种气体的物质的量之和为
您最近一年使用:0次
名校
解题方法
4 . 完成下列问题
(1)8 g CH4在标准状况下所占的体积约为_______ L。
(2)20g重水(D2O)中所含中子数目为_______ 。
(3)10.8g R2O5中氧原子数目为3.01×1023 ,则元素R的相对原子质量为_______ 。
(4)向10.0mL1.00mol·L-1 Na2CO3溶液加水稀释至100mL溶液,此时溶液中Na+的物质的量浓度为_______ 。
(5)实验室常用邻苯二甲酸氢钾(KHC8H4O4)来标定氢氧化钠溶液的浓度,其操作过程为:准确称取4.080g邻苯二甲酸氢钾,加水配成溶液,向溶液中加入1~2滴指示剂,用氢氧化钠溶液滴定至终点,消耗氢氧化钠溶液19.60mL。该氢氧化钠溶液的物质的量浓度为_______ 。(已知:KHC8H4O4+NaOH=KNaC8H4O4+H2O)
(6)100g质量分数为46%的酒精(CH3CH2OH)溶液中氧原子的物质的量为_______ 。
(1)8 g CH4在标准状况下所占的体积约为
(2)20g重水(D2O)中所含中子数目为
(3)10.8g R2O5中氧原子数目为3.01×1023 ,则元素R的相对原子质量为
(4)向10.0mL1.00mol·L-1 Na2CO3溶液加水稀释至100mL溶液,此时溶液中Na+的物质的量浓度为
(5)实验室常用邻苯二甲酸氢钾(KHC8H4O4)来标定氢氧化钠溶液的浓度,其操作过程为:准确称取4.080g邻苯二甲酸氢钾,加水配成溶液,向溶液中加入1~2滴指示剂,用氢氧化钠溶液滴定至终点,消耗氢氧化钠溶液19.60mL。该氢氧化钠溶液的物质的量浓度为
(6)100g质量分数为46%的酒精(CH3CH2OH)溶液中氧原子的物质的量为
您最近一年使用:0次
5 . 已知可逆反应CO(g)+H2O(g) CO2(g)+H2(g),平衡常数为K。
CO2(g)+H2(g),平衡常数为K。
(1)557℃时,若起始浓度:CO为1mol·L-1,H2O为1.5mol·L-1,平衡时CO转化率为60%,则H2O的转化率为___________ ;K值为___________ 。
(2)557℃时,若起始浓度改为:CO为1mol·L-1,H2O为3mol·L-1,平衡时H2O的转化率为___________ 。
 CO2(g)+H2(g),平衡常数为K。
CO2(g)+H2(g),平衡常数为K。(1)557℃时,若起始浓度:CO为1mol·L-1,H2O为1.5mol·L-1,平衡时CO转化率为60%,则H2O的转化率为
(2)557℃时,若起始浓度改为:CO为1mol·L-1,H2O为3mol·L-1,平衡时H2O的转化率为
您最近一年使用:0次
2022-08-27更新
|
624次组卷
|
5卷引用:福建省莆田第十五中学2019-2020学年高二上学期期末考试化学试题
福建省莆田第十五中学2019-2020学年高二上学期期末考试化学试题(已下线)2.2.2 化学平衡常数(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)2.2.1 化学平衡常数-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第09讲 化学平衡常数(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)河北省邯郸市魏县2022-2023学年高二上学期期末考试化学试题
21-22高一·全国·课后作业
6 . 氯化钠是一种重要的化工原料,电解氯化钠溶液可制得氯气、氢氧化钠等物质,发生的化学反应如下:2NaCl + 2H2O Cl2 ↑+ H2 ↑+ 2NaOH。现取一定质量的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电。生成氯气的质量与时间的关系如图所示。请计算:
Cl2 ↑+ H2 ↑+ 2NaOH。现取一定质量的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电。生成氯气的质量与时间的关系如图所示。请计算:
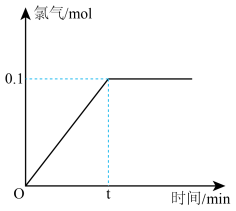
(1)参加反应的氯化钠是_______ 克?
(2)生成氢气_______ 克?生成NaOH_______ mol?
 Cl2 ↑+ H2 ↑+ 2NaOH。现取一定质量的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电。生成氯气的质量与时间的关系如图所示。请计算:
Cl2 ↑+ H2 ↑+ 2NaOH。现取一定质量的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电。生成氯气的质量与时间的关系如图所示。请计算:
(1)参加反应的氯化钠是
(2)生成氢气
您最近一年使用:0次
2021-07-27更新
|
494次组卷
|
6卷引用:福建省莆田第十五中学2021-2022学年高一上学期期末考试化学试题
福建省莆田第十五中学2021-2022学年高一上学期期末考试化学试题(已下线)1.2.1 物质的量(2)(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)(已下线)周末培优5 物质的量应用于化学方程式的计算专练-2021-2022学年高一化学课后培优练(人教版2019必修第一册)(已下线)第14讲 化学方程式的计算-【暑假自学课】2022年新高一化学暑假精品课(沪科版2020必修第一册)作业(八) 物质的量在化学反应中的应用(已下线)【定心卷】3.2.2 物质的量在化学方程式计算中的应用随堂练习-人教版2023-2024学年必修第一册
名校
7 . 将24.0gNaOH固体溶于水配成100mL溶液,其密度为1.20g•mL-1。
(1)该溶液中NaOH的质量分数为_______ ,Na+的数目为_______ 。
(2)从该溶液中取出10.0mL,其中NaOH的物质的量浓度为_______ mol•L-1,含NaOH的物质的量为_______ mol。
(3)将取出的10mL溶液加水稀释到50mL,稀释后溶液中Na+的物质的量浓度为___ mol•L-1,含NaOH的质量为____ g。
(1)该溶液中NaOH的质量分数为
(2)从该溶液中取出10.0mL,其中NaOH的物质的量浓度为
(3)将取出的10mL溶液加水稀释到50mL,稀释后溶液中Na+的物质的量浓度为
您最近一年使用:0次
8 . 已知Ksp(AgCl)=1.8×10-10,将足量的AgCl加入0.3 mol·L-1的MgCl2溶液中,c(Ag+)最大是_______ 。
您最近一年使用:0次
解题方法
9 . 酸性锌锰干电池是一种一次性电池,外壳为金属锌,用废电池的锌皮制备ZnSO4·7H2O的过程中,需去除少量杂质铁,其方法是:加稀硫酸和H2O2溶解,铁变为_______ ,加碱调节至pH为_______ 时,铁刚好完全沉淀(离子浓度小于1×10-5mol/L时,即可认为该离子沉淀完全);继续加碱调节至pH为_______ 时,锌开始沉淀(假定Zn2+浓度为0.1mol/L)。若上述过程不加H2O2后果是_______ ,原因是 _______ 。
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
您最近一年使用:0次
10 . 过量的铁粉与稀硝酸反应的方程式为:3Fe +8HNO3 =3Fe(NO3)2+ 2NO↑+4H2O
(1)标出电子转移的方向和数目______ 。
(2)在标准状况下,当生成22.4LNO气体时,有_______ gFe参加反应,转移电子的物质的量为_______ 。
(1)标出电子转移的方向和数目
(2)在标准状况下,当生成22.4LNO气体时,有
您最近一年使用:0次



