1 . 回答下列问题:
(1)含有0.4molAl3+的Al2(SO4)3中,所含有的SO 的物质的量为
的物质的量为________ 。
(2)已知16gA和20gB恰好完全反应生成0.04mol的C和31.76g的D,则C的摩尔质量为_______ 。
(3)如果ag某气体中的分子数为b,则cg该气体在标准状况下的体积为_______ (设NA为阿伏加德罗常数)。
(4)把VL含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含amolNaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含bmolBaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为________ 。
(1)含有0.4molAl3+的Al2(SO4)3中,所含有的SO
 的物质的量为
的物质的量为(2)已知16gA和20gB恰好完全反应生成0.04mol的C和31.76g的D,则C的摩尔质量为
(3)如果ag某气体中的分子数为b,则cg该气体在标准状况下的体积为
(4)把VL含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含amolNaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含bmolBaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为
您最近一年使用:0次
2 . 利用 制甲醇具有重要意义。其过程可能发生的反应如下:
制甲醇具有重要意义。其过程可能发生的反应如下:
反应1: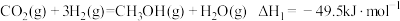
反应2:
反应3: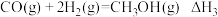
(1)
_______ 
(2)恒容条件下,下列有利于提高 平衡产率的条件是_______。
平衡产率的条件是_______。
(3)控制一定压强,通入 和
和 ,反应
,反应 后,
后, 转化率
转化率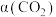 、
、 产率
产率 及
及 产率
产率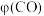 随温度变化曲线如图。
随温度变化曲线如图。
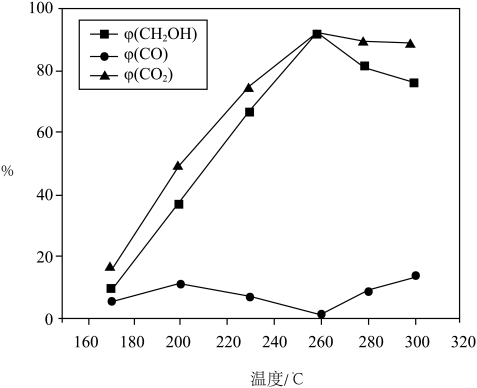
①温度升高, 先升高后降低的原因是
先升高后降低的原因是_______ 。
②260℃时,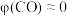 (认为此时只发生反应1),
(认为此时只发生反应1),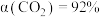 ,气体总体积为
,气体总体积为 ,则该温度下反应1的平衡常数
,则该温度下反应1的平衡常数
_______ (列出代数式即可),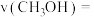
_______ (列出代数式即可)。
③280℃时, ,
, ,则反应2的平衡常数
,则反应2的平衡常数
_______ (列出代数式即可)。
(4)学界关于反应2产生的 能否发生反应3存在争议。科学家利用
能否发生反应3存在争议。科学家利用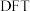 模拟
模拟 催化剂表面合成
催化剂表面合成 的两种不同路径,其决速步及活化能
的两种不同路径,其决速步及活化能 分别如下。
分别如下。
路径1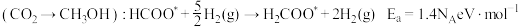
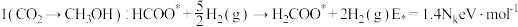 路径2
路径2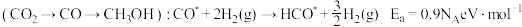
由此分析,200~260℃时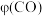 降低的原因是
降低的原因是_______ 。
 制甲醇具有重要意义。其过程可能发生的反应如下:
制甲醇具有重要意义。其过程可能发生的反应如下:反应1:
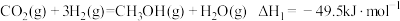
反应2:

反应3:
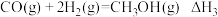
(1)


(2)恒容条件下,下列有利于提高
 平衡产率的条件是_______。
平衡产率的条件是_______。| A.使用催化剂 | B.调整 和 和 的投料比由1∶1至1∶3 的投料比由1∶1至1∶3 |
| C.增大反应物总压 | D.通入稀有气体 |
 和
和 ,反应
,反应 后,
后, 转化率
转化率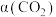 、
、 产率
产率 及
及 产率
产率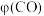 随温度变化曲线如图。
随温度变化曲线如图。
①温度升高,
 先升高后降低的原因是
先升高后降低的原因是②260℃时,
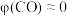 (认为此时只发生反应1),
(认为此时只发生反应1),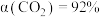 ,气体总体积为
,气体总体积为 ,则该温度下反应1的平衡常数
,则该温度下反应1的平衡常数
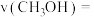
③280℃时,
 ,
, ,则反应2的平衡常数
,则反应2的平衡常数
(4)学界关于反应2产生的
 能否发生反应3存在争议。科学家利用
能否发生反应3存在争议。科学家利用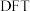 模拟
模拟 催化剂表面合成
催化剂表面合成 的两种不同路径,其决速步及活化能
的两种不同路径,其决速步及活化能 分别如下。
分别如下。路径1
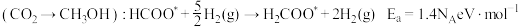
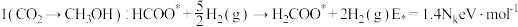 路径2
路径2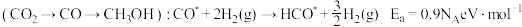
由此分析,200~260℃时
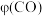 降低的原因是
降低的原因是
您最近一年使用:0次
名校
3 . 回答下列问题:
(1)“春蚕到死丝方尽,蜡炬成灰泪始干”中涉及到蜡烛与 的燃烧反应,反应生成
的燃烧反应,反应生成 和
和 ,该反应一定是______(填序号)。
,该反应一定是______(填序号)。
素材I.“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为: 。结合素材回答问题(2)~(4):
。结合素材回答问题(2)~(4):
(2)该反应中 的摩尔质量是
的摩尔质量是______
(3)28g铁粉中含有的Fe原子数是______ 。
(4)若28g铁粉完全反应,析出Cu单质的质量为______ 。
素材II.宋代《洗冤集录》中记载有“银针探毒”,其原理是: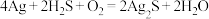 。结合素材回答问题(5)~(6):
。结合素材回答问题(5)~(6):
(5)在相同条件下体积相同的 和
和 两种气体分子数之比为
两种气体分子数之比为______ 。
(6)在0℃、101kPa条件下,11.2L氧气完全反应,消耗的 的体积是
的体积是______ 。
素材III.我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为: 。结合素材回答问题(7)~(8):
。结合素材回答问题(7)~(8):
(7)该反应中,化合价升高的元素是______ (填元素符号)。
(8)该反应中,作为氧化剂的物质是______ (填化学式)。
(9)向空气中排放 会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
该雨水中氢离子的浓度a=______ 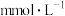 。
。
(1)“春蚕到死丝方尽,蜡炬成灰泪始干”中涉及到蜡烛与
 的燃烧反应,反应生成
的燃烧反应,反应生成 和
和 ,该反应一定是______(填序号)。
,该反应一定是______(填序号)。| A.离子反应 | B.分解反应 | C.氧化还原反应 | D.置换反应 |
素材I.“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为:
 。结合素材回答问题(2)~(4):
。结合素材回答问题(2)~(4):(2)该反应中
 的摩尔质量是
的摩尔质量是(3)28g铁粉中含有的Fe原子数是
(4)若28g铁粉完全反应,析出Cu单质的质量为
素材II.宋代《洗冤集录》中记载有“银针探毒”,其原理是:
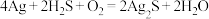 。结合素材回答问题(5)~(6):
。结合素材回答问题(5)~(6):(5)在相同条件下体积相同的
 和
和 两种气体分子数之比为
两种气体分子数之比为(6)在0℃、101kPa条件下,11.2L氧气完全反应,消耗的
 的体积是
的体积是素材III.我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为:
 。结合素材回答问题(7)~(8):
。结合素材回答问题(7)~(8):(7)该反应中,化合价升高的元素是
(8)该反应中,作为氧化剂的物质是
(9)向空气中排放
 会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:离子 |
|
|
|
|
|
浓度( | 0.06 | 0.08 | 0.02 | 0.04 | a |
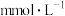 。
。
您最近一年使用:0次
2022-12-13更新
|
198次组卷
|
2卷引用:福建省厦门市第十中学2022-2023学年高一上学期期中考试化学试题
名校
4 . C、N、O、S、H、Na都是中学化学中常见的元素。按要求完成下列填空。
(1)2molC2H6O分子中含_______ mol碳原子、_______ 个氢原子。
(2)0.5NA个H2SO4分子的质量为____ ;0.1molAl2(SO4)3所含SO 的物质的量为
的物质的量为_____ 。
(3)等物质的量的NH3和N2两种气体,所含原子数之比为_______ ,等质量的NH3和N2物质的量之比为_______ 。
(4)24.8gNa2R含Na+0.8mol,则Na2R物质的量为_______ ,摩尔质量为_______ 。
(1)2molC2H6O分子中含
(2)0.5NA个H2SO4分子的质量为
 的物质的量为
的物质的量为(3)等物质的量的NH3和N2两种气体,所含原子数之比为
(4)24.8gNa2R含Na+0.8mol,则Na2R物质的量为
您最近一年使用:0次
名校
5 . 已知反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,现有1.92g铜和足量稀硝酸完全反应,
(1)求产生气体在标准状况下的体积是多少?___________
(2)将所得溶液加水配成200mL溶液,求最终溶液中溶质的物质的量浓度是多少?___________
(1)求产生气体在标准状况下的体积是多少?
(2)将所得溶液加水配成200mL溶液,求最终溶液中溶质的物质的量浓度是多少?
您最近一年使用:0次
名校
解题方法
6 . 某温度时,在容积为5L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间变化的曲线如图所示:(注:A的转化率= ×100%)
×100%)
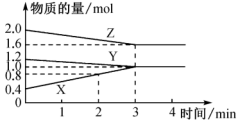
(1)该反应的化学方程式为_______ 。
(2)该反应是从_______ (填“正反应”“逆反应”“正、逆反应同时”)开始的;反应开始至2min末,用X表示的化学反应速率为_______ ,此时Z与Y的物质的量之比为_______ 。
(3)该反应从开始到达到平衡时,Z的转化率与Y的转化率之比为_______ 。
(4)4min时,v(X):v(Y):v(Z)=_______ ;下列哪些数据在反应开始至反应达到平衡时。一直保持不变是_______ (填字母)。
a.压强 b.密度 c.相对平均式量 d.反应物的浓度
 ×100%)
×100%)
(1)该反应的化学方程式为
(2)该反应是从
(3)该反应从开始到达到平衡时,Z的转化率与Y的转化率之比为
(4)4min时,v(X):v(Y):v(Z)=
a.压强 b.密度 c.相对平均式量 d.反应物的浓度
您最近一年使用:0次
2021-06-09更新
|
759次组卷
|
3卷引用:福建省厦门第一中学2021-2022学年高一下学期期中考试化学试题
福建省厦门第一中学2021-2022学年高一下学期期中考试化学试题河北省邯郸市九校联盟2020-2021学年高一下学期期中考试化学试题(已下线)期末综合检测卷01【综合检测】-2020-2021学年高一化学下学期期末专项复习(人教版2019必修第二册)
名校
解题方法
7 . 已知铝与氢氧化钠溶液反应的方程式为:2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑,一定质量的金属铝与足量的NaOH溶液反应,放出3.36L的H2(标准状况下),则该铝的质量为多少克______ ?若反应后溶液体积为500ml,则反应后溶液中Na[Al(OH)4]的物质的量浓度为多少____ ?
您最近一年使用:0次
名校
解题方法
8 . 按要求完成下列热化学方程式:
(1)汽车尾气中的主要污染物是NO和CO,已知:
I 2CO(g)+O2(g) = 2CO2(g) ΔH 1= -566.0kJ•mol-1
II 2NO(g) = N2(g)+O2(g) ΔH 2= -180.8kJ•mol-1;
则将汽车尾气处理成无毒无害产物的热化学方程式为___________ 。
(2)最近意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图,已知298K时断裂1molN≡N键吸收942 kJ热量,生成1molN-N放出167 kJ热量。根据以上信息和数据,则由气态N2生成1 mol气态N4的的热化学方程式为___________ 。

(1)汽车尾气中的主要污染物是NO和CO,已知:
I 2CO(g)+O2(g) = 2CO2(g) ΔH 1= -566.0kJ•mol-1
II 2NO(g) = N2(g)+O2(g) ΔH 2= -180.8kJ•mol-1;
则将汽车尾气处理成无毒无害产物的热化学方程式为
(2)最近意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图,已知298K时断裂1molN≡N键吸收942 kJ热量,生成1molN-N放出167 kJ热量。根据以上信息和数据,则由气态N2生成1 mol气态N4的的热化学方程式为

您最近一年使用:0次
9 . (1)反应2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl中,氧化产物是___________ ,氧化剂和还原剂的物质的量之比为___________ ,依据氧化还原反应规律判断,氧化性强弱为NaClO3___________ Cl2(填>、<或=)。
(2)根据下图中的能量关系,可求得C-H键的键能___________ kJ/mol。
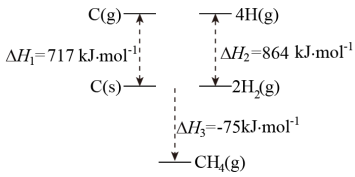
(3)已知:
I. CO(g) + 2H2(g) =CH 3OH(l) △H= −128.6 kJ/mol
II.2CO(g) + O2(g) =2 CO2(g) △H=−566.0 kJ/mol
III.2H2(g) + O2(g) =2 H2O(l) △H=−571.6 kJ/mol
写出 CH3OH燃烧热的热化学方程式:___________ 。
(2)根据下图中的能量关系,可求得C-H键的键能

(3)已知:
I. CO(g) + 2H2(g) =CH 3OH(l) △H= −128.6 kJ/mol
II.2CO(g) + O2(g) =2 CO2(g) △H=−566.0 kJ/mol
III.2H2(g) + O2(g) =2 H2O(l) △H=−571.6 kJ/mol
写出 CH3OH燃烧热的热化学方程式:
您最近一年使用:0次
名校
解题方法
10 . 1774 年,瑞典化学家舍勒发现软锰矿(主要成分是MnO2)和浓盐酸混合加热能制取氯气: MnO2 + 4HCl MnCl2 + Cl2↑+2H2O,现将23.2 g含MnO2的质量分数为75%的软锰矿与足量浓盐酸完全反应(杂质不参加反应)。计算:
MnCl2 + Cl2↑+2H2O,现将23.2 g含MnO2的质量分数为75%的软锰矿与足量浓盐酸完全反应(杂质不参加反应)。计算:
(1)参加反应的MnO2的质量为__________ g。
(2)消耗盐酸溶质的物质的量为_________ mol。
(3)生成的Cl2的体积(标准状况下)_________ L。
 MnCl2 + Cl2↑+2H2O,现将23.2 g含MnO2的质量分数为75%的软锰矿与足量浓盐酸完全反应(杂质不参加反应)。计算:
MnCl2 + Cl2↑+2H2O,现将23.2 g含MnO2的质量分数为75%的软锰矿与足量浓盐酸完全反应(杂质不参加反应)。计算:(1)参加反应的MnO2的质量为
(2)消耗盐酸溶质的物质的量为
(3)生成的Cl2的体积(标准状况下)
您最近一年使用:0次








