(1)反应2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl中,氧化产物是___________ ,氧化剂和还原剂的物质的量之比为___________ ,依据氧化还原反应规律判断,氧化性强弱为NaClO3___________ Cl2(填>、<或=)。
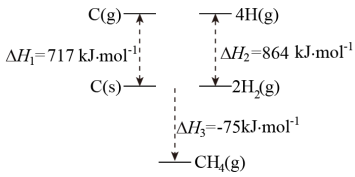
(2)根据下图中的能量关系,可求得C-H键的键能___________ kJ/mol。
(3)已知:
I. CO(g) + 2H2(g) =CH 3OH(l) △H= −128.6 kJ/mol
II.2CO(g) + O2(g) =2 CO2(g) △H=−566.0 kJ/mol
III.2H2(g) + O2(g) =2 H2O(l) △H=−571.6 kJ/mol
写出 CH3OH燃烧热的热化学方程式:___________ 。
(2)根据下图中的能量关系,可求得C-H键的键能

(3)已知:
I. CO(g) + 2H2(g) =CH 3OH(l) △H= −128.6 kJ/mol
II.2CO(g) + O2(g) =2 CO2(g) △H=−566.0 kJ/mol
III.2H2(g) + O2(g) =2 H2O(l) △H=−571.6 kJ/mol
写出 CH3OH燃烧热的热化学方程式:
更新时间:2021-01-13 00:33:22
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】在Fe + 2HCl =FeCl2(氯化亚铁) + H2↑ 反应中。
(1)_______ 元素被氧化,________ 是氧化剂,氧化产物是_________ 。
(2)此反应若转移了12mol的电子,则生成氢气_________ L(标准状况下)。
(1)
(2)此反应若转移了12mol的电子,则生成氢气
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】物质的量是学习化学的基础,按要求完成下列填空。
(1)0.3 g 3H含有_______ mol中子。
(2)0.5 mol H2SO4分子的质量为_______ ;有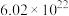 个Al3+的Al2(SO4)3晶体中所含
个Al3+的Al2(SO4)3晶体中所含 的物质的量为
的物质的量为_______ 。
(3)等物质的量的NH3和N2两种气体,所含原子数之比为_______ ,等质量的 和
和 的物质的量之比为
的物质的量之比为_______ 。
(4)24.8 gNa2R含 0.8 mol,则Na2R物质的量为
0.8 mol,则Na2R物质的量为_______ ,Na2R的摩尔质量为_______ 。
(5)根据反应2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,可知当生成2.5 mol Cl2时,被氧化的氯化氢的物质的量为_______ 。
(1)0.3 g 3H含有
(2)0.5 mol H2SO4分子的质量为
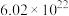 个Al3+的Al2(SO4)3晶体中所含
个Al3+的Al2(SO4)3晶体中所含 的物质的量为
的物质的量为(3)等物质的量的NH3和N2两种气体,所含原子数之比为
 和
和 的物质的量之比为
的物质的量之比为(4)24.8 gNa2R含
 0.8 mol,则Na2R物质的量为
0.8 mol,则Na2R物质的量为(5)根据反应2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,可知当生成2.5 mol Cl2时,被氧化的氯化氢的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】按要求写出相关内容
(1)已知:C(s)+O2(g)=CO2(g) △H= -393.5 kJ/mol
CO(g)+ O2(g)=CO2(g) △H= -283 kJ/mol
O2(g)=CO2(g) △H= -283 kJ/mol
则1 mol C(s)与O2(g)反应生成CO(g)放出的热量为_______ ,反应的热化学方程式为:_______ 。
(2)1 L 1 mol/LH2SO4溶液与2 L 1 mol/LNaOH溶液完全反应,放出114.6 kJ的热量,表示该中和热的热化学方程式为_______ 。
(1)已知:C(s)+O2(g)=CO2(g) △H= -393.5 kJ/mol
CO(g)+
 O2(g)=CO2(g) △H= -283 kJ/mol
O2(g)=CO2(g) △H= -283 kJ/mol则1 mol C(s)与O2(g)反应生成CO(g)放出的热量为
(2)1 L 1 mol/LH2SO4溶液与2 L 1 mol/LNaOH溶液完全反应,放出114.6 kJ的热量,表示该中和热的热化学方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源。
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为______ 。
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关。已知:H2(g)+Cl2(g)=2HCl(g) △H=﹣185kJ/mol,E(H﹣Cl)=432kJ/mol,E(Cl﹣Cl)=243kJ/mol则E(H﹣H)=_____ 。
(3)纳米级Cu2O由于具有优良的催化性能而受到关注.已知:2Cu(s)+ O2(g)═Cu2O(s)△H=﹣169kJ•mol﹣1,C(s)+
O2(g)═Cu2O(s)△H=﹣169kJ•mol﹣1,C(s)+  O2(g)═CO(g)△H=﹣110.5kJ•mol﹣1,2Cu(s)+O2(g)═2CuO(s)△H=﹣314kJ•mol﹣1,则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式
O2(g)═CO(g)△H=﹣110.5kJ•mol﹣1,2Cu(s)+O2(g)═2CuO(s)△H=﹣314kJ•mol﹣1,则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式_____ 。
(4)如图是N2(g)和H2(g)反应生成2molNH3(g)过程中能量变化示意图:
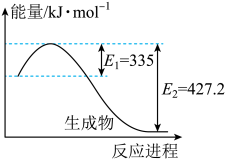
①请计算每生成1molNH3放出热量为:______ 。
②若起始时向容器内充入1molN2和3molH2达平衡后N2的转化率为20%,则反应放出的热量为Q1kJ,则Q1的数值为_________ 。
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关。已知:H2(g)+Cl2(g)=2HCl(g) △H=﹣185kJ/mol,E(H﹣Cl)=432kJ/mol,E(Cl﹣Cl)=243kJ/mol则E(H﹣H)=
(3)纳米级Cu2O由于具有优良的催化性能而受到关注.已知:2Cu(s)+
 O2(g)═Cu2O(s)△H=﹣169kJ•mol﹣1,C(s)+
O2(g)═Cu2O(s)△H=﹣169kJ•mol﹣1,C(s)+  O2(g)═CO(g)△H=﹣110.5kJ•mol﹣1,2Cu(s)+O2(g)═2CuO(s)△H=﹣314kJ•mol﹣1,则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式
O2(g)═CO(g)△H=﹣110.5kJ•mol﹣1,2Cu(s)+O2(g)═2CuO(s)△H=﹣314kJ•mol﹣1,则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式(4)如图是N2(g)和H2(g)反应生成2molNH3(g)过程中能量变化示意图:

①请计算每生成1molNH3放出热量为:
②若起始时向容器内充入1molN2和3molH2达平衡后N2的转化率为20%,则反应放出的热量为Q1kJ,则Q1的数值为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:
①CO(g)+ O2(g)=CO2(g) ΔH=-280.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-280.0 kJ·mol-1
②S(s)+O2(g)=SO2(g) ΔH=-290.0 kJ·mol-1
此反应的热化学方程式是_______ 。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
若用标准状况下22.4L CO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为_ mol,放出的热量为___ kJ(用含有a和b的代数式表示)。
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-540 kJ·mol-1①
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=?②
若1molCH4还原NO2至N2,整个过程中放出的热量为860 kJ,则ΔH2=__ 。
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:
①CO(g)+
 O2(g)=CO2(g) ΔH=-280.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-280.0 kJ·mol-1②S(s)+O2(g)=SO2(g) ΔH=-290.0 kJ·mol-1
此反应的热化学方程式是
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-a kJ·mol-1(a>0)
2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-b kJ·mol-1(b>0)
若用标准状况下22.4L CO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-540 kJ·mol-1①
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=?②
若1molCH4还原NO2至N2,整个过程中放出的热量为860 kJ,则ΔH2=
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】在恒温(500K)、体积为2.0L的密闭容器中通入1.0molN2和1molH2发生合成氨反应,20min后达到平衡,测得反应放出的热量为18.4kJ,混合气体的总物质的量为1.6mol。
(1)从开始反应至达到平衡时,用NH3表示该反应的化学反应速率v(NH3)=______ 。
(2)该反应的热化学方程式为______ 。
(3)若拆开1molH—H键和1molN N键需要的能量分别是436kJ和946kJ,则拆开1molN—H键需要的能量是
N键需要的能量分别是436kJ和946kJ,则拆开1molN—H键需要的能量是______ kJ。
(1)从开始反应至达到平衡时,用NH3表示该反应的化学反应速率v(NH3)=
(2)该反应的热化学方程式为
(3)若拆开1molH—H键和1molN
 N键需要的能量分别是436kJ和946kJ,则拆开1molN—H键需要的能量是
N键需要的能量分别是436kJ和946kJ,则拆开1molN—H键需要的能量是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】按要求回答下列问题:
(1)300℃,硅粉与HCl(g)反应生成1mol SiHCl3气体和H2(g) 时,放出225 kJ的热量。该反应的热化学方程式是_____________________ 。
(2)已知:CuCl2(s)=CuCl(s) + Cl2(g) ΔH1=+83 kJ/mol
Cl2(g) ΔH1=+83 kJ/mol
CuCl(s) + O2(g)=CuO(s) +
O2(g)=CuO(s) +  Cl2(g) ΔH2=-20 kJ/mol
Cl2(g) ΔH2=-20 kJ/mol
CuO(s) + 2HCl(g) = CuCl2(s) + H2O(g) ΔH3=-121 kJ/mol
则:4HCl(g) + O2(g) = 2Cl2(g) + 2H2O(g)的ΔH=_________ kJ/mol。
又知:
推算:断开1 mol H-O键与断开1 mol H-Cl键所需能量相差_______ kJ。
(1)300℃,硅粉与HCl(g)反应生成1mol SiHCl3气体和H2(g) 时,放出225 kJ的热量。该反应的热化学方程式是
(2)已知:CuCl2(s)=CuCl(s) +
 Cl2(g) ΔH1=+83 kJ/mol
Cl2(g) ΔH1=+83 kJ/molCuCl(s) +
 O2(g)=CuO(s) +
O2(g)=CuO(s) +  Cl2(g) ΔH2=-20 kJ/mol
Cl2(g) ΔH2=-20 kJ/molCuO(s) + 2HCl(g) = CuCl2(s) + H2O(g) ΔH3=-121 kJ/mol
则:4HCl(g) + O2(g) = 2Cl2(g) + 2H2O(g)的ΔH=
又知:

推算:断开1 mol H-O键与断开1 mol H-Cl键所需能量相差
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】人民网报道,浙江温岭一河流氨氮超标五倍,河水黑如墨水。氮氧化物污染日益严重,请分析下列有关NO、NO2等的试题,然后填空。
(1)下图所示为N2(g)和O2(g)生成NO(g)过程中的能量变化。

由上图写出N2(g)和O2(g)生成NO(g)的热化学反应方程式____________
(2)下图是1 mol NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式________________________ .

(3)已知:在298K、101kPa下,由稳定的单质生成1mol化合物的反应热叫做该化合物的生成热。如图为氧族元素(除钋外)的氢化物a、b、c、d的生成热数据示意图

①请归纳:非金属元素的气态氢化物的稳定性与氢化物的生成热(ΔH)之间的关系______________________________
②写出硒化氢在298K、101kPa时发生分解反应的热化学反应方程式__________
(1)下图所示为N2(g)和O2(g)生成NO(g)过程中的能量变化。

由上图写出N2(g)和O2(g)生成NO(g)的热化学反应方程式
(2)下图是1 mol NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式

(3)已知:在298K、101kPa下,由稳定的单质生成1mol化合物的反应热叫做该化合物的生成热。如图为氧族元素(除钋外)的氢化物a、b、c、d的生成热数据示意图

①请归纳:非金属元素的气态氢化物的稳定性与氢化物的生成热(ΔH)之间的关系
②写出硒化氢在298K、101kPa时发生分解反应的热化学反应方程式
您最近一年使用:0次



