1 . 工业上,可用纯碱溶液吸收硝酸厂排放的尾气中的 ,并实现资源再利用。有关反应如下:
,并实现资源再利用。有关反应如下:
①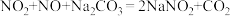
②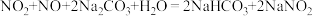
③
下列叙述正确的是
 ,并实现资源再利用。有关反应如下:
,并实现资源再利用。有关反应如下:①
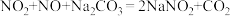
②
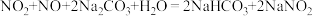
③

下列叙述正确的是
A.常温下溶解度: |
B. 和 和 的混合气体一定能被 的混合气体一定能被 溶液完全吸收 溶液完全吸收 |
C.用澄清石灰水可以区分 和 和 溶液 溶液 |
D.①、②、③中氧化剂与还原剂的物质的量之比均为 |
您最近半年使用:0次
名校
解题方法
2 . 高铁酸钾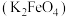 是一种环保、高效的饮用水处理剂。
是一种环保、高效的饮用水处理剂。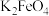 能溶于水,微溶于浓
能溶于水,微溶于浓 溶液,难溶于无水乙醇,在水处理时可转化为
溶液,难溶于无水乙醇,在水处理时可转化为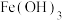 胶体。制备
胶体。制备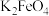 的流程如图所示,下列说法不正确的是
的流程如图所示,下列说法不正确的是
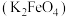 是一种环保、高效的饮用水处理剂。
是一种环保、高效的饮用水处理剂。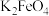 能溶于水,微溶于浓
能溶于水,微溶于浓 溶液,难溶于无水乙醇,在水处理时可转化为
溶液,难溶于无水乙醇,在水处理时可转化为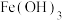 胶体。制备
胶体。制备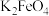 的流程如图所示,下列说法不正确的是
的流程如图所示,下列说法不正确的是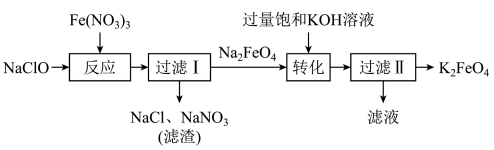
A.可以用滤纸分离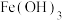 胶体和 胶体和 溶液 溶液 |
B.“反应”中,氧化剂和还原剂的物质的量之比为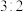 |
C.“转化”说明,该条件下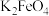 的溶解度小于 的溶解度小于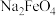 |
D.“过滤Ⅱ”所得的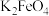 晶体可用无水乙醇洗涤 晶体可用无水乙醇洗涤 |
您最近半年使用:0次
3 . 硝酸镍、硝酸钠在陶瓷、玻璃工业应用广泛。以废弃镍板(含有少量的氧化铝杂质)生产硝酸镍、硝酸钠工艺流程如下:
(1)工业生产普通玻璃的主要原料有石英砂、__________ 、__________ 。
(2)“反应器”中需控制反应温度50~60℃,若温度太低,可能导致的后果是__________ ;若温度太高,可能导致的后果是__________ 。
(3)假如Ni与浓硝酸反应产生的混合气体中 ,该反应的离子方程式为
,该反应的离子方程式为__________ 。
(4)向“浸取液”中加入 调节pH至5~6,能除去浸取液中的
调节pH至5~6,能除去浸取液中的 ,相应原理为
,相应原理为_______ 。__________ 。
(6)向“转化器”中加入稀硝酸的目的是__________ 。
(7)已知:①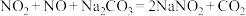 ;
;
②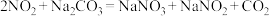 。
。
若将一定体积的 、NO混合气体,通入
、NO混合气体,通入 溶液中恰好被完全吸收,则反应中被氧化的氮原子与被还原的氮原子的质量之比为
溶液中恰好被完全吸收,则反应中被氧化的氮原子与被还原的氮原子的质量之比为__________ 。

(1)工业生产普通玻璃的主要原料有石英砂、
(2)“反应器”中需控制反应温度50~60℃,若温度太低,可能导致的后果是
(3)假如Ni与浓硝酸反应产生的混合气体中
 ,该反应的离子方程式为
,该反应的离子方程式为(4)向“浸取液”中加入
 调节pH至5~6,能除去浸取液中的
调节pH至5~6,能除去浸取液中的 ,相应原理为
,相应原理为__________+
 +
+ __________
__________ +
+ _________+
_________+
 。
。
(6)向“转化器”中加入稀硝酸的目的是
(7)已知:①
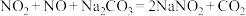 ;
;②
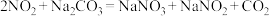 。
。若将一定体积的
 、NO混合气体,通入
、NO混合气体,通入 溶液中恰好被完全吸收,则反应中被氧化的氮原子与被还原的氮原子的质量之比为
溶液中恰好被完全吸收,则反应中被氧化的氮原子与被还原的氮原子的质量之比为
您最近半年使用:0次
4 . 已知氯酸钠与浓盐酸反应的化学方程式为NaClO3+6HCl(浓)=NaCl+3Cl2↑+3H2O。下列说法正确的是
| A.该反应每生成3molCl2,转移6NA个电子 |
| B.NaClO3是氧化剂,发生还原反应 |
| C.还原性:Cl2>HCl |
| D.氧化剂与还原剂的物质的量之比为1∶6 |
您最近半年使用:0次
解题方法
5 . 氢氧化铈  是淡黄色粉末,具有很好的光学性质、电学性质和催化性能,被广泛应用于气数传感器、燃料电池、催化剂等领域。利用铈矿石[主要成分为
是淡黄色粉末,具有很好的光学性质、电学性质和催化性能,被广泛应用于气数传感器、燃料电池、催化剂等领域。利用铈矿石[主要成分为 ]制备氢氧化铈的流程如图。下列说法
]制备氢氧化铈的流程如图。下列说法错误 的是
 是淡黄色粉末,具有很好的光学性质、电学性质和催化性能,被广泛应用于气数传感器、燃料电池、催化剂等领域。利用铈矿石[主要成分为
是淡黄色粉末,具有很好的光学性质、电学性质和催化性能,被广泛应用于气数传感器、燃料电池、催化剂等领域。利用铈矿石[主要成分为 ]制备氢氧化铈的流程如图。下列说法
]制备氢氧化铈的流程如图。下列说法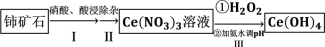
| A.铈是一种常见的稀土元素且属于金属元素 |
B.步骤Ⅰ中发生的反应为 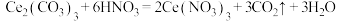 |
| C.步骤Ⅱ中用到的玻璃仪器有漏斗、烧杯、玻璃棒 |
D.步骤Ⅲ中参加反应的氧化剂与还原剂的物质的量之比为 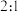 |
您最近半年使用:0次
名校
解题方法
6 . 下列说法中错误的是
A.除去 中NO的气体的方法是将通入足量的 中NO的气体的方法是将通入足量的 |
B. 与 与 的反应中氧化剂与还原剂的质量比为1∶2 的反应中氧化剂与还原剂的质量比为1∶2 |
C.除去NO中 气体的方法是将气体依次通入盛有水和浓 气体的方法是将气体依次通入盛有水和浓 的洗气瓶中 的洗气瓶中 |
D. 与溴蒸气的鉴别可以用水、 与溴蒸气的鉴别可以用水、 溶液或 溶液或 ,但不能用湿润的碘化钾淀粉试纸 ,但不能用湿润的碘化钾淀粉试纸 |
您最近半年使用:0次
解题方法
7 . 在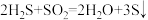 中,氧化剂与还原剂的物质的量之比为
中,氧化剂与还原剂的物质的量之比为
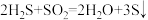 中,氧化剂与还原剂的物质的量之比为
中,氧化剂与还原剂的物质的量之比为| A.2∶1 | B.1∶2 | C.1∶1 | D.16∶17 |
您最近半年使用:0次
名校
8 . 中国科学院科研团队研究表明,在常温、常压和可见光下,基于LDH(一种固体催化剂)合成 的原理示意图如图。下列说法错误的是
的原理示意图如图。下列说法错误的是
 的原理示意图如图。下列说法错误的是
的原理示意图如图。下列说法错误的是
| A.氧化剂与还原剂的物质的量之比为3∶1 |
| B.该过程中涉及极性键和非极性键的断裂与生成 |
C.上述生成 的过程属于氮的固定 的过程属于氮的固定 |
| D.原料氮气可通过分离液态空气获得 |
您最近半年使用:0次
7日内更新
|
146次组卷
|
2卷引用:广东省深圳市翠园中学、龙城高级中学2023-2024学年高一下学期第一次月考化学试题
名校
解题方法
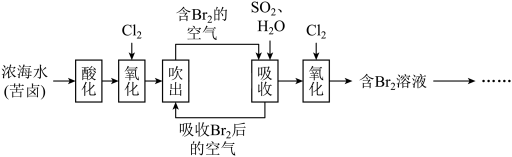
9 . 已知海水中溴元素主要以Br形式存在,工业上从海水中提取溴的流程如下:____________ 。
(2)将吹出后的含Br的空气按一定速率通入吸收塔,用SO2和水进行吸收,吸收后的空气进行循环利用。
①写出吸收反应的离子方程式:_____________ 。
②吹出时,Br2吹出率与吸收塔中SO2流量的关系如图所示。如果SO2流量过大,Br2吹出率反而下降,原因是____________ 。
(4)工业上也可用Na2CO3溶液代替二氧化硫水溶液吸收Br2,根据下列提示写出化学方程式:_________ 。
_________Br2+__________Na2CO3=__________NaBrO3+___________CO2+__________
当有1.204×1024个电子发生转移时,理论上参加反应Br2的质量为________ 。
(2)将吹出后的含Br的空气按一定速率通入吸收塔,用SO2和水进行吸收,吸收后的空气进行循环利用。
①写出吸收反应的离子方程式:
②吹出时,Br2吹出率与吸收塔中SO2流量的关系如图所示。如果SO2流量过大,Br2吹出率反而下降,原因是

| A.NaOH | B.FeCl2 | C.Na2SO3 | D.H2O |
(4)工业上也可用Na2CO3溶液代替二氧化硫水溶液吸收Br2,根据下列提示写出化学方程式:
_________Br2+__________Na2CO3=__________NaBrO3+___________CO2+__________
当有1.204×1024个电子发生转移时,理论上参加反应Br2的质量为
您最近半年使用:0次
10 . 三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生反应:3NF3+5H2O=2NO+HNO3+9HF.下列有关说法正确的是
| A.NF3是氧化剂,H2O是还原剂 |
| B.氧化产物和还原产物的物质的量之比为1∶2 |
| C.还原剂与氧化剂的物质的量之比为2∶1 |
| D.若生成0.2 mol HNO3,则转移0.2 mol电子 |
您最近半年使用:0次



