名校
解题方法
1 . 利用工业废气NO生产 的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中
的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中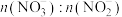 都为
都为 。下列说法错误的是
。下列说法错误的是
 的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中
的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中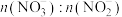 都为
都为 。下列说法错误的是
。下列说法错误的是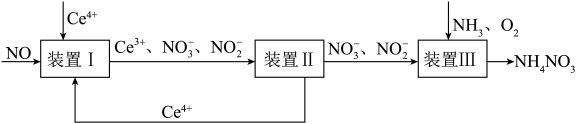
A.装置Ⅰ中若有 参与反应,则转移 参与反应,则转移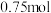 电子 电子 |
B.装置Ⅰ中反应为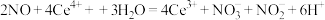 |
C.装置Ⅲ中氧化剂和还原剂的物质的量之比为 |
D.装置Ⅲ中 和 和 的体积比 的体积比 时,可实现原子利用率最大化 时,可实现原子利用率最大化 |
您最近半年使用:0次
名校
解题方法
2 .  是一种重要的杀菌消毒剂,也常用来漂白织物等。已知:饱和
是一种重要的杀菌消毒剂,也常用来漂白织物等。已知:饱和 溶液在温度低于
溶液在温度低于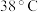 时析出
时析出 晶体,温度高于
晶体,温度高于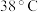 时析出
时析出 晶体,温度高于
晶体,温度高于 时,
时, 分解生成
分解生成 和
和 。其生产工艺如图所示。
。其生产工艺如图所示。
(1) 中氯元素的化合价为
中氯元素的化合价为_______ 。
(2)“反应Ⅰ”中氧化剂与还原剂的物质的量之比为_______ 。
(3)“反应Ⅱ”的离子方程式为_______ 。
(4)“一系列操作”为蒸发浓缩、趁热过滤、_____ 、干燥,其中“趁热过滤”应控制的温度范围是_______ 。
(5)“反应Ⅱ”产生的 可用于制备含氯消毒剂。将
可用于制备含氯消毒剂。将 通入足量
通入足量 溶液中,加热后得到
溶液中,加热后得到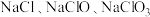 的混合液。经测定
的混合液。经测定 与
与 的物质的量浓度之比为
的物质的量浓度之比为 ,则
,则 与
与 溶液反应时,被氧化的氯元素与被还原的氯元素的物质的量之比为
溶液反应时,被氧化的氯元素与被还原的氯元素的物质的量之比为_______ 。
 是一种重要的杀菌消毒剂,也常用来漂白织物等。已知:饱和
是一种重要的杀菌消毒剂,也常用来漂白织物等。已知:饱和 溶液在温度低于
溶液在温度低于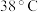 时析出
时析出 晶体,温度高于
晶体,温度高于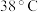 时析出
时析出 晶体,温度高于
晶体,温度高于 时,
时, 分解生成
分解生成 和
和 。其生产工艺如图所示。
。其生产工艺如图所示。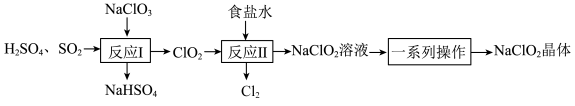
(1)
 中氯元素的化合价为
中氯元素的化合价为(2)“反应Ⅰ”中氧化剂与还原剂的物质的量之比为
(3)“反应Ⅱ”的离子方程式为
(4)“一系列操作”为蒸发浓缩、趁热过滤、
(5)“反应Ⅱ”产生的
 可用于制备含氯消毒剂。将
可用于制备含氯消毒剂。将 通入足量
通入足量 溶液中,加热后得到
溶液中,加热后得到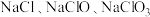 的混合液。经测定
的混合液。经测定 与
与 的物质的量浓度之比为
的物质的量浓度之比为 ,则
,则 与
与 溶液反应时,被氧化的氯元素与被还原的氯元素的物质的量之比为
溶液反应时,被氧化的氯元素与被还原的氯元素的物质的量之比为
您最近半年使用:0次
名校
3 . 利用工业废气NO生产 的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中
的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中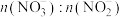 都为1∶1.下列说法错误的是
都为1∶1.下列说法错误的是
 的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中
的流程如图所示。已知装置Ⅰ和装置Ⅱ反应后溶液中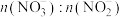 都为1∶1.下列说法错误的是
都为1∶1.下列说法错误的是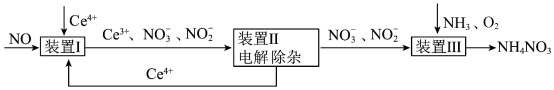
| A.装置江中若有5.6L(标准状况)NO参与反应,则转移1mol电子 |
B.装置Ⅰ中反应为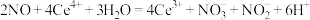 |
| C.装置Ⅲ中氧化剂和还原剂的物质的量之比为1∶2 |
D.装置Ⅲ中 和 和 的体积比3∶1时,可实现原子利用率最大化 的体积比3∶1时,可实现原子利用率最大化 |
您最近半年使用:0次
2024-04-10更新
|
82次组卷
|
2卷引用:山东省青岛第二中学2023-2024学年高一上学期第二次月考化学试卷
名校
解题方法
4 . 《环境科学》刊发了我国科研部门采用零价铁活化过硫酸钠( ,其中S为+6价)去除废水中的正五价砷[As(V)]的研究成果,其反应机制模型如图所示。设阿伏加德罗常数的值为
,其中S为+6价)去除废水中的正五价砷[As(V)]的研究成果,其反应机制模型如图所示。设阿伏加德罗常数的值为 ,
,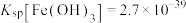 。下列叙述正确的是
。下列叙述正确的是
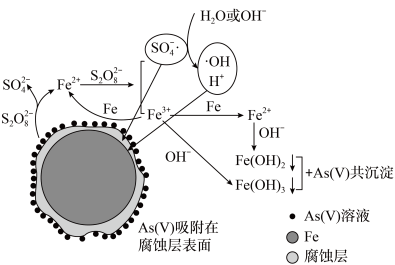
A.1 mol过硫酸钠( )含 )含 个过氧键 个过氧键 |
B.若56 g Fe参加反应,共有 个 个 被还原 被还原 |
C.室温下,中间产物 溶于水所得饱和溶液中 溶于水所得饱和溶液中 为 为 mol⋅L mol⋅L |
| D.pH越小,越有利于去除废水中的正五价砷 |
您最近半年使用:0次
解题方法
5 . K2FeO4具有强氧化性,易溶于水,可迅速杀灭水体中的细菌。某化学小组通过如图装置以Cl2、Fe(OH)3和KOH为 原料制备K2FeO4。
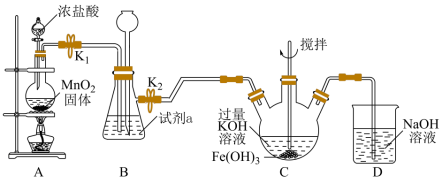
回答下列问题:
(1)K2FeO4属于___________ (填选项字母),其电离方程式为___________ 。
A.酸 B.碱 C.有机物 D.盐
(2)实验前,检查装置 A 气密性的操作为关闭止水夹K1,通过分液漏斗向圆底烧瓶中加水,若观察到___________ ,则证明装置A气密性良好。
(3)装置A中发生反应的离子方程式___________ ;装置B中的试剂a为___________ 。
(4)装置C中发生的反应为 (未配平),该反应中氧化剂和还原剂的物质的量之比为
(未配平),该反应中氧化剂和还原剂的物质的量之比为___________ 。
(5)装置D中发生反应的离子方程式为___________ 。
(6)在用高铁酸钾(K2FeO4)进行水处理时,发生反应的化学方程式为4K2FeO4+10H2O=4Fe(OH)3(胶体)+8KOH+3O2↑。现取49.5g某高铁酸钾样品完全发生上述反应,生成标准状况下3.36LO2,则反应中转移了___________ mole-,该高铁酸钾样品的纯度为___________ 。(用质量分数表示)

回答下列问题:
(1)K2FeO4属于
A.酸 B.碱 C.有机物 D.盐
(2)实验前,检查装置 A 气密性的操作为关闭止水夹K1,通过分液漏斗向圆底烧瓶中加水,若观察到
(3)装置A中发生反应的离子方程式
(4)装置C中发生的反应为
 (未配平),该反应中氧化剂和还原剂的物质的量之比为
(未配平),该反应中氧化剂和还原剂的物质的量之比为(5)装置D中发生反应的离子方程式为
(6)在用高铁酸钾(K2FeO4)进行水处理时,发生反应的化学方程式为4K2FeO4+10H2O=4Fe(OH)3(胶体)+8KOH+3O2↑。现取49.5g某高铁酸钾样品完全发生上述反应,生成标准状况下3.36LO2,则反应中转移了
您最近半年使用:0次
6 . 利用“价类二维图”可以从不同角度研究含铁物质的性质及其转化关系,图中甲~戊均含铁元素。回答下列问题:
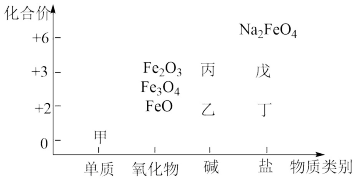
(1)Na2FeO4是一种新型饮用水消毒剂。工业上常用NaClO、Fe(NO3)3、NaOH制备:3ClO-+2Fe3++10OH-=2
 +3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为
+3Cl-+5H2O,该反应中氧化剂与还原剂的物质的量之比为(2)打印机使用的墨粉中含有Fe3O4,下列关于Fe3O4的说法正确的是 (填标号)。
| A.有磁性,是FeO与Fe2O3的混合物 |
| B.属于两性氧化物,与酸、碱都能反应 |
| C.Fe3O4与稀盐酸反应生成Fe2+与Fe3+物质的量之比为1:2 |
| D.Fe与水蒸气在高温下反应能生成Fe3O4 |
您最近半年使用:0次
7 . 用还原法可以将硝酸厂烟气中的大量氮氧化物(NOx)转化为无害物质。常温下,将NO与H2的混合气体通入Ce(SO4)2与Ce2(SO4)2的混合溶液中,其物质的转化过程如图所示。
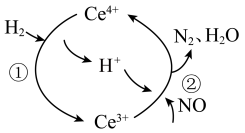
下列说法正确的是

下列说法正确的是
| A.反应①②中含Ce的物质均作氧化剂 |
| B.反应①中氧化剂与还原剂的个数之比为1:2 |
C.总反应的化学方程式为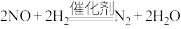 |
| D.转化反应前后混合溶液内Ce3+和Ce4+的总数保持不变 |
您最近半年使用:0次
解题方法
8 . 水体中过量氨氮(以NH3表示)含量过高会导致水体富营养化。用次氯酸钠除去氨氮的一种原理如图所示。下列说法正确的是
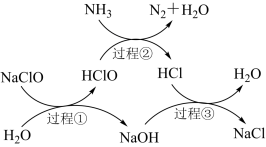

| A.过程①②③均属于氧化还原反应 |
| B.在较高温度下,氨氮去除率会降低 |
| C.每生成一个N2分子,转移6个电子 |
D.过程②中氧化剂与还原剂的物质的量之比是 |
您最近半年使用:0次
名校
解题方法
9 . 二氧化氯(ClO2)是一种黄绿色气体,熔点为-59.5℃,沸点为11.0℃,易溶于水且不与冷水反应,浓度过高时易发生分解引起爆炸,制备二氧化氯溶液的装置如图所示:
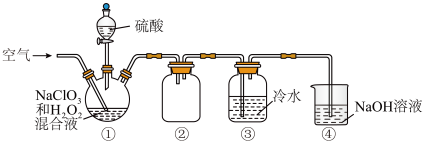
下列说法错误的是

下列说法错误的是
| A.实验中,通入空气的作用之一是稀释ClO2 |
| B.装置②作安全瓶,起防止倒吸的作用 |
| C.装置①反应中氧化剂与还原剂的物质的量之比为1:2 |
| D.当看到装置③中导管内液面上升时,应增大空气的通入速率 |
您最近半年使用:0次
2024-03-01更新
|
234次组卷
|
2卷引用:山东省淄博市2023-2024学年高一上学期期末考试化学试题
解题方法
10 . 一种制备 的工艺路线如图所示
的工艺路线如图所示
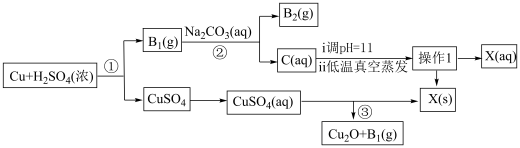
已知:ⅰ.常温下, 的电离平衡常数
的电离平衡常数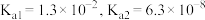
ⅱ.反应②所得C溶液 在
在 之间
之间
ⅲ.反应③需及时补加 以保持反应在
以保持反应在 条件下进行。
条件下进行。
(1)反应①中氧化剂与还原剂物质的量之比为___________ ,溶液C的溶质为___________ (填化学式)。
(2)低温真空蒸发主要目的是___________ ,操作1的名称为___________ 。
(3)写出流程中可以循环利用的物质___________ (填化学式)。
(4)写出反应③的化学反应方程式___________ 。
(5)若 产量不变,参与反应③的X与
产量不变,参与反应③的X与 物质的量之比
物质的量之比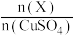 增大时,需补加
增大时,需补加 的量
的量___________ (填“减少”或“增多”或“不变”)。
 的工艺路线如图所示
的工艺路线如图所示
已知:ⅰ.常温下,
 的电离平衡常数
的电离平衡常数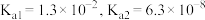
ⅱ.反应②所得C溶液
 在
在 之间
之间ⅲ.反应③需及时补加
 以保持反应在
以保持反应在 条件下进行。
条件下进行。(1)反应①中氧化剂与还原剂物质的量之比为
(2)低温真空蒸发主要目的是
(3)写出流程中可以循环利用的物质
(4)写出反应③的化学反应方程式
(5)若
 产量不变,参与反应③的X与
产量不变,参与反应③的X与 物质的量之比
物质的量之比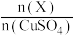 增大时,需补加
增大时,需补加 的量
的量
您最近半年使用:0次



