解题方法
1 . Ⅰ、
(1)室温下,试计算:
①pH=4的亚硫酸溶液中,c(H+)H2O=___________ 。
②pH=2的盐酸加水稀释到1000倍,溶液的pH=___________ 。
Ⅱ、某温度下的水溶液中,c(H+)=10-xmol·L-1,c(OH-)=10-ymol·L-1。x与y的关系如图所示:

(2)该温度下水的离子积为___________ (填具体数值);该温度___________ (填“高于”“低于”或“等于”)常温。
(3)该温度下0.01mol·L-1NaOH溶液的pH为___________ 。
(4)除了用pH外,科学家还建议用酸度(AG)来表示溶液的酸碱性:AG=lg 。则该温度下,0.01mol·L-1盐酸的酸度AG=
。则该温度下,0.01mol·L-1盐酸的酸度AG=___________ 。
(1)室温下,试计算:
①pH=4的亚硫酸溶液中,c(H+)H2O=
②pH=2的盐酸加水稀释到1000倍,溶液的pH=
Ⅱ、某温度下的水溶液中,c(H+)=10-xmol·L-1,c(OH-)=10-ymol·L-1。x与y的关系如图所示:

(2)该温度下水的离子积为
(3)该温度下0.01mol·L-1NaOH溶液的pH为
(4)除了用pH外,科学家还建议用酸度(AG)来表示溶液的酸碱性:AG=lg
 。则该温度下,0.01mol·L-1盐酸的酸度AG=
。则该温度下,0.01mol·L-1盐酸的酸度AG=
您最近一年使用:0次
2 . 回答下列问题
(1)25℃时有甲、乙、丙三种溶液,甲为 溶液,乙为
溶液,乙为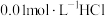 溶液,丙为
溶液,丙为 溶液,请回答下列问题:
溶液,请回答下列问题:
①甲溶液的
_____ 。乙溶液中由水电离出的
_____  。
。
②写出丙的电离方程式_____ 。
③用 的HCl和
的HCl和 两溶液分别与25mL甲完全中和,则消耗这两种酸的体积大小关系为
两溶液分别与25mL甲完全中和,则消耗这两种酸的体积大小关系为
_____  (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
(2)室温时,向 的醋酸溶液中加入等体积的
的醋酸溶液中加入等体积的 的
的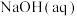 ,充分反应后所得溶液的
,充分反应后所得溶液的 ,所得溶液中
,所得溶液中
_____  。
。
(1)25℃时有甲、乙、丙三种溶液,甲为
 溶液,乙为
溶液,乙为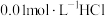 溶液,丙为
溶液,丙为 溶液,请回答下列问题:
溶液,请回答下列问题:①甲溶液的


 。
。②写出丙的电离方程式
③用
 的HCl和
的HCl和 两溶液分别与25mL甲完全中和,则消耗这两种酸的体积大小关系为
两溶液分别与25mL甲完全中和,则消耗这两种酸的体积大小关系为
 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。(2)室温时,向
 的醋酸溶液中加入等体积的
的醋酸溶液中加入等体积的 的
的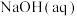 ,充分反应后所得溶液的
,充分反应后所得溶液的 ,所得溶液中
,所得溶液中
 。
。
您最近一年使用:0次
3 . 已知在800 K时,反应:CO(g)+H2O(g)⇌H2(g)+CO2(g),若初始浓度c0(CO)=2 mol·L-1,c0(H2O)=3 mol·L-1,则反应达到平衡时,CO转化成CO2的转化率为60%。求:
(1)800 K时该反应的平衡常数_______ ;
(2)如果将H2O的初始浓度加大为6 mol·L-1,求此时CO转化为CO2的转化率______ 。
(1)800 K时该反应的平衡常数
(2)如果将H2O的初始浓度加大为6 mol·L-1,求此时CO转化为CO2的转化率
您最近一年使用:0次
名校
4 . 含有 个HCl分子,物质的量是
个HCl分子,物质的量是_______ mol,在标准状况下的体积是_______ 升,溶于水得到50mL盐酸溶液,物质的量浓度是_______  ,加入足量的
,加入足量的 粉末,生成的
粉末,生成的 全部通入足量NaOH溶液中,溶液增重
全部通入足量NaOH溶液中,溶液增重_______ 克。
 个HCl分子,物质的量是
个HCl分子,物质的量是 ,加入足量的
,加入足量的 粉末,生成的
粉末,生成的 全部通入足量NaOH溶液中,溶液增重
全部通入足量NaOH溶液中,溶液增重
您最近一年使用:0次
5 . 现用Zn与实验室中的盐酸反应制取6.72 L H2(标准状况)。
(1)如果选用所贴标签为3.0mol·L-1的盐酸,至少需该盐酸多少毫升_____ ?
(2)该盐酸密度为1.052g·mL-1,则该盐酸溶质的质量分数是多少_____ ? (保留三位有效数字3分)
(1)如果选用所贴标签为3.0mol·L-1的盐酸,至少需该盐酸多少毫升
(2)该盐酸密度为1.052g·mL-1,则该盐酸溶质的质量分数是多少
您最近一年使用:0次
解题方法
6 . 关于物质的量的计算(要写单位)
(1)34gNH3含有___________ 个氢原子。
(2)1.2g RSO4中含0.01 mol R2+,则RSO4的摩尔质量是___________ 。
(3)将8g NaOH配制成1L溶液,其物质的量浓度为___________ 。
(4)标准状况下,与72 g H2O 含有相同氢原子数的CH4 的体积是___________ 。
(5)质量相同的 HCl、NH3、CO2、O2四种气体中,在相同温度和相同压强条件下,体积最大的是___________ 。
(1)34gNH3含有
(2)1.2g RSO4中含0.01 mol R2+,则RSO4的摩尔质量是
(3)将8g NaOH配制成1L溶液,其物质的量浓度为
(4)标准状况下,与72 g H2O 含有相同氢原子数的CH4 的体积是
(5)质量相同的 HCl、NH3、CO2、O2四种气体中,在相同温度和相同压强条件下,体积最大的是
您最近一年使用:0次
解题方法
7 . 向200mL 6mol·L-1盐酸中加入一定量的纯净CaCO3,产生气体的体积随时间的变化曲线如图所示(气体体积均在标准状况下测定)。若反应过程中溶液体积的变化忽略不计,则EF段用盐酸表示的化学反应速率 v(HCl) =___________


您最近一年使用:0次
解题方法
8 . (1)用KMnO4氧化盐酸溶液,反应方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,若产生的Cl2在标准状况下体积为56L,计算:参加反应的HCl的物质的量_______ 反应中被氧化的HCl的物质的量_______
(2)向某硝酸银溶液中,逐滴加入密度为1.10g·mL-1的盐酸溶液,恰好完全反应时,过滤所得沉淀的质量恰好与盐酸溶液的质量相等。求盐酸的质量分数_______ (需要过程)。
(2)向某硝酸银溶液中,逐滴加入密度为1.10g·mL-1的盐酸溶液,恰好完全反应时,过滤所得沉淀的质量恰好与盐酸溶液的质量相等。求盐酸的质量分数
您最近一年使用:0次
解题方法
9 . 在2L密闭容器中,800℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
(1)上述反应___________ (填“是”或“不是”)可逆反应。
(2)如图所示,到达化学平衡的时间大约为___________ 秒。表示NO2变化曲线的是___________ ,用O2表示从0~2s内该反应的平均速率v=___________

(3)能说明该反应已达到平衡状态的是___________ (填序号)。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)如图所示,到达化学平衡的时间大约为

(3)能说明该反应已达到平衡状态的是
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
您最近一年使用:0次
10 . 某温度时,在2L的密闭容器中,X、Y、Z三种物质的量随时间的变化曲线如图所示。
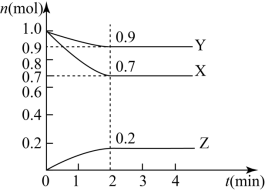
(1)X的转化率是___________ ;
(2)由图中所给数据进行分析,该反应的化学方程式为___________ ;
(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=___________ .

(1)X的转化率是
(2)由图中所给数据进行分析,该反应的化学方程式为
(3)反应从开始至2分钟末,用Z的浓度变化表示的平均反应速率为v(Z)=
您最近一年使用:0次
2021-03-31更新
|
183次组卷
|
3卷引用:福建省建瓯市芝华中学2021-2022学年高二上学期期中考试化学试题



