1 . 化学实验兴趣小组对当地出产的大理石中所含碳酸钙的质量分数进行了测定。取15g大理石样品放入烧杯中,再向其中加入194.4g盐酸充分反应。反应结束后称量剩余混合物的质量为205g(提示:大理石样品中的杂质不与稀盐酸反应也不溶于水;反应的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑),求:
(1)反应生成CO2的质量_____ 。
(2)反应后所得溶液的溶质质量分数(结果保留一位小数)_____ 。
(1)反应生成CO2的质量
(2)反应后所得溶液的溶质质量分数(结果保留一位小数)
您最近一年使用:0次
2 . 将4.6g钠投入一定量的水中,充分反应,所得溶液加水稀释到500mL。求:
(1)反应中生成的气体在标况下的体积______ ?
(2)所得溶液中,溶质的物质的量浓度______ ?
(1)反应中生成的气体在标况下的体积
(2)所得溶液中,溶质的物质的量浓度
您最近一年使用:0次
3 . 一定温度下,体积为2L的密闭容器中装有4molSO2和2molO2,发生反应2SO2+O2 2SO3。2min末达到平衡测得容器中有1.6molSO2,请计算:
2SO3。2min末达到平衡测得容器中有1.6molSO2,请计算:
(1)2min末SO3的浓度是___________ ;
(2)2min内SO2的平均反应速率是___________ 。
(3)2min内O2的转化率是___________ 。
(4)该温度下的平衡常数为K=___________ L·mol-1。(计算结果)
 2SO3。2min末达到平衡测得容器中有1.6molSO2,请计算:
2SO3。2min末达到平衡测得容器中有1.6molSO2,请计算:(1)2min末SO3的浓度是
(2)2min内SO2的平均反应速率是
(3)2min内O2的转化率是
(4)该温度下的平衡常数为K=
您最近一年使用:0次
名校
解题方法
4 . 完成下列两小题的计算:
(1)现有14.4gCO和CO2的混合气体,在标准状况下其体积为8.96L。
①该混合气体的平均摩尔质量为______ ,混合气体中碳原子的个数为______ (用NA表示阿伏加德罗常数)。
②将混合气体依次通过如图所示装置,最后收集在气球中(实验在标准状况下测定)。
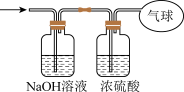
气球中收集到的气体的摩尔质量为______ ,气球的体积为______  。
。
(2) 固体中含有部分
固体中含有部分 。取该固体
。取该固体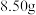 充分加热,产生的气体依次通过浓硫酸(增重
充分加热,产生的气体依次通过浓硫酸(增重 )和碱石灰(增重
)和碱石灰(增重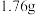 )。请计算:
)。请计算:
①加热分解产生的气体中 在标准状况下的体积为
在标准状况下的体积为______ L。
②固体中 的质量为
的质量为______ g。
③固体中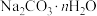 的
的 值为
值为______ 。
(1)现有14.4gCO和CO2的混合气体,在标准状况下其体积为8.96L。
①该混合气体的平均摩尔质量为
②将混合气体依次通过如图所示装置,最后收集在气球中(实验在标准状况下测定)。

气球中收集到的气体的摩尔质量为
 。
。(2)
 固体中含有部分
固体中含有部分 。取该固体
。取该固体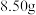 充分加热,产生的气体依次通过浓硫酸(增重
充分加热,产生的气体依次通过浓硫酸(增重 )和碱石灰(增重
)和碱石灰(增重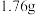 )。请计算:
)。请计算:①加热分解产生的气体中
 在标准状况下的体积为
在标准状况下的体积为②固体中
 的质量为
的质量为③固体中
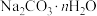 的
的 值为
值为
您最近一年使用:0次
2024-01-10更新
|
141次组卷
|
2卷引用: 云南师范大学附属中学2023-2024学年高一上学期教学测评月考卷(二)化学试题
名校
解题方法
5 . 研究物质性质及物质转化具有重要的价值。回答下列问题:
(1)已知常温下,在溶液中可发生如下反应。
① ;②
;② 。
。
反应①中还原剂为_____ ;反应②中每消耗1个 ,转移
,转移_____ 个电子。
(2)某反应的反应物与生成物有 ,已知氧化性:
,已知氧化性: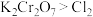 ,写出并配平该化学方程式:
,写出并配平该化学方程式:_____ 。
(3)按如图所示操作,充分反应后。

①试管Ⅰ中发生反应的化学方程式为_____ ;试管Ⅱ中铜丝上观察到的现象是_____ 。
②结合Ⅰ、Ⅱ实验现象可知 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为_____ 。
(1)已知常温下,在溶液中可发生如下反应。
①
 ;②
;② 。
。反应①中还原剂为
 ,转移
,转移(2)某反应的反应物与生成物有
 ,已知氧化性:
,已知氧化性: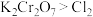 ,写出并配平该化学方程式:
,写出并配平该化学方程式:(3)按如图所示操作,充分反应后。

①试管Ⅰ中发生反应的化学方程式为
②结合Ⅰ、Ⅱ实验现象可知
 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为
您最近一年使用:0次
解题方法
6 . 实验室制备氯气的反应为: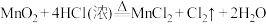 ,当生成7.1g
,当生成7.1g 时,计算:(要求有计算过程)
时,计算:(要求有计算过程)
(1)参加反应的 的质量
的质量___________ ;
(2)被氧化的HCl的质量___________ 。
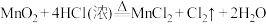 ,当生成7.1g
,当生成7.1g 时,计算:(要求有计算过程)
时,计算:(要求有计算过程)(1)参加反应的
 的质量
的质量(2)被氧化的HCl的质量
您最近一年使用:0次
名校
解题方法
7 . 某固体粉末由Na2O与Na2O2组成,将其分成等量的两份,第一份恰好与 2 L 0.3 mol/L 盐酸完全中和;第二份与足量的CO2气体作用,发现该固体质量增加了 11.6 g,试计算:
(1)与第一份反应的盐酸的物质的量是___________ 。
(2)第一份中和所得溶质的质量___________ g;
(3)固体中Na2O与Na2O2的物质的量之比是___________ 。
(1)与第一份反应的盐酸的物质的量是
(2)第一份中和所得溶质的质量
(3)固体中Na2O与Na2O2的物质的量之比是
您最近一年使用:0次
2023-11-23更新
|
328次组卷
|
3卷引用:浙江省温州市2023-2024学年瑞安市十校联考高一上学期化学期中试卷
浙江省温州市2023-2024学年瑞安市十校联考高一上学期化学期中试卷浙江省温州市瑞安十校联考2023-2024学年高一上学期期中化学试题(已下线)【精品卷】3.2.2 物质的量在化学方程式计算中的应用课堂例题-人教版2023-2024学年必修第一册
名校
8 . 有机物M可从酸牛奶中提取。已知纯净的M为无色黏液体,易溶于水。研究M的组成与结构,进行了如下实验:
| 实验步骤 | 解释或实验结论 |
| (1)称取M4.5g,升温使其汽化,测其密度是相同条件下H2的45倍。 | 试通过计算填空: (1)M的摩尔质量为: |
| (2)将此4.5gM在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重2.7g和6.6g | (2)M的分子式为: |
| (3)通过M的红外光谱图发现该分子中既有羟基,还有羧基 | (3)写出羟基电子式 |
M的核磁共振氢谱如下图: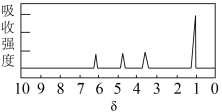 | (4)M中含有 (5)写出M中所含官能团的名称: (6)综上所述,M的结构简式为 |
您最近一年使用:0次
名校
9 . 某学生在实验室里分析一瓶部分变质的氢氧化钠样品的组成。他先称取mg此样品倒入某容器,然后加入245g10%的稀硫酸,结果恰好完全反应,收集到8.8g气体;再取相同质量的该样品配成405.2g溶液,加入一定质量的熟石灰后也恰好完全反应。求:
(1)该样品的组成情况和m的值_______ ;
(2)405.2g该样品溶液与熟石灰反应后所得溶液的溶质质量分数_______ 。
(1)该样品的组成情况和m的值
(2)405.2g该样品溶液与熟石灰反应后所得溶液的溶质质量分数
您最近一年使用:0次
10 . )某化学小组为测定有机物G的组成和结构,设计如图实验装置:
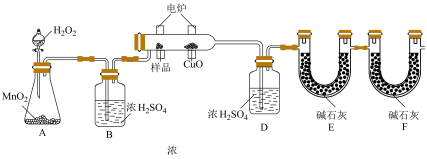
回答下列问题:
(1)实验开始时,先打开__________ (填装置名称),一段时间后再加热反应管C,目的是__________ 。写出A中发生的反应方程式:__________ 。
(2)装置B和装置D中浓硫酸的作用分别是__________ 和__________ 。
(3)装置E和装置F中碱石灰的作用分别是__________ 和__________ 。
(4)若准确称取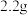 样品G(只含C、H、O三种元素),经充分燃烧后(
样品G(只含C、H、O三种元素),经充分燃烧后( 的作用是确保有机物充分氧化,最终生成
的作用是确保有机物充分氧化,最终生成 和
和 ),装置D质量增加
),装置D质量增加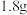 ,U形管E质量增加
,U形管E质量增加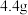 。又知有机物G的质谱图如图所示。
。又知有机物G的质谱图如图所示。
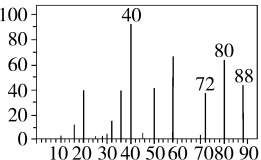
该有机物的分子式为__________ 。
(5)已知有机物G中含有羧基,经测定其核磁共振氢谱有3组峰,且峰面积之比为 。综上所述,G的结构简式为
。综上所述,G的结构简式为__________ 。

回答下列问题:
(1)实验开始时,先打开
(2)装置B和装置D中浓硫酸的作用分别是
(3)装置E和装置F中碱石灰的作用分别是
(4)若准确称取
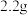 样品G(只含C、H、O三种元素),经充分燃烧后(
样品G(只含C、H、O三种元素),经充分燃烧后( 的作用是确保有机物充分氧化,最终生成
的作用是确保有机物充分氧化,最终生成 和
和 ),装置D质量增加
),装置D质量增加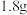 ,U形管E质量增加
,U形管E质量增加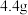 。又知有机物G的质谱图如图所示。
。又知有机物G的质谱图如图所示。
该有机物的分子式为
(5)已知有机物G中含有羧基,经测定其核磁共振氢谱有3组峰,且峰面积之比为
 。综上所述,G的结构简式为
。综上所述,G的结构简式为
您最近一年使用:0次



