完成下列两小题的计算:
(1)现有14.4gCO和CO2的混合气体,在标准状况下其体积为8.96L。
①该混合气体的平均摩尔质量为______ ,混合气体中碳原子的个数为______ (用NA表示阿伏加德罗常数)。
②将混合气体依次通过如图所示装置,最后收集在气球中(实验在标准状况下测定)。
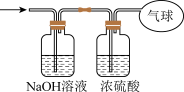
气球中收集到的气体的摩尔质量为______ ,气球的体积为______  。
。
(2) 固体中含有部分
固体中含有部分 。取该固体
。取该固体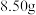 充分加热,产生的气体依次通过浓硫酸(增重
充分加热,产生的气体依次通过浓硫酸(增重 )和碱石灰(增重
)和碱石灰(增重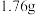 )。请计算:
)。请计算:
①加热分解产生的气体中 在标准状况下的体积为
在标准状况下的体积为______ L。
②固体中 的质量为
的质量为______ g。
③固体中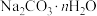 的
的 值为
值为______ 。
(1)现有14.4gCO和CO2的混合气体,在标准状况下其体积为8.96L。
①该混合气体的平均摩尔质量为
②将混合气体依次通过如图所示装置,最后收集在气球中(实验在标准状况下测定)。

气球中收集到的气体的摩尔质量为
 。
。(2)
 固体中含有部分
固体中含有部分 。取该固体
。取该固体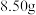 充分加热,产生的气体依次通过浓硫酸(增重
充分加热,产生的气体依次通过浓硫酸(增重 )和碱石灰(增重
)和碱石灰(增重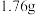 )。请计算:
)。请计算:①加热分解产生的气体中
 在标准状况下的体积为
在标准状况下的体积为②固体中
 的质量为
的质量为③固体中
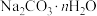 的
的 值为
值为
更新时间:2024-01-10 15:19:03
|
相似题推荐
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】某化工厂以甲烷为原料合成甲醇的反应为:(所有气体体积均已折算为标准状况)
反应器①中: CH4(g)+H2O(g)→CO(g)+3H2(g)
反应器②中: CO(g)+2H2(g)→CH3OH(g)
(该反应CO的转化率为 )
)
(1)在反应器①中通入体积为672m3的甲烷和足量的水蒸气,充分反应后通入反应器②,则反应剩余物中n(CO)=________________ ,n(H2)=__________________ 。
(2)为增大产量,该厂在原工艺的基础上,将下列反应运用于生产甲醇原料气:反应器③中2CH4(g)+O2(g)→2CO(g)+4H2(g),若新工艺中充入反应器 ①的甲烷体积为a,水蒸气足量,反应器③的甲烷体积为b,最终反应产物中:V(CO)︰V(H2) = 1︰3。
①求充入反应器①③的甲烷的体积比a︰b=________ ;
②若最终反应剩余物中有N2,且V ( N2) = V(CO),则该空气中氧气的体积分数为多少?(要求:写出本小题的计算过程)________________
反应器①中: CH4(g)+H2O(g)→CO(g)+3H2(g)
反应器②中: CO(g)+2H2(g)→CH3OH(g)
(该反应CO的转化率为
 )
)(1)在反应器①中通入体积为672m3的甲烷和足量的水蒸气,充分反应后通入反应器②,则反应剩余物中n(CO)=
(2)为增大产量,该厂在原工艺的基础上,将下列反应运用于生产甲醇原料气:反应器③中2CH4(g)+O2(g)→2CO(g)+4H2(g),若新工艺中充入反应器 ①的甲烷体积为a,水蒸气足量,反应器③的甲烷体积为b,最终反应产物中:V(CO)︰V(H2) = 1︰3。
①求充入反应器①③的甲烷的体积比a︰b=
②若最终反应剩余物中有N2,且V ( N2) = V(CO),则该空气中氧气的体积分数为多少?(要求:写出本小题的计算过程)
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
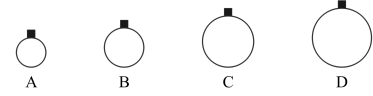
【推荐2】(1)常温常压下,用等质量的CH4、CO2、O2、SO2四种气体分别吹出四个气球,其中气体为SO2的是_________ (填选项序号)。
(2)在标准状况下,2.24L由N2、N2O组成的混合气体中含有的氮元素的质量约为_______ 。
(3)在0.1L由KCl、K2SO4、ZnSO4形成的某植物营养液中,c(K+)=0.7mol•L﹣1,c(Zn2+)=0.1mol•L﹣1,c(Cl﹣)=0.3mol•L﹣1,向混合溶液中滴加足量的BaCl2溶液后产生沉淀的物质的量为_________ 。
(4)0.3mol的甲烷与_________ g氨气中所含氢原子数相等。
(5)在同温同压下,2g二氧化碳的体积为120ml,而2gA气体的体积为165ml,则气体A的摩尔质量_________________ ;
(6)标准状况下,11.2L二氧化碳和一氧化碳混合气体的质量为18g,则其中二氧化碳的质量为_________ ,一氧化碳的体积为_________ 。
(7)氯气(Cl2)、重铬酸钾(K2Cr2O7)是常用的氧化剂。
①硫代硫酸钠(Na2S2O3)被称为“养鱼宝”,可降低水中的氯气对鱼的危害。已知25.0mL0.100mol•L﹣1 Na2S2O3溶液恰好把标准状况下224mL的Cl2完全转化为Cl﹣,则S2O32﹣将转化成____________ 。
A.S2﹣ B.S C.SO32﹣ D.SO42﹣
②实验室可用K2Cr2O7固体与浓盐酸反应制备氯气,发生反应的化学方程式为K2Cr2O7+14HCl(浓)=3Cl2↑+2CrCl3+2KCl+7H2O,若反应中转移0.6mole﹣,则被氧化的HCl的物质的量为_____________ 。

(2)在标准状况下,2.24L由N2、N2O组成的混合气体中含有的氮元素的质量约为
(3)在0.1L由KCl、K2SO4、ZnSO4形成的某植物营养液中,c(K+)=0.7mol•L﹣1,c(Zn2+)=0.1mol•L﹣1,c(Cl﹣)=0.3mol•L﹣1,向混合溶液中滴加足量的BaCl2溶液后产生沉淀的物质的量为
(4)0.3mol的甲烷与
(5)在同温同压下,2g二氧化碳的体积为120ml,而2gA气体的体积为165ml,则气体A的摩尔质量
(6)标准状况下,11.2L二氧化碳和一氧化碳混合气体的质量为18g,则其中二氧化碳的质量为
(7)氯气(Cl2)、重铬酸钾(K2Cr2O7)是常用的氧化剂。
①硫代硫酸钠(Na2S2O3)被称为“养鱼宝”,可降低水中的氯气对鱼的危害。已知25.0mL0.100mol•L﹣1 Na2S2O3溶液恰好把标准状况下224mL的Cl2完全转化为Cl﹣,则S2O32﹣将转化成
A.S2﹣ B.S C.SO32﹣ D.SO42﹣
②实验室可用K2Cr2O7固体与浓盐酸反应制备氯气,发生反应的化学方程式为K2Cr2O7+14HCl(浓)=3Cl2↑+2CrCl3+2KCl+7H2O,若反应中转移0.6mole﹣,则被氧化的HCl的物质的量为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】在100mL NaOH溶液中加入NH4NO3和(NH4)2SO4的固体混合物,加热充分反应。下图表示加入的混合物的质量与产生的气体体积(标准状况)的关系。
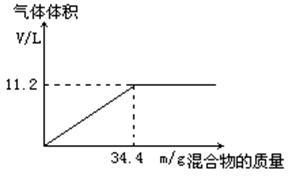
(1) NaOH溶液的物质的量浓度为________ 。
(2)当NaOH溶液的体积为80mL,固体混合物的质量为34.4g,充分反应后,生成气体的体积在标准状况下为_______ 升。
(3)当NaOH溶液的体积为120mL,固体混合物的质量仍为34.4g,充分反应后,生成气体的体积在标准状况下为_______ 升。

(1) NaOH溶液的物质的量浓度为
(2)当NaOH溶液的体积为80mL,固体混合物的质量为34.4g,充分反应后,生成气体的体积在标准状况下为
(3)当NaOH溶液的体积为120mL,固体混合物的质量仍为34.4g,充分反应后,生成气体的体积在标准状况下为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】(1)NA为阿伏加德罗常数。25℃时,1g水中含H+离子个数约为__________ NA。
(2)通过氨的催化氧化法制取硝酸,在此全过程中,理论上氨与所耗氧气的物质的量比为__________ ,这样所得硝酸的质量分数为_____________ 。
(3)往含0.2 mol NaOH和0.1 mol Ca(OH)2的混合溶液中持续稳定地通入CO2气体0.5 mol。请以CO2的量为横坐标,以溶液中离子的总量为横坐标,画出离子总量随CO2加入量变化的折线图。(不计弱电解质的电离和盐的水解)_____________

(4)某研究性学习小组拟用铜屑与氧化铜混合物与硫酸和硝酸组成的混酸反应来制取CuSO4·5H2O晶体,混酸中硝酸的还原产物为NO,反应过程中不产生SO2,反应后的溶液中不含Cu(NO3)2, 反应中固体完全溶解,两种酸均恰好完全反应。设固体混合物的总质量为480 g,其中铜屑的质量分数为0.4, 480g固体混合物与一定量混酸微热后,充分反应,冷却恰好只得到CuSO4·5H2O,试求原混酸中H2SO4的质量分数_____________ (写出计算过程)
(2)通过氨的催化氧化法制取硝酸,在此全过程中,理论上氨与所耗氧气的物质的量比为
(3)往含0.2 mol NaOH和0.1 mol Ca(OH)2的混合溶液中持续稳定地通入CO2气体0.5 mol。请以CO2的量为横坐标,以溶液中离子的总量为横坐标,画出离子总量随CO2加入量变化的折线图。(不计弱电解质的电离和盐的水解)

(4)某研究性学习小组拟用铜屑与氧化铜混合物与硫酸和硝酸组成的混酸反应来制取CuSO4·5H2O晶体,混酸中硝酸的还原产物为NO,反应过程中不产生SO2,反应后的溶液中不含Cu(NO3)2, 反应中固体完全溶解,两种酸均恰好完全反应。设固体混合物的总质量为480 g,其中铜屑的质量分数为0.4, 480g固体混合物与一定量混酸微热后,充分反应,冷却恰好只得到CuSO4·5H2O,试求原混酸中H2SO4的质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】(1)Na2O2因能发生下列反应被用作补氧剂:2Na2O2+2CO2=2Na2CO3+O2,上述反应中,氧化剂与还原剂的物质的量之比为:___ 。
(2)某潜艇上有50人,每人每分钟消耗1.12LO2(标况),则一天需___ molNa2O2。如用KO2作补氧剂,写出它和CO2反应的化学方程式_____ 。
①1kgNa2O2和1kgKO2分别和足量的CO2反应,生成O2的体积(同温同压)比为_____ 。
②等量的CO2分别和足量的Na2O2、KO2反应,生成O2的分子数(同温同压)比为____ 。
③你认为选用____ 作补氧剂更为合适,理由是_____ 。
(2)某潜艇上有50人,每人每分钟消耗1.12LO2(标况),则一天需
①1kgNa2O2和1kgKO2分别和足量的CO2反应,生成O2的体积(同温同压)比为
②等量的CO2分别和足量的Na2O2、KO2反应,生成O2的分子数(同温同压)比为
③你认为选用
您最近一年使用:0次
【推荐3】黄色固体聚合硫酸铁(SPFS)是一种重要的无机高分子絮凝剂,极易溶于水,作为工业和生活污水处理等领域具有重要的应用。SPFS可表示成Fex(OH)y(SO4)z·nH2O。工业上常用的一种制备流程为:

在SPFS的多个质量指标中,盐基度是重要的质量指标之一,盐基度定义为:
盐基度= ×100%。式中n(OH-)、n(Fe)分别表示固体聚合硫酸铁中OH-和Fe元素的物质的量。请回答下列问题:
×100%。式中n(OH-)、n(Fe)分别表示固体聚合硫酸铁中OH-和Fe元素的物质的量。请回答下列问题:
(1)写出在酸性介质中用NaClO3氧化绿矾(FeSO4·7H2O)的离子方程式________ 。
(2)取7.51 g某固体聚合硫酸铁溶解于水,向其中加入过量的BaCl2溶液到沉淀完全,经过滤、洗涤、干燥得白色沉淀10.485 g,向上述滤液中加入NH3·H2O,调节溶液pH=6,经过滤、洗涤、干燥得Fe2O3固体2.80 g。试计算该固体聚合硫酸铁的盐基度为_____ 。
(3)计算出该固体聚合硫酸铁样品的化学式(x、y、z、n均取整数)为____________ 。

在SPFS的多个质量指标中,盐基度是重要的质量指标之一,盐基度定义为:
盐基度=
 ×100%。式中n(OH-)、n(Fe)分别表示固体聚合硫酸铁中OH-和Fe元素的物质的量。请回答下列问题:
×100%。式中n(OH-)、n(Fe)分别表示固体聚合硫酸铁中OH-和Fe元素的物质的量。请回答下列问题:(1)写出在酸性介质中用NaClO3氧化绿矾(FeSO4·7H2O)的离子方程式
(2)取7.51 g某固体聚合硫酸铁溶解于水,向其中加入过量的BaCl2溶液到沉淀完全,经过滤、洗涤、干燥得白色沉淀10.485 g,向上述滤液中加入NH3·H2O,调节溶液pH=6,经过滤、洗涤、干燥得Fe2O3固体2.80 g。试计算该固体聚合硫酸铁的盐基度为
(3)计算出该固体聚合硫酸铁样品的化学式(x、y、z、n均取整数)为
您最近一年使用:0次
计算题
|
较难
(0.4)
真题
【推荐1】白磷(P4)是磷的单质之一,易氧化,与卤素单质反应生成卤化磷。卤化磷通常有三卤化磷或五卤化磷,五卤化磷分子结构(以PCl5为例)如右图所示。该结构中氯原子有两种不同位置。
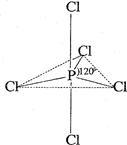
(1)6.20g白磷在足量氧气中完全燃烧生成氧化物,反应所消耗的氧气在标准状况下的体积为______________ L。上述燃烧产物溶于水配成50.0mL磷酸(H3PO4)溶液,该磷酸溶液的物质的量浓度为________________ mol·L-1。
(2)含0.300mol H3PO4的水溶液滴加到含0.500mol Ca(OH)2的悬浮液中,反应恰好完全,生成l种难溶盐和16.2g H2O。该难溶盐的化学式可表示为____________________ 。
(3)白磷和氯、溴反应,生成混合卤化磷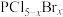 (
( ,且x为整数)。如果某混合卤化磷共有3种不同结构(分子中溴原子位置不完全相同的结构),该混合卤化磷的相对分子质量为
,且x为整数)。如果某混合卤化磷共有3种不同结构(分子中溴原子位置不完全相同的结构),该混合卤化磷的相对分子质量为____________________________ 。
(4)磷腈化合物含有3种元素,且分子中原子总数小于20。0.10mol PCl5和0.10mol NH4Cl恰好完全反应,生成氯化氢和0.030mol磷腈化合物。推算磷腈化合物的相对分子质量______ (提示:M>300)。

(1)6.20g白磷在足量氧气中完全燃烧生成氧化物,反应所消耗的氧气在标准状况下的体积为
(2)含0.300mol H3PO4的水溶液滴加到含0.500mol Ca(OH)2的悬浮液中,反应恰好完全,生成l种难溶盐和16.2g H2O。该难溶盐的化学式可表示为
(3)白磷和氯、溴反应,生成混合卤化磷
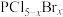 (
( ,且x为整数)。如果某混合卤化磷共有3种不同结构(分子中溴原子位置不完全相同的结构),该混合卤化磷的相对分子质量为
,且x为整数)。如果某混合卤化磷共有3种不同结构(分子中溴原子位置不完全相同的结构),该混合卤化磷的相对分子质量为(4)磷腈化合物含有3种元素,且分子中原子总数小于20。0.10mol PCl5和0.10mol NH4Cl恰好完全反应,生成氯化氢和0.030mol磷腈化合物。推算磷腈化合物的相对分子质量
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】SO2和CO2的混合气体38g ,测得CO2体积为11.2L(STP),则
(1)混合气体中SO2的质量是__________ g
(2)混合气体中SO2在标准状况下的体积是__________ L
(3)SO2和CO2同温同压下体积比是______________
(4)标准状况下混合气体的密度为____________ g/L
(1)混合气体中SO2的质量是
(2)混合气体中SO2在标准状况下的体积是
(3)SO2和CO2同温同压下体积比是
(4)标准状况下混合气体的密度为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐3】按要求进行计算。
(1)0.5mol C2H6O的质量是_______ 克,与_______ g H2O分子中的氢的原子数目相同。
(2)40.5g某金属氯化物 ,含有0.6mol氯离子,则金属R的相对原子质量
,含有0.6mol氯离子,则金属R的相对原子质量_______ 。
(3)20g A物质和14g B物质恰好完全反应,生成8.8g C物质、3.6g D物质和气体E(相对分子质量108),则标准状况下E的体积为_______ L。
(4)某溶液中仅含有H+、Al3+、Cl-、 四种离子,其中H+ 的浓度为0.5 mol·L-1, Cl-的浓度为0.2 mol·L-1,Al3+的浓度为0.1 mol·L-1,则
四种离子,其中H+ 的浓度为0.5 mol·L-1, Cl-的浓度为0.2 mol·L-1,Al3+的浓度为0.1 mol·L-1,则 的浓度是
的浓度是_______ mol·L-1。
(5)等质量的两份铝分别与适量的稀硫酸和NaOH溶液完全反应,若消耗两溶液的体积相同,则稀硫酸与NaOH溶液中溶质的物质的量浓度之比为_______ 。
(1)0.5mol C2H6O的质量是
(2)40.5g某金属氯化物
 ,含有0.6mol氯离子,则金属R的相对原子质量
,含有0.6mol氯离子,则金属R的相对原子质量(3)20g A物质和14g B物质恰好完全反应,生成8.8g C物质、3.6g D物质和气体E(相对分子质量108),则标准状况下E的体积为
(4)某溶液中仅含有H+、Al3+、Cl-、
 四种离子,其中H+ 的浓度为0.5 mol·L-1, Cl-的浓度为0.2 mol·L-1,Al3+的浓度为0.1 mol·L-1,则
四种离子,其中H+ 的浓度为0.5 mol·L-1, Cl-的浓度为0.2 mol·L-1,Al3+的浓度为0.1 mol·L-1,则 的浓度是
的浓度是(5)等质量的两份铝分别与适量的稀硫酸和NaOH溶液完全反应,若消耗两溶液的体积相同,则稀硫酸与NaOH溶液中溶质的物质的量浓度之比为
您最近一年使用:0次



