1 . 回答下列问题:
素材Ⅰ.“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为: ,结合素材回答问题(1)~(3):
,结合素材回答问题(1)~(3):
(1)该反应中 的摩尔质量是
的摩尔质量是________ 。
(2)28g铁粉中含有的Fe原子数是_______ 。
(3)若28g铁粉完全反应,析出Cu单质的物质的量为_______ 。
素材Ⅱ.宋代《洗冤集录》中记载有“银针探毒”,其原理是: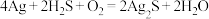 ,结合素材回答问题(4)~(5):
,结合素材回答问题(4)~(5):
(4)在相同条件下体积相同的 和
和 两种气体含有的原子数之比为
两种气体含有的原子数之比为_______ 。
(5)在0℃、101kPa条件下,11.2L氧气完全反应,消耗的 的体积是
的体积是_______ 。
素材Ⅲ.向空气中排放 会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
(6)该雨水中氢离子的浓度
________ 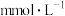 。
。
素材Ⅰ.“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为:
 ,结合素材回答问题(1)~(3):
,结合素材回答问题(1)~(3):(1)该反应中
 的摩尔质量是
的摩尔质量是(2)28g铁粉中含有的Fe原子数是
(3)若28g铁粉完全反应,析出Cu单质的物质的量为
素材Ⅱ.宋代《洗冤集录》中记载有“银针探毒”,其原理是:
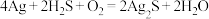 ,结合素材回答问题(4)~(5):
,结合素材回答问题(4)~(5):(4)在相同条件下体积相同的
 和
和 两种气体含有的原子数之比为
两种气体含有的原子数之比为(5)在0℃、101kPa条件下,11.2L氧气完全反应,消耗的
 的体积是
的体积是素材Ⅲ.向空气中排放
 会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:离子 |
|
|
|
|
|
浓度( | 0.06 | 0.08 | 0.02 | 0.04 | a |

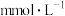 。
。
您最近一年使用:0次
名校
解题方法
2 . 完成下列小题
(1) 溶液含中,含
溶液含中,含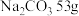 ,则该溶液中
,则该溶液中 的物质的量浓度
的物质的量浓度_____  。
。
(2)对于反应: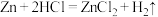 ,现有
,现有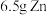 放入
放入 的
的 溶液中充分反应后,溶液中存在的溶质有
溶液中充分反应后,溶液中存在的溶质有_____ 。
(3)对于反应: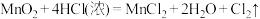 。
。
①用双线桥法表示上述反应电子转移的方向和数目_____ 。
②上述反应中还原剂是_____ ,若该反应有中有 电子转移,实际参加反应的
电子转移,实际参加反应的 质量
质量_____ g,生成氯在气在STP时体积是_____ L。
③若使用浓盐酸的质量分数0.365、密度 ,该浓盐酸物质的量浓度是
,该浓盐酸物质的量浓度是_____  。
。
(1)
 溶液含中,含
溶液含中,含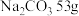 ,则该溶液中
,则该溶液中 的物质的量浓度
的物质的量浓度 。
。(2)对于反应:
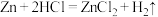 ,现有
,现有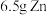 放入
放入 的
的 溶液中充分反应后,溶液中存在的溶质有
溶液中充分反应后,溶液中存在的溶质有(3)对于反应:
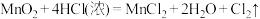 。
。①用双线桥法表示上述反应电子转移的方向和数目
②上述反应中还原剂是
 电子转移,实际参加反应的
电子转移,实际参加反应的 质量
质量③若使用浓盐酸的质量分数0.365、密度
 ,该浓盐酸物质的量浓度是
,该浓盐酸物质的量浓度是 。
。
您最近一年使用:0次
名校
解题方法
3 . 中国古代科学家在化学取得了非常多的成就。
素材I.“熬胆矾铁釜,久之亦化为铜”涉及到化学反应为: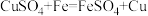 。
。
素材Ⅱ.宋代《洗冤集录》中记载有“银针探毒”,其原理是: 。
。
素材Ⅲ.我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为: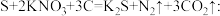 。回答下列问题:
。回答下列问题:
(1)该反应中 的摩尔质量是
的摩尔质量是___________ 。
(2) 铁粉中含有的
铁粉中含有的 原子数目为
原子数目为___________ 。
(3)若 铁粉完全反应,析出
铁粉完全反应,析出 单质的质量为
单质的质量为___________ 。
(4)在相同条件下体积相同的 和
和 两种气体分子数之比为
两种气体分子数之比为___________ 。
(5)“银针探毒”反应中, 完全反应时,消耗的
完全反应时,消耗的 的体积为
的体积为___________ L。
(6)黑火药反应中,化合价升高的元素是___________ (填元素符号)。
(7)黑火药反应中,作为氧化剂的物质是___________ (填化学式)。
(8)向空气中排放 会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
该雨水中氢离子的浓度a=___________ 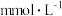 。
。
素材I.“熬胆矾铁釜,久之亦化为铜”涉及到化学反应为:
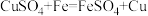 。
。素材Ⅱ.宋代《洗冤集录》中记载有“银针探毒”,其原理是:
 。
。素材Ⅲ.我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为:
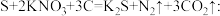 。回答下列问题:
。回答下列问题:(1)该反应中
 的摩尔质量是
的摩尔质量是(2)
 铁粉中含有的
铁粉中含有的 原子数目为
原子数目为(3)若
 铁粉完全反应,析出
铁粉完全反应,析出 单质的质量为
单质的质量为(4)在相同条件下体积相同的
 和
和 两种气体分子数之比为
两种气体分子数之比为(5)“银针探毒”反应中,
 完全反应时,消耗的
完全反应时,消耗的 的体积为
的体积为(6)黑火药反应中,化合价升高的元素是
(7)黑火药反应中,作为氧化剂的物质是
(8)向空气中排放
 会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:| 离子 |  |  |  |  |  |
浓度(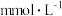 ) ) | 0.06 | 0.08 | 0.02 | 0.04 | a |
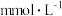 。
。
您最近一年使用:0次
名校
4 . 请根据要求回答下列问题:
(1)49g 的物质的量是
的物质的量是_______ mol,含_______ 个 分子,与
分子,与_______ mol NaOH恰好完全中和。
(2)在标准状况下,3.4g 所占的体积为
所占的体积为_______ L,它与标况下_______ L  所含的氢原子数目相同。
所含的氢原子数目相同。
(3)等质量的 和
和 ,它们的物质的量之比为
,它们的物质的量之比为_______ ,所含分子数之比为_______ ,所含原子数之比为_______ 。
(4)某气态氧化物的化学式为 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为_______ ,R的相对原子质量为_______ 。
(5)若a g某气体中含有的分子数为b个,则c g该气体在标准状况下的体积为_______ 。(设 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
(1)49g
 的物质的量是
的物质的量是 分子,与
分子,与(2)在标准状况下,3.4g
 所占的体积为
所占的体积为 所含的氢原子数目相同。
所含的氢原子数目相同。(3)等质量的
 和
和 ,它们的物质的量之比为
,它们的物质的量之比为(4)某气态氧化物的化学式为
 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为(5)若a g某气体中含有的分子数为b个,则c g该气体在标准状况下的体积为
 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
您最近一年使用:0次
解题方法
5 . 把11.2 L(标准状况)HCl气体溶于水,配制成250mL的溶液,求:
(1)该溶液的物质的量浓度_____
(2)将该溶液与足量的锌反应,在标准状况下,能生成多少升的H2_____ ? (反应的化学方程式为 Zn + 2HCl = ZnCl2 + H2↑)
(1)该溶液的物质的量浓度
(2)将该溶液与足量的锌反应,在标准状况下,能生成多少升的H2
您最近一年使用:0次
名校
解题方法
6 . 回答下列问题(用NA表示阿伏加德罗常数的值)
(1)9.03 1023个CO2在标准状况下的体积为
1023个CO2在标准状况下的体积为_______ ,质量是_______ 。
(2)3.4gNH3与标准状况下的_______ L的H2S含有相同数目的氢原子。
(3)在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示。

该混合液中CaCl2的物质的量为_______ ;
(4)现有14.4gCO和CO2的混合气体,在标准状况下其体积为8.96L。回答问题:
①该混合气体的平均摩尔质量为_______ 。
②混合气体中碳原子的个数为_______ 。
(1)9.03
 1023个CO2在标准状况下的体积为
1023个CO2在标准状况下的体积为(2)3.4gNH3与标准状况下的
(3)在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示。

该混合液中CaCl2的物质的量为
(4)现有14.4gCO和CO2的混合气体,在标准状况下其体积为8.96L。回答问题:
①该混合气体的平均摩尔质量为
②混合气体中碳原子的个数为
您最近一年使用:0次
名校
解题方法
7 . 填空
(1)在标准状况下,3.4g NH3所占的体积为_______ L,它与标况下_______ L H2S所含的氢原子数目相同。
(2)200 mL溶液中,含Na2CO3 53 g,则该溶液中Na2CO3 的物质的量浓度_______ mol/L,Na+的物质的量浓度_______ mol/L。
(3)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是_______ 。(用X、Y表示)
(4)对于反应:Zn+2HCl=ZnCl2+H2↑,现有26 g Zn放入200mL2mol/L的HCl溶液中,此反应中_______ (填Zn或HCl)过量,该反应可生成氢气在标准状况时体积是_______ 。
(1)在标准状况下,3.4g NH3所占的体积为
(2)200 mL溶液中,含Na2CO3 53 g,则该溶液中Na2CO3 的物质的量浓度
(3)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是
(4)对于反应:Zn+2HCl=ZnCl2+H2↑,现有26 g Zn放入200mL2mol/L的HCl溶液中,此反应中
您最近一年使用:0次
名校
解题方法
8 . 配平以下方程式并用单线桥法标出下列反应电子转移的方向和数目。(若系数为“1”,请标出)
(1)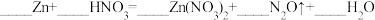
_______ 。
(2)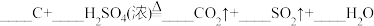
_______ 。
(3)
_______ 。
(4)
_______ 。
(5)
_______ 。
(6)
_______ 。
(1)
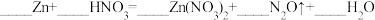
(2)
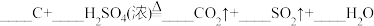
(3)

(4)

(5)

(6)

您最近一年使用:0次
名校
9 . 设NA为阿伏加德罗常数的值,回答下列问题:
(1)0.3molNH3分子中所含原子数与_______ 个H2O分子中所含原子数相等。
(2)某气体在标准状况下的密度为1.25g·L-1,则14g该气体所含有的分子数为_______ 。
(3)同温同压下,同体积的H2和A气体的质量分别为1.0g和16.0g,则A的摩尔质量为_______ 。
(4)从400mL2.0mol·L-1的Al2(SO4)3溶液中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中SO 的物质的量浓度为
的物质的量浓度为_______ 。
(5)某结晶水合物的化学式为R·nH2O,该结晶水合物的摩尔质量为Mg·mol-1,25℃时ag该结晶水合物晶体能够溶于bg水中,形成密度为ρg/mL的溶液,则:
①该溶液中溶质的质量分数为_______ 。
②该溶液中溶质的物质的量浓度为_______ 。
(1)0.3molNH3分子中所含原子数与
(2)某气体在标准状况下的密度为1.25g·L-1,则14g该气体所含有的分子数为
(3)同温同压下,同体积的H2和A气体的质量分别为1.0g和16.0g,则A的摩尔质量为
(4)从400mL2.0mol·L-1的Al2(SO4)3溶液中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中SO
 的物质的量浓度为
的物质的量浓度为(5)某结晶水合物的化学式为R·nH2O,该结晶水合物的摩尔质量为Mg·mol-1,25℃时ag该结晶水合物晶体能够溶于bg水中,形成密度为ρg/mL的溶液,则:
①该溶液中溶质的质量分数为
②该溶液中溶质的物质的量浓度为
您最近一年使用:0次
10 . 碳及其化合物在生产、生活中广泛存在。请回答下列问题:
(1)已知某温度下某反应 的化学平衡常数表达式为 K=
的化学平衡常数表达式为 K=_______ 。
(2)已知在一定温度下,
①
 平衡常数
平衡常数
②
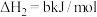 平衡常数
平衡常数
③
 平衡常数
平衡常数
则 、
、 、
、 之间的关系是
之间的关系是
_______ ,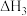 =
=_______  用含a、b的代数式表示
用含a、b的代数式表示 。
。
(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应: ;该反应平衡常数随温度的变化如表所示:
;该反应平衡常数随温度的变化如表所示:
该反应的正反应方向是_______ 反应 填“吸热”或“放热”
填“吸热”或“放热” ,若在500℃时进行,设起始时CO和H2O起始浓度均为0.02mol/L,在该条件下,CO的平衡转化率为
,若在500℃时进行,设起始时CO和H2O起始浓度均为0.02mol/L,在该条件下,CO的平衡转化率为_______ 。
(4)电化学法还原二氧化碳为乙烯原理如下图所示。

A为电源的_______ 极(填“正”或“负”),阴极电极反应式为_______ 。电路中转移0.2 mol 电子,理论上产生氧气_______ L(标准状况)。
(1)已知某温度下某反应
 的化学平衡常数表达式为 K=
的化学平衡常数表达式为 K=(2)已知在一定温度下,
①

 平衡常数
平衡常数
②

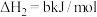 平衡常数
平衡常数
③

 平衡常数
平衡常数
则
 、
、 、
、 之间的关系是
之间的关系是
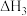 =
= 用含a、b的代数式表示
用含a、b的代数式表示 。
。(3)煤化工通常通过研究不同温度下平衡常数以解决各种实际问题。已知等体积的一氧化碳和水蒸气进入反应器时,发生如下反应:
 ;该反应平衡常数随温度的变化如表所示:
;该反应平衡常数随温度的变化如表所示:温度 | 400 | 500 | 800 |
| 平衡常数K |  | 9 | 1 |
 填“吸热”或“放热”
填“吸热”或“放热” ,若在500℃时进行,设起始时CO和H2O起始浓度均为0.02mol/L,在该条件下,CO的平衡转化率为
,若在500℃时进行,设起始时CO和H2O起始浓度均为0.02mol/L,在该条件下,CO的平衡转化率为(4)电化学法还原二氧化碳为乙烯原理如下图所示。

A为电源的
您最近一年使用:0次







