(1)用KMnO4氧化盐酸溶液,反应方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,若产生的Cl2在标准状况下体积为56L,计算:参加反应的HCl的物质的量_______ 反应中被氧化的HCl的物质的量_______
(2)向某硝酸银溶液中,逐滴加入密度为1.10g·mL-1的盐酸溶液,恰好完全反应时,过滤所得沉淀的质量恰好与盐酸溶液的质量相等。求盐酸的质量分数_______ (需要过程)。
(2)向某硝酸银溶液中,逐滴加入密度为1.10g·mL-1的盐酸溶液,恰好完全反应时,过滤所得沉淀的质量恰好与盐酸溶液的质量相等。求盐酸的质量分数
更新时间:2021-04-03 18:18:10
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】有氯化钠、碳酸钠、碳酸氢钠的固体混合物共4克,加热到质量不再减少为止。此时剩余固体质量为3.38克,在残留的固体中加入足量盐酸,将产生的气体通过干燥管后,通入澄清石灰水中,生成2g固体。
(1)原混合物中碳酸氢钠的物质的量是___________ 。
(2)原混合物中碳酸钠的质量是多少?(写出具体计算过程)___________
(1)原混合物中碳酸氢钠的物质的量是
(2)原混合物中碳酸钠的质量是多少?(写出具体计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】实验室常利用反应:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O来制取NO,当有6.4gCu参加反应时,计算:
(1)用双线桥法标出电子转移的方向和数目;___________
(2)能生成_______ 升NO(标准状况下);
(3)使生成的Cu(NO3)2中Cu2+全部转化成沉淀,则至少需要质量分数为40%密度为1.42g/mL的NaOH溶液体积______ 。
(1)用双线桥法标出电子转移的方向和数目;
(2)能生成
(3)使生成的Cu(NO3)2中Cu2+全部转化成沉淀,则至少需要质量分数为40%密度为1.42g/mL的NaOH溶液体积
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】将32.64g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和 混合气体在标准状况下的体积为11.2L。请回答:
混合气体在标准状况下的体积为11.2L。请回答:
(1)求NO和 混合气体的平均摩尔质量
混合气体的平均摩尔质量_______ 。
(2)待产生的气体全部释放后,向溶液加入V mL浓度为a mol/L的NaOH溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为___________ mol/L。
(3)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为 ,至少需要30%的过氧化氢
,至少需要30%的过氧化氢___________ g。
 混合气体在标准状况下的体积为11.2L。请回答:
混合气体在标准状况下的体积为11.2L。请回答:(1)求NO和
 混合气体的平均摩尔质量
混合气体的平均摩尔质量(2)待产生的气体全部释放后,向溶液加入V mL浓度为a mol/L的NaOH溶液,恰好使溶液中的
 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为(3)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为
 ,至少需要30%的过氧化氢
,至少需要30%的过氧化氢
您最近一年使用:0次
【推荐2】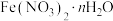 可用作媒染剂、医药、分析试剂、催化剂等,某同学设计实验确定其结晶水数目。用电子天平称取样品17.280g,一定条件下,经热分解测得气体产物中有
可用作媒染剂、医药、分析试剂、催化剂等,某同学设计实验确定其结晶水数目。用电子天平称取样品17.280g,一定条件下,经热分解测得气体产物中有 、
、 、
、 、
、 ,其中水的质量为6.300g,残留的固体产物是
,其中水的质量为6.300g,残留的固体产物是 ,质量为4.800g。
,质量为4.800g。
(1)n=_______ (写出计算过程)。
(2)在标准状况下气体产物中 的体积为
的体积为_______ L。
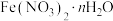 可用作媒染剂、医药、分析试剂、催化剂等,某同学设计实验确定其结晶水数目。用电子天平称取样品17.280g,一定条件下,经热分解测得气体产物中有
可用作媒染剂、医药、分析试剂、催化剂等,某同学设计实验确定其结晶水数目。用电子天平称取样品17.280g,一定条件下,经热分解测得气体产物中有 、
、 、
、 、
、 ,其中水的质量为6.300g,残留的固体产物是
,其中水的质量为6.300g,残留的固体产物是 ,质量为4.800g。
,质量为4.800g。(1)n=
(2)在标准状况下气体产物中
 的体积为
的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】1.52g 铜镁合金完全溶解于50mL 密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。则
(1)该合金中铜与镁的物质的量之比是__________
(2)该浓硝酸中HNO3的物质的量浓度是___________ mol/L
(3)NO2和N2O4的混合气体中,NO2的体积分数是_____________
(4)得到2.54 g沉淀时,加入NaOH溶液的体积是______ mL
(1)该合金中铜与镁的物质的量之比是
(2)该浓硝酸中HNO3的物质的量浓度是
(3)NO2和N2O4的混合气体中,NO2的体积分数是
(4)得到2.54 g沉淀时,加入NaOH溶液的体积是
您最近一年使用:0次

 和
和 混合物溶液与过量盐酸反应,生成2.016L
混合物溶液与过量盐酸反应,生成2.016L (标况下),然后加入足量的
(标况下),然后加入足量的 溶液,得到沉淀的质量为2.33g。
溶液,得到沉淀的质量为2.33g。

