制取SO2的方程式为: ,将12.6g Na2SO3与足量浓硫酸反应,求制得标准状况下SO2的体积
,将12.6g Na2SO3与足量浓硫酸反应,求制得标准状况下SO2的体积
更新时间:2024-03-25 16:18:25
|
相似题推荐
【推荐1】将2.3克Na溶于水中,得到体积为1L的溶液,求
(1)生成的H2在标况下的体积为多少______ 。
(2)此溶液中溶质的物质的量浓度为多少______ 。
(3)2.3克Na完全反应后转移的电子数目为多少______ 。
(1)生成的H2在标况下的体积为多少
(2)此溶液中溶质的物质的量浓度为多少
(3)2.3克Na完全反应后转移的电子数目为多少
您最近一年使用:0次
【推荐2】向 和
和 的混合溶液中加入过量的
的混合溶液中加入过量的 溶液,得到
溶液,得到 白色沉淀,向白色沉淀中再加入过量的稀
白色沉淀,向白色沉淀中再加入过量的稀 ,充分反应后,沉淀减少到
,充分反应后,沉淀减少到 ,并有气体产生。
,并有气体产生。
(1)原混合物溶液中 和
和 的物质的量各是多少
的物质的量各是多少____ ?
(2)产生的气体在标准状况下的体积是多少升____ ?
 和
和 的混合溶液中加入过量的
的混合溶液中加入过量的 溶液,得到
溶液,得到 白色沉淀,向白色沉淀中再加入过量的稀
白色沉淀,向白色沉淀中再加入过量的稀 ,充分反应后,沉淀减少到
,充分反应后,沉淀减少到 ,并有气体产生。
,并有气体产生。(1)原混合物溶液中
 和
和 的物质的量各是多少
的物质的量各是多少(2)产生的气体在标准状况下的体积是多少升
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐1】硫化钠是由无水硫酸钠与炭粉在高温下反应制得,反应的化学方程式为:①Na2SO4+4C Na2S+4CO↑;②Na2SO4+4CO
Na2S+4CO↑;②Na2SO4+4CO Na2S+4CO2↑。要制取15.6gNa2S,需原料芒硝(Na2SO4•10H2O)
Na2S+4CO2↑。要制取15.6gNa2S,需原料芒硝(Na2SO4•10H2O)_______ mol。
 Na2S+4CO↑;②Na2SO4+4CO
Na2S+4CO↑;②Na2SO4+4CO Na2S+4CO2↑。要制取15.6gNa2S,需原料芒硝(Na2SO4•10H2O)
Na2S+4CO2↑。要制取15.6gNa2S,需原料芒硝(Na2SO4•10H2O)
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐2】完成以下计算。
(1)12.4gNa2X中含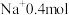 ,则
,则 的摩尔质量是
的摩尔质量是_______ 。
(2)标况下5.6L的CO2含有的电子数为_______ (用NA表示)。
(3)常温下,将20.0g14.0%的NaCl溶液,跟30.0g24.0%的NaCl溶液混合,得到密度为1.158g·cm-3的混合溶液。计算混合溶液中溶质的物质的量浓度:_______ (保留三位有效数字)
(4)将适量碳酸钙投入2L的盐酸中,恰好完全反应,标准状况下生成11.2LCO2,求碳酸钙的质量和盐酸的物质的量浓度_______ 。(写出计算过程和结果)
(1)12.4gNa2X中含
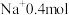 ,则
,则 的摩尔质量是
的摩尔质量是(2)标况下5.6L的CO2含有的电子数为
(3)常温下,将20.0g14.0%的NaCl溶液,跟30.0g24.0%的NaCl溶液混合,得到密度为1.158g·cm-3的混合溶液。计算混合溶液中溶质的物质的量浓度:
(4)将适量碳酸钙投入2L的盐酸中,恰好完全反应,标准状况下生成11.2LCO2,求碳酸钙的质量和盐酸的物质的量浓度
您最近一年使用:0次



