名校
解题方法
1 . 完成下列小题
(1) 溶液含中,含
溶液含中,含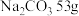 ,则该溶液中
,则该溶液中 的物质的量浓度
的物质的量浓度_____  。
。
(2)对于反应: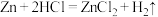 ,现有
,现有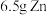 放入
放入 的
的 溶液中充分反应后,溶液中存在的溶质有
溶液中充分反应后,溶液中存在的溶质有_____ 。
(3)对于反应: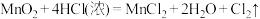 。
。
①用双线桥法表示上述反应电子转移的方向和数目_____ 。
②上述反应中还原剂是_____ ,若该反应有中有 电子转移,实际参加反应的
电子转移,实际参加反应的 质量
质量_____ g,生成氯在气在STP时体积是_____ L。
③若使用浓盐酸的质量分数0.365、密度 ,该浓盐酸物质的量浓度是
,该浓盐酸物质的量浓度是_____  。
。
(1)
 溶液含中,含
溶液含中,含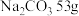 ,则该溶液中
,则该溶液中 的物质的量浓度
的物质的量浓度 。
。(2)对于反应:
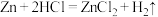 ,现有
,现有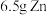 放入
放入 的
的 溶液中充分反应后,溶液中存在的溶质有
溶液中充分反应后,溶液中存在的溶质有(3)对于反应:
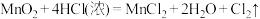 。
。①用双线桥法表示上述反应电子转移的方向和数目
②上述反应中还原剂是
 电子转移,实际参加反应的
电子转移,实际参加反应的 质量
质量③若使用浓盐酸的质量分数0.365、密度
 ,该浓盐酸物质的量浓度是
,该浓盐酸物质的量浓度是 。
。
您最近一年使用:0次
2 . 请回答下列问题:
(1)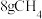 的物质的量是
的物质的量是________ mol,含有_______ 个甲烷分子,______ 个电子。
(2)在一定温度和压强下,0.2mol空气的体积为4.5L,则该条件下的气体摩尔体积________ 。
(3)某气体氧化物的化学式为 ,在标准状况下,1.92g该氧化物的体积为672mL,则该R的摩尔质量为
,在标准状况下,1.92g该氧化物的体积为672mL,则该R的摩尔质量为___________ 。
(4)某混合盐溶液中含有离子: 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则
___________  。
。
(5)标准状况下,密度为1.25g/L的 与
与 组成的混合气体中,该混合气体的平均相对分子质量为
组成的混合气体中,该混合气体的平均相对分子质量为___________ , 的体积分数为
的体积分数为___________ 。
(1)
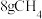 的物质的量是
的物质的量是(2)在一定温度和压强下,0.2mol空气的体积为4.5L,则该条件下的气体摩尔体积
(3)某气体氧化物的化学式为
 ,在标准状况下,1.92g该氧化物的体积为672mL,则该R的摩尔质量为
,在标准状况下,1.92g该氧化物的体积为672mL,则该R的摩尔质量为(4)某混合盐溶液中含有离子:
 、
、 、
、 、
、 ,测得
,测得 、
、 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: 、
、 、
、 ,则
,则
 。
。(5)标准状况下,密度为1.25g/L的
 与
与 组成的混合气体中,该混合气体的平均相对分子质量为
组成的混合气体中,该混合气体的平均相对分子质量为 的体积分数为
的体积分数为
您最近一年使用:0次
3 . 根据已知,回答下列问题。
(1)在 、
、 下,
下, 甲烷燃烧生成
甲烷燃烧生成 和液态水时放热
和液态水时放热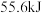 。则表示甲烷燃烧热的热化学方程式为
。则表示甲烷燃烧热的热化学方程式为______ 。
(2)常温常压下,断裂 (理想)气体分子化学键所吸收的能量或形成
(理想)气体分子化学键所吸收的能量或形成 (理想)气体分子化学键所放出的能量称为键能,下表是一些键能数
(理想)气体分子化学键所放出的能量称为键能,下表是一些键能数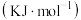
根据键能数据计算以下反应的反应热: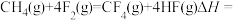
______ 。
(3)随着科学技术的进步,人们研制了多种甲醇质子交换膜燃料电池,以满足不同的需求。有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是
A.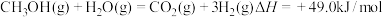
B.
由上述方程式可知, 的燃烧热
的燃烧热______ (填“大于”、“等于”或“小于”)
(4)火箭的常规燃料是液态四氧化二氮和液态肼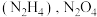 作氧化剂,有人认为若用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
作氧化剂,有人认为若用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
已知:


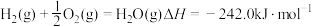
请写出肼和氟气反应的热化学方程式:______ 。
(1)在
 、
、 下,
下, 甲烷燃烧生成
甲烷燃烧生成 和液态水时放热
和液态水时放热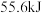 。则表示甲烷燃烧热的热化学方程式为
。则表示甲烷燃烧热的热化学方程式为(2)常温常压下,断裂
 (理想)气体分子化学键所吸收的能量或形成
(理想)气体分子化学键所吸收的能量或形成 (理想)气体分子化学键所放出的能量称为键能,下表是一些键能数
(理想)气体分子化学键所放出的能量称为键能,下表是一些键能数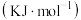
化学键 | 键能 | 化学键 | 键能 | 化学键 | 键能 |
C-H | 414 | C-F | 489 | H-F | 565 |
| 436 |
| 391 |
| 158 |
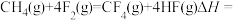
(3)随着科学技术的进步,人们研制了多种甲醇质子交换膜燃料电池,以满足不同的需求。有一类甲醇质子交换膜燃料电池,需将甲醇蒸气转化为氢气,两种反应原理是
A.
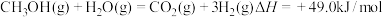
B.

由上述方程式可知,
 的燃烧热
的燃烧热
(4)火箭的常规燃料是液态四氧化二氮和液态肼
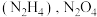 作氧化剂,有人认为若用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
作氧化剂,有人认为若用氟气代替四氧化二氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。已知:


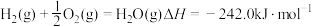
请写出肼和氟气反应的热化学方程式:
您最近一年使用:0次
名校
4 . 电解饱和食盐水的化学反应方程式为 ,现电解消耗
,现电解消耗 的质量为
的质量为 ,完全反应后,测得烧杯中剩余溶液的质量是
,完全反应后,测得烧杯中剩余溶液的质量是 ,请计算:
,请计算:
(1)求消耗的 的物质的量
的物质的量_______ 。
(2)求生成的 在标准状况下的体积
在标准状况下的体积_______ 。
(3)求生成的 的质量
的质量_______ 。
(4)反应后所得 溶液的溶质质量分数
溶液的溶质质量分数_______ 。
 ,现电解消耗
,现电解消耗 的质量为
的质量为 ,完全反应后,测得烧杯中剩余溶液的质量是
,完全反应后,测得烧杯中剩余溶液的质量是 ,请计算:
,请计算:(1)求消耗的
 的物质的量
的物质的量(2)求生成的
 在标准状况下的体积
在标准状况下的体积(3)求生成的
 的质量
的质量(4)反应后所得
 溶液的溶质质量分数
溶液的溶质质量分数
您最近一年使用:0次
名校
解题方法
5 . 中国古代科学家在化学取得了非常多的成就。
素材I.“熬胆矾铁釜,久之亦化为铜”涉及到化学反应为: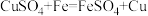 。
。
素材Ⅱ.宋代《洗冤集录》中记载有“银针探毒”,其原理是: 。
。
素材Ⅲ.我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为: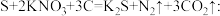 。回答下列问题:
。回答下列问题:
(1)该反应中 的摩尔质量是
的摩尔质量是___________ 。
(2) 铁粉中含有的
铁粉中含有的 原子数目为
原子数目为___________ 。
(3)若 铁粉完全反应,析出
铁粉完全反应,析出 单质的质量为
单质的质量为___________ 。
(4)在相同条件下体积相同的 和
和 两种气体分子数之比为
两种气体分子数之比为___________ 。
(5)“银针探毒”反应中, 完全反应时,消耗的
完全反应时,消耗的 的体积为
的体积为___________ L。
(6)黑火药反应中,化合价升高的元素是___________ (填元素符号)。
(7)黑火药反应中,作为氧化剂的物质是___________ (填化学式)。
(8)向空气中排放 会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
该雨水中氢离子的浓度a=___________ 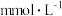 。
。
素材I.“熬胆矾铁釜,久之亦化为铜”涉及到化学反应为:
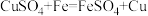 。
。素材Ⅱ.宋代《洗冤集录》中记载有“银针探毒”,其原理是:
 。
。素材Ⅲ.我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为:
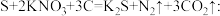 。回答下列问题:
。回答下列问题:(1)该反应中
 的摩尔质量是
的摩尔质量是(2)
 铁粉中含有的
铁粉中含有的 原子数目为
原子数目为(3)若
 铁粉完全反应,析出
铁粉完全反应,析出 单质的质量为
单质的质量为(4)在相同条件下体积相同的
 和
和 两种气体分子数之比为
两种气体分子数之比为(5)“银针探毒”反应中,
 完全反应时,消耗的
完全反应时,消耗的 的体积为
的体积为(6)黑火药反应中,化合价升高的元素是
(7)黑火药反应中,作为氧化剂的物质是
(8)向空气中排放
 会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:| 离子 |  |  |  |  |  |
浓度(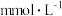 ) ) | 0.06 | 0.08 | 0.02 | 0.04 | a |
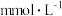 。
。
您最近一年使用:0次
名校
解题方法
6 . 将15.6g表面已被氧化的铝片投入300mL的稀硫酸中,恰好完全反应,产生标准状况下H2的体积为6.72L。计算下列问题并写出过程。
(1)铝片中Al和Al2O3的物质的量______ ;
(2)稀硫酸的物质的量浓度______ ;
(3)若该稀硫酸用18.0mol/L的浓硫酸配制,求所需浓硫酸的体积为______ ?
(1)铝片中Al和Al2O3的物质的量
(2)稀硫酸的物质的量浓度
(3)若该稀硫酸用18.0mol/L的浓硫酸配制,求所需浓硫酸的体积为
您最近一年使用:0次
7 . 物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)标准状况下,含有相同氧原子数的 和
和 的体积之比为
的体积之比为_____ 。
(2)某气体氧化物的化学式为 ,在标准状况下,
,在标准状况下, 该气体的体积为
该气体的体积为 ,则该氧化物的摩尔质量为
,则该氧化物的摩尔质量为_____ 。
(3)某混合溶液中含有离子: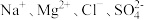 ,测得
,测得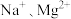 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: ,则
,则
_____  。
。
(4)一瓶 的某品牌矿泉水中部分天然矿物质含量如下:
的某品牌矿泉水中部分天然矿物质含量如下: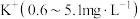 ,
, ,
, ,
, ,一瓶合格的这种矿泉水中
,一瓶合格的这种矿泉水中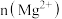 不能超过
不能超过_____  。
。
(1)标准状况下,含有相同氧原子数的
 和
和 的体积之比为
的体积之比为(2)某气体氧化物的化学式为
 ,在标准状况下,
,在标准状况下, 该气体的体积为
该气体的体积为 ,则该氧化物的摩尔质量为
,则该氧化物的摩尔质量为(3)某混合溶液中含有离子:
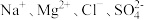 ,测得
,测得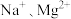 和
和 的物质的量浓度依次为:
的物质的量浓度依次为: ,则
,则
 。
。(4)一瓶
 的某品牌矿泉水中部分天然矿物质含量如下:
的某品牌矿泉水中部分天然矿物质含量如下: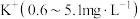 ,
, ,
, ,
, ,一瓶合格的这种矿泉水中
,一瓶合格的这种矿泉水中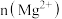 不能超过
不能超过 。
。
您最近一年使用:0次
8 . 利用太阳能光解水,制备的H2用于还原CO2合成有机物甲醇(CH3OH),可实现资源的再利用。回答下列问题:
(1)CH3OH的摩尔质量是___________ g∙mol-1。
(2)2mol CO2中所含原子的物质的量为___________ mol。
(3)___________ g的氢气中所含H原子的数目与1mol CH3OH相同。
(4)含0.1NA个O的CO2中有___________ 个电子,标准状况下该CO2的体积为___________ L。
(5)在标准状况下,H2和CO2的混合气体共11.2 L,质量为13.6 g,其中H2为___________ mol。
(1)CH3OH的摩尔质量是
(2)2mol CO2中所含原子的物质的量为
(3)
(4)含0.1NA个O的CO2中有
(5)在标准状况下,H2和CO2的混合气体共11.2 L,质量为13.6 g,其中H2为
您最近一年使用:0次
解题方法
9 . I.碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质,请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:

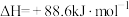
则M、N相比,较稳定的是___________ 。
(2)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,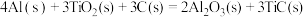
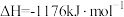 ,则反应过程中,每转移
,则反应过程中,每转移 电子放出的热量为
电子放出的热量为___________ kJ。
(3) 、
、 、C都是优质的能源物质,它们燃烧的热化学方程式分别为
、C都是优质的能源物质,它们燃烧的热化学方程式分别为
①
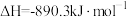 ;
;
②
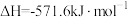 ;
;
③
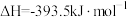 ;
;
已知 、
、 组成的混合气体
组成的混合气体 ,又
,又 与
与 的物质的量之比
的物质的量之比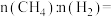 3:2,则该混合气体完全燃烧后放出的热量为
3:2,则该混合气体完全燃烧后放出的热量为___________ kJ; 的反应热无法直接测量,但通过上述反应可求出其反应热
的反应热无法直接测量,但通过上述反应可求出其反应热
___________  。
。
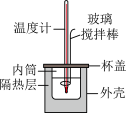
II. 的盐酸与
的盐酸与 的
的 溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和反应反应热,回答下列问题:
溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和反应反应热,回答下列问题:
(4)实验中若改用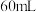
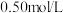 的盐酸与
的盐酸与
 的氢氧化钠溶液进行反应,若实验操作均正确,则所求中和热
的氢氧化钠溶液进行反应,若实验操作均正确,则所求中和热___________ (填“相等”或“不相等”)。
(5)下列说法正确的是___________(填字母)。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:

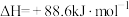
则M、N相比,较稳定的是
(2)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,
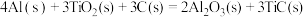
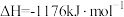 ,则反应过程中,每转移
,则反应过程中,每转移 电子放出的热量为
电子放出的热量为(3)
 、
、 、C都是优质的能源物质,它们燃烧的热化学方程式分别为
、C都是优质的能源物质,它们燃烧的热化学方程式分别为①

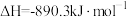 ;
;②

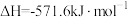 ;
;③

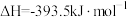 ;
;已知
 、
、 组成的混合气体
组成的混合气体 ,又
,又 与
与 的物质的量之比
的物质的量之比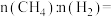 3:2,则该混合气体完全燃烧后放出的热量为
3:2,则该混合气体完全燃烧后放出的热量为 的反应热无法直接测量,但通过上述反应可求出其反应热
的反应热无法直接测量,但通过上述反应可求出其反应热
 。
。II.
 的盐酸与
的盐酸与 的
的 溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和反应反应热,回答下列问题:
溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和反应反应热,回答下列问题:
(4)实验中若改用
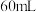
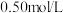 的盐酸与
的盐酸与
 的氢氧化钠溶液进行反应,若实验操作均正确,则所求中和热
的氢氧化钠溶液进行反应,若实验操作均正确,则所求中和热(5)下列说法正确的是___________(填字母)。
| A.玻璃搅拌棒可用铜丝搅拌棒替代 |
| B.向内筒中加入稀碱时,应当缓慢而匀速地加入 |
| C.实验中如果用相同体积、相同浓度的醋酸代替盐酸,测得的中和热数值将偏小 |
| D.将用量筒量取好的稀盐酸加入内筒后,应当快速用水冲洗量筒内壁剩余的稀盐酸至内筒中,以免造成测量误差 |
您最近一年使用:0次
10 . 物质的量是联系宏观和微观的桥梁:某三原子分子构成的气体,其摩尔质量为44g/mol,该气体质量为11g,则:
(1)①该气体的物质的量为___________ ;
②该气体在标准状况下的体积约为___________ ;
③该气体所含原子总数为___________ 个;
(2)电子数为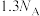 的Al的质量为
的Al的质量为___________ g;
(3)在27.2g某二价金属的氯化物中含有 ,该金属元素的相对原子质量为
,该金属元素的相对原子质量为________ ;
(4)同温同压下同体积的 和
和 (g)所含原子个数比为
(g)所含原子个数比为___________ ;
(5)某 溶液500mL含
溶液500mL含 ,该溶液的物质的量浓度是
,该溶液的物质的量浓度是___________ 。
(1)①该气体的物质的量为
②该气体在标准状况下的体积约为
③该气体所含原子总数为
(2)电子数为
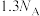 的Al的质量为
的Al的质量为(3)在27.2g某二价金属的氯化物中含有
 ,该金属元素的相对原子质量为
,该金属元素的相对原子质量为(4)同温同压下同体积的
 和
和 (g)所含原子个数比为
(g)所含原子个数比为(5)某
 溶液500mL含
溶液500mL含 ,该溶液的物质的量浓度是
,该溶液的物质的量浓度是
您最近一年使用:0次






