名校
解题方法
1 . 完成下列问题
(1)8 g CH4在标准状况下所占的体积约为_______ L。
(2)20g重水(D2O)中所含中子数目为_______ 。
(3)10.8g R2O5中氧原子数目为3.01×1023 ,则元素R的相对原子质量为_______ 。
(4)向10.0mL1.00mol·L-1 Na2CO3溶液加水稀释至100mL溶液,此时溶液中Na+的物质的量浓度为_______ 。
(5)实验室常用邻苯二甲酸氢钾(KHC8H4O4)来标定氢氧化钠溶液的浓度,其操作过程为:准确称取4.080g邻苯二甲酸氢钾,加水配成溶液,向溶液中加入1~2滴指示剂,用氢氧化钠溶液滴定至终点,消耗氢氧化钠溶液19.60mL。该氢氧化钠溶液的物质的量浓度为_______ 。(已知:KHC8H4O4+NaOH=KNaC8H4O4+H2O)
(6)100g质量分数为46%的酒精(CH3CH2OH)溶液中氧原子的物质的量为_______ 。
(1)8 g CH4在标准状况下所占的体积约为
(2)20g重水(D2O)中所含中子数目为
(3)10.8g R2O5中氧原子数目为3.01×1023 ,则元素R的相对原子质量为
(4)向10.0mL1.00mol·L-1 Na2CO3溶液加水稀释至100mL溶液,此时溶液中Na+的物质的量浓度为
(5)实验室常用邻苯二甲酸氢钾(KHC8H4O4)来标定氢氧化钠溶液的浓度,其操作过程为:准确称取4.080g邻苯二甲酸氢钾,加水配成溶液,向溶液中加入1~2滴指示剂,用氢氧化钠溶液滴定至终点,消耗氢氧化钠溶液19.60mL。该氢氧化钠溶液的物质的量浓度为
(6)100g质量分数为46%的酒精(CH3CH2OH)溶液中氧原子的物质的量为
您最近一年使用:0次
名校
2 . 含有 个HCl分子,物质的量是
个HCl分子,物质的量是_______ mol,在标准状况下的体积是_______ 升,溶于水得到50mL盐酸溶液,物质的量浓度是_______  ,加入足量的
,加入足量的 粉末,生成的
粉末,生成的 全部通入足量NaOH溶液中,溶液增重
全部通入足量NaOH溶液中,溶液增重_______ 克。
 个HCl分子,物质的量是
个HCl分子,物质的量是 ,加入足量的
,加入足量的 粉末,生成的
粉末,生成的 全部通入足量NaOH溶液中,溶液增重
全部通入足量NaOH溶液中,溶液增重
您最近一年使用:0次
名校
3 . 填写下列空白:
(1)含有 个
个 的
的 ,则
,则 的物质的量为
的物质的量为_______ 。
(2)_______  中含有的氧原子数与标准状况下
中含有的氧原子数与标准状况下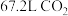 中含有的氧原子数相等。
中含有的氧原子数相等。
(3)同温同压下, 和
和 体积比为4∶3,它们的质量之比为
体积比为4∶3,它们的质量之比为_______ 。
(4)已知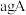 和
和 恰好完全反应生成
恰好完全反应生成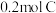 和
和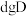 ,则C的摩尔质量为
,则C的摩尔质量为_______ 。
(1)含有
 个
个 的
的 ,则
,则 的物质的量为
的物质的量为(2)
 中含有的氧原子数与标准状况下
中含有的氧原子数与标准状况下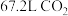 中含有的氧原子数相等。
中含有的氧原子数相等。(3)同温同压下,
 和
和 体积比为4∶3,它们的质量之比为
体积比为4∶3,它们的质量之比为(4)已知
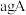 和
和 恰好完全反应生成
恰好完全反应生成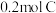 和
和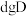 ,则C的摩尔质量为
,则C的摩尔质量为
您最近一年使用:0次
解题方法
4 . 回答下列问题:
(1)6.02×1024个Na+约含_________ mol Na+,其质量为____________ g;
(2)4.5molCH4约含有_____________ 个CH4,其质量为________ g;
(3)49gH2SO4约含有____________ 个H,共含有_______ mol原子。
(1)6.02×1024个Na+约含
(2)4.5molCH4约含有
(3)49gH2SO4约含有
您最近一年使用:0次
名校
解题方法
5 . 填空
(1)在标准状况下,3.4g NH3所占的体积为_______ L,它与标况下_______ L H2S所含的氢原子数目相同。
(2)200 mL溶液中,含Na2CO3 53 g,则该溶液中Na2CO3 的物质的量浓度_______ mol/L,Na+的物质的量浓度_______ mol/L。
(3)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是_______ 。(用X、Y表示)
(4)对于反应:Zn+2HCl=ZnCl2+H2↑,现有26 g Zn放入200mL2mol/L的HCl溶液中,此反应中_______ (填Zn或HCl)过量,该反应可生成氢气在标准状况时体积是_______ 。
(1)在标准状况下,3.4g NH3所占的体积为
(2)200 mL溶液中,含Na2CO3 53 g,则该溶液中Na2CO3 的物质的量浓度
(3)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是
(4)对于反应:Zn+2HCl=ZnCl2+H2↑,现有26 g Zn放入200mL2mol/L的HCl溶液中,此反应中
您最近一年使用:0次
6 . 物质的量是高中化学中常用的物理量,请按要求完成下列各小题。
(1)9.03×1023个NH3含___________ mol氢原子,___________ mol质子,在标准状况下的体积约为___________ L,氮原子与氢原子个数比___________ 。
(2)___________ molCO2分子中含有的氧原子数与1.806×1024个H2O中含有的氧原子数相同。
(3)在NaCl、MgCl2、MgSO4形成的混合溶液中,C(Na+)=0.10mol·L-1,C(Mg2+)=0.25mol·L-1,C(Cl-)=0.20mol·L-1,则C(S )为
)为___________ 。
(1)9.03×1023个NH3含
(2)
(3)在NaCl、MgCl2、MgSO4形成的混合溶液中,C(Na+)=0.10mol·L-1,C(Mg2+)=0.25mol·L-1,C(Cl-)=0.20mol·L-1,则C(S
 )为
)为
您最近一年使用:0次
名校
7 . 回答下列问题:
(1)在下列物质中,可以导电的是_______ (填序号,下同),是电解质的有_______ 。
①氯化钠晶体②熔融的氢氧化钠③Cu④酒精⑤Na2SO4溶液⑥液氨⑦稀盐酸⑧BaSO4晶体
(2)某气体在标准状况下的密度为1.25g/L,则14g该气体所含有的物质的量为_______ 。
(3)从400mL2.0mol·L-1的Al2(SO4)3溶液中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中 的物质的量浓度为
的物质的量浓度为_______ mol·L-1。
(4)已知Mm+与Nn-具有相同的电子层结构(核外电子排布相同),若N的核电荷数为a,M的质量数为A,则M的中子数为_______ 。
(1)在下列物质中,可以导电的是
①氯化钠晶体②熔融的氢氧化钠③Cu④酒精⑤Na2SO4溶液⑥液氨⑦稀盐酸⑧BaSO4晶体
(2)某气体在标准状况下的密度为1.25g/L,则14g该气体所含有的物质的量为
(3)从400mL2.0mol·L-1的Al2(SO4)3溶液中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中
 的物质的量浓度为
的物质的量浓度为(4)已知Mm+与Nn-具有相同的电子层结构(核外电子排布相同),若N的核电荷数为a,M的质量数为A,则M的中子数为
您最近一年使用:0次
名校
解题方法
8 . 用CO与H2反应合成甲醇符合原子经济的绿色化学理念,反应过程中能量变化如图所示。
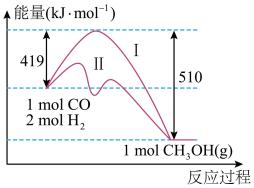
(1)请写出CO与H2反应合成甲醇的热化学方程式_______ ;
(2)该反应中相关的化学键键能数据如表所示:则C≡O中的键能为_______ kJ/mol;
(3)图中曲线I和II所对应的反应路径,比较容易发生的是_______ (填I或II);
(4)已知:①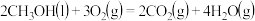
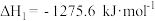 ,
,
②
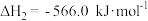 ,
,
③
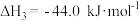 ,
,
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:_______ 。
(5)一定条件下,1 g甲醇蒸气完全燃烧生成二氧化碳和液态水,放出Q kJ的热量。则表示甲醇燃烧热的热化学方程式为_______ 。

(1)请写出CO与H2反应合成甲醇的热化学方程式
(2)该反应中相关的化学键键能数据如表所示:则C≡O中的键能为
| 化学键 | H-H | C-O | H-O | C-H |
| E/(kJ/mol) | 436 | 343 | 465 | 413 |
(3)图中曲线I和II所对应的反应路径,比较容易发生的是
(4)已知:①
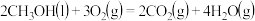
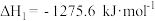 ,
,②

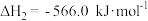 ,
,③

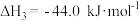 ,
,写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(5)一定条件下,1 g甲醇蒸气完全燃烧生成二氧化碳和液态水,放出Q kJ的热量。则表示甲醇燃烧热的热化学方程式为
您最近一年使用:0次
名校
解题方法
9 . 完成以下计算。
(1)12.4gNa2X中含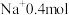 ,则
,则 的摩尔质量是
的摩尔质量是_______ 。
(2)标况下5.6L的CO2含有的电子数为_______ (用NA表示)。
(3)常温下,将20.0g14.0%的NaCl溶液,跟30.0g24.0%的NaCl溶液混合,得到密度为1.158g·cm-3的混合溶液。计算混合溶液中溶质的物质的量浓度:_______ (保留三位有效数字)
(4)将适量碳酸钙投入2L的盐酸中,恰好完全反应,标准状况下生成11.2LCO2,求碳酸钙的质量和盐酸的物质的量浓度_______ 。(写出计算过程和结果)
(1)12.4gNa2X中含
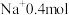 ,则
,则 的摩尔质量是
的摩尔质量是(2)标况下5.6L的CO2含有的电子数为
(3)常温下,将20.0g14.0%的NaCl溶液,跟30.0g24.0%的NaCl溶液混合,得到密度为1.158g·cm-3的混合溶液。计算混合溶液中溶质的物质的量浓度:
(4)将适量碳酸钙投入2L的盐酸中,恰好完全反应,标准状况下生成11.2LCO2,求碳酸钙的质量和盐酸的物质的量浓度
您最近一年使用:0次
10 . 甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、 和
和 )在催化剂作用下合成甲醇,发生的主要反应如下:
)在催化剂作用下合成甲醇,发生的主要反应如下:
①

②

③

(1)回答下列问题:已知反应①中相关的化学键键能数据如下:
由此计算
_______  ;已知
;已知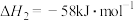 ,则
,则
_______  。
。
(2)已知在常温常压下:
①
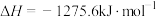
②
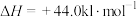
写出表示甲醇燃烧热的热化学方程式_______ 。
(3)已知常温时红磷比白磷稳定,已知:
① (白磷,s)
(白磷,s)

②4P(红磷,s)

比较反应中 的大小:
的大小:
_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)人体内葡萄糖的消耗可用下列热化学方程式表示:
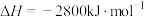 ;如果某人每天消耗12600kJ热量,则他每天至少要摄入葡萄糖的质量为
;如果某人每天消耗12600kJ热量,则他每天至少要摄入葡萄糖的质量为_______ 。
 和
和 )在催化剂作用下合成甲醇,发生的主要反应如下:
)在催化剂作用下合成甲醇,发生的主要反应如下:①


②


③


(1)回答下列问题:已知反应①中相关的化学键键能数据如下:
| 化学键 | H—H | C—O | C≡O | H—O | C—H |
E/ | 436 | 343 | 1076 | 465 | 413 |

 ;已知
;已知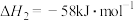 ,则
,则
 。
。(2)已知在常温常压下:
①

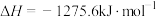
②

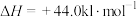
写出表示甲醇燃烧热的热化学方程式
(3)已知常温时红磷比白磷稳定,已知:
①
 (白磷,s)
(白磷,s)

②4P(红磷,s)


比较反应中
 的大小:
的大小:
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(4)人体内葡萄糖的消耗可用下列热化学方程式表示:

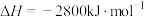 ;如果某人每天消耗12600kJ热量,则他每天至少要摄入葡萄糖的质量为
;如果某人每天消耗12600kJ热量,则他每天至少要摄入葡萄糖的质量为
您最近一年使用:0次



