名校
1 . 物质的量是高中化学常用的物理量,请完成以下有关计算:
(1) 个
个 分子的物质的量为
分子的物质的量为_______ ,质量为_______ 。
(2)0.5mol NaOH中含有的电子数为_______ ,在_______ mol 中所含
中所含 数目与上述0.5mol NaOH所含
数目与上述0.5mol NaOH所含 数目相等。
数目相等。
(3)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积_______ 。
(4)现有14.4gCO和 的混合气体,在标准状况下体积为8.96L。则混合气体的平均摩尔质量为
的混合气体,在标准状况下体积为8.96L。则混合气体的平均摩尔质量为_______ ,其中CO的体积分数为_______ 。
(5)40%氢氧化钠溶液的密度为1.525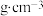 ,该溶液中溶质的物质的量浓度
,该溶液中溶质的物质的量浓度_______ 。
(1)
 个
个 分子的物质的量为
分子的物质的量为(2)0.5mol NaOH中含有的电子数为
 中所含
中所含 数目与上述0.5mol NaOH所含
数目与上述0.5mol NaOH所含 数目相等。
数目相等。(3)在一定温度和压强下,0.4mol某气体的体积为9.8L,则该条件下的气体摩尔体积
(4)现有14.4gCO和
 的混合气体,在标准状况下体积为8.96L。则混合气体的平均摩尔质量为
的混合气体,在标准状况下体积为8.96L。则混合气体的平均摩尔质量为(5)40%氢氧化钠溶液的密度为1.525
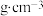 ,该溶液中溶质的物质的量浓度
,该溶液中溶质的物质的量浓度
您最近一年使用:0次
2 . 完成下列填空题。
(1)标准状况下, 二氧化碳的质量是
二氧化碳的质量是_______ g,含有的分子数是_______ 个。
(2) 氧气含有的原子数是
氧气含有的原子数是_______ 个,标准状况下的体积是_______ L。
(3)标准状况下, 二氧化碳和氧气的混合气体中含有的氧原子数是
二氧化碳和氧气的混合气体中含有的氧原子数是_______ 个。
(4) 个
个 的质量与
的质量与_______  的质量相等。
的质量相等。
(5)标准状况下, 氦气的分子数目是
氦气的分子数目是_______ 个;标准状况下, 个氧气分子的体积是
个氧气分子的体积是_______ L,氧气的质量是_______ g。
(6)相同物质的量的 和
和 ,它们的质量之比为
,它们的质量之比为_______ ;相同质量的 和
和 ,它们物质的量之比为
,它们物质的量之比为_______ ,所含氧原子个数比为_______ 。
(1)标准状况下,
 二氧化碳的质量是
二氧化碳的质量是(2)
 氧气含有的原子数是
氧气含有的原子数是(3)标准状况下,
 二氧化碳和氧气的混合气体中含有的氧原子数是
二氧化碳和氧气的混合气体中含有的氧原子数是(4)
 个
个 的质量与
的质量与 的质量相等。
的质量相等。(5)标准状况下,
 氦气的分子数目是
氦气的分子数目是 个氧气分子的体积是
个氧气分子的体积是(6)相同物质的量的
 和
和 ,它们的质量之比为
,它们的质量之比为 和
和 ,它们物质的量之比为
,它们物质的量之比为
您最近一年使用:0次
解题方法
3 . 回答下列问题
(1)3.01×1023个氯气分子的物质的量是_______ 。
(2)1.5 molNa2SO4·10H2O中所含的Na+的物质的量是_______ ,所含的SO 的物质的量是
的物质的量是_______ ,所含H2O的数目是_______ 。
(3)一定量的Na2CO3中,碳原子和氧原子的物质的量之比为_______ 。
(4)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为_______ ,R的相对原子质量是_______
(5)汽车受到猛烈撞击时,气囊内的NaN3会发生分解反应生成Na和N2。,写出发生分解反应的化学方程式_______ ;能保护司机不受伤害的某气囊需要0.0672m3(标准状况)的N2,该气囊中需要装入_______ 克的NaN3
(1)3.01×1023个氯气分子的物质的量是
(2)1.5 molNa2SO4·10H2O中所含的Na+的物质的量是
 的物质的量是
的物质的量是(3)一定量的Na2CO3中,碳原子和氧原子的物质的量之比为
(4)12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为
(5)汽车受到猛烈撞击时,气囊内的NaN3会发生分解反应生成Na和N2。,写出发生分解反应的化学方程式
您最近一年使用:0次
解题方法
4 . 将等物质的量的A、B混合于2 L的密闭容器中,发生反应: 3A(g)+B(g)  3C(g)+2D(g),经5 min后,测得D的浓度为0.5 mol·L-1,n(A)∶n(B)=3∶5.求:
3C(g)+2D(g),经5 min后,测得D的浓度为0.5 mol·L-1,n(A)∶n(B)=3∶5.求:
(1)5 min 末C的浓度是多少_______ ?
(2)这5 min 内B的平均反应速率是多少_______ ?
(3)反应开始前容器中的A的物质的量是多少_______ ?
 3C(g)+2D(g),经5 min后,测得D的浓度为0.5 mol·L-1,n(A)∶n(B)=3∶5.求:
3C(g)+2D(g),经5 min后,测得D的浓度为0.5 mol·L-1,n(A)∶n(B)=3∶5.求:(1)5 min 末C的浓度是多少
(2)这5 min 内B的平均反应速率是多少
(3)反应开始前容器中的A的物质的量是多少
您最近一年使用:0次
5 . 回答下列问题
(1)下列变化过程属于放热反应的是_________ 。
①2Al + Fe2O3 2Fe + Al2O3 ②酸碱中和反应 ③浓H2SO4稀释 ④醋酸电离 ⑤NH4Cl晶体与Ba(OH)2·8H2O混合搅拌
2Fe + Al2O3 ②酸碱中和反应 ③浓H2SO4稀释 ④醋酸电离 ⑤NH4Cl晶体与Ba(OH)2·8H2O混合搅拌
(2)CaCO3(s)=CaO(s)+CO2(g) ΔH1 CaO(s)+H2O(l)=Ca(OH)2(s) ΔH2
则ΔH1_______ ΔH2(填“>”、“<”或“=”)。
(3)已知1g苯燃烧生成二氧化碳和气态水时放出a kJ热量,1mol液态水气化需要吸收b kJ热量,请写出苯的燃烧热的热化学方程__________________ 。
(4)让生态环境更秀美、人民生活更幸福!为此,天津冬季取暖许多家庭用上了清洁能源天然气。实际生产中天然气需要脱硫,在1200℃时,工艺中会发生下列反应:
①H2S(g) + O2(g)= SO2(g) + H2O(g) ΔH1 ②2H2S(g) + SO2(g)=
O2(g)= SO2(g) + H2O(g) ΔH1 ②2H2S(g) + SO2(g)=  S2(g) + 2H2O(g) ΔH2
S2(g) + 2H2O(g) ΔH2
③H2S(g) + O2(g)= S(g) + H2O(g) ΔH3 ④2S(g) = S2(g) ΔH4
O2(g)= S(g) + H2O(g) ΔH3 ④2S(g) = S2(g) ΔH4
则ΔH4的表达式为________________ 。
(5)CO(g)和CH3OH(l)的摩尔燃烧焓ΔH分别为a kJ·mol-1和b kJ·mol-1,则甲醇不完全燃烧生成一氧化碳和1mol液态水的ΔH=__________ 。
(6)对温室气体CO2进行减排和综合治理具有十分重要的意义。CH4—CO2催化重整不仅对温室气体的减排具有重要意义,还可以得到合成气(CO和H2)。
已知:①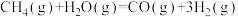
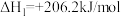
②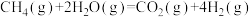
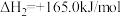
写出该催化重整反应的热化学方程式:_____________ 。
(1)下列变化过程属于放热反应的是
①2Al + Fe2O3
 2Fe + Al2O3 ②酸碱中和反应 ③浓H2SO4稀释 ④醋酸电离 ⑤NH4Cl晶体与Ba(OH)2·8H2O混合搅拌
2Fe + Al2O3 ②酸碱中和反应 ③浓H2SO4稀释 ④醋酸电离 ⑤NH4Cl晶体与Ba(OH)2·8H2O混合搅拌(2)CaCO3(s)=CaO(s)+CO2(g) ΔH1 CaO(s)+H2O(l)=Ca(OH)2(s) ΔH2
则ΔH1
(3)已知1g苯燃烧生成二氧化碳和气态水时放出a kJ热量,1mol液态水气化需要吸收b kJ热量,请写出苯的燃烧热的热化学方程
(4)让生态环境更秀美、人民生活更幸福!为此,天津冬季取暖许多家庭用上了清洁能源天然气。实际生产中天然气需要脱硫,在1200℃时,工艺中会发生下列反应:
①H2S(g) +
 O2(g)= SO2(g) + H2O(g) ΔH1 ②2H2S(g) + SO2(g)=
O2(g)= SO2(g) + H2O(g) ΔH1 ②2H2S(g) + SO2(g)=  S2(g) + 2H2O(g) ΔH2
S2(g) + 2H2O(g) ΔH2③H2S(g) +
 O2(g)= S(g) + H2O(g) ΔH3 ④2S(g) = S2(g) ΔH4
O2(g)= S(g) + H2O(g) ΔH3 ④2S(g) = S2(g) ΔH4则ΔH4的表达式为
(5)CO(g)和CH3OH(l)的摩尔燃烧焓ΔH分别为a kJ·mol-1和b kJ·mol-1,则甲醇不完全燃烧生成一氧化碳和1mol液态水的ΔH=
(6)对温室气体CO2进行减排和综合治理具有十分重要的意义。CH4—CO2催化重整不仅对温室气体的减排具有重要意义,还可以得到合成气(CO和H2)。
已知:①
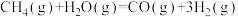
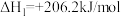
②
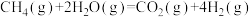
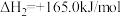
写出该催化重整反应的热化学方程式:
您最近一年使用:0次
6 . 已知可逆反应CO(g)+H2O(g) CO2(g)+H2(g),平衡常数为K。
CO2(g)+H2(g),平衡常数为K。
(1)557℃时,若起始浓度:CO为1mol·L-1,H2O为1.5mol·L-1,平衡时CO转化率为60%,则H2O的转化率为___________ ;K值为___________ 。
(2)557℃时,若起始浓度改为:CO为1mol·L-1,H2O为3mol·L-1,平衡时H2O的转化率为___________ 。
 CO2(g)+H2(g),平衡常数为K。
CO2(g)+H2(g),平衡常数为K。(1)557℃时,若起始浓度:CO为1mol·L-1,H2O为1.5mol·L-1,平衡时CO转化率为60%,则H2O的转化率为
(2)557℃时,若起始浓度改为:CO为1mol·L-1,H2O为3mol·L-1,平衡时H2O的转化率为
您最近一年使用:0次
2022-08-27更新
|
624次组卷
|
5卷引用:福建省莆田第十五中学2019-2020学年高二上学期期末考试化学试题
福建省莆田第十五中学2019-2020学年高二上学期期末考试化学试题(已下线)2.2.2 化学平衡常数(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)2.2.1 化学平衡常数-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)第09讲 化学平衡常数(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)河北省邯郸市魏县2022-2023学年高二上学期期末考试化学试题
解题方法
7 . 温度对反应速率的影响可用阿伦尼乌斯公式的一种形式表示: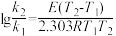 。式中k1、k2分别为温度T1、T2时某反应的速率常数;E为反应的活化能(单位:kJ/mol)(假定活化能在温度变化范围不大时是常数);R为常数8.314,单位J/(mol·K)。又对同一反应,在不同温度下反应速率常数与反应时间的关系如下:
。式中k1、k2分别为温度T1、T2时某反应的速率常数;E为反应的活化能(单位:kJ/mol)(假定活化能在温度变化范围不大时是常数);R为常数8.314,单位J/(mol·K)。又对同一反应,在不同温度下反应速率常数与反应时间的关系如下: 。
。
(1)现知在300K,鲜牛奶5小时后即变酸,但在275K的冰箱里可保存50小时,牛奶变酸反应的活化能是_______ 。
(2)若鲜牛奶存放2.5小时后即变酸,则此时温度为_______ 。
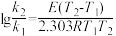 。式中k1、k2分别为温度T1、T2时某反应的速率常数;E为反应的活化能(单位:kJ/mol)(假定活化能在温度变化范围不大时是常数);R为常数8.314,单位J/(mol·K)。又对同一反应,在不同温度下反应速率常数与反应时间的关系如下:
。式中k1、k2分别为温度T1、T2时某反应的速率常数;E为反应的活化能(单位:kJ/mol)(假定活化能在温度变化范围不大时是常数);R为常数8.314,单位J/(mol·K)。又对同一反应,在不同温度下反应速率常数与反应时间的关系如下: 。
。(1)现知在300K,鲜牛奶5小时后即变酸,但在275K的冰箱里可保存50小时,牛奶变酸反应的活化能是
(2)若鲜牛奶存放2.5小时后即变酸,则此时温度为
您最近一年使用:0次
名校
8 . 如图,向盛有3.0 mL NO的试管中缓缓通入1.5 mLO2 (气体体积均为标准状况下测定) 。
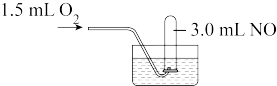
(1)写出观察到的现象:___________ 。
(2)若将充满30 mL NO2和O2混合气体的量筒倒立于装满水的水槽内,最后剩余5 mL气体,则原混合气体中NO2的体积是___________ mL或者___________ mL。

(1)写出观察到的现象:
(2)若将充满30 mL NO2和O2混合气体的量筒倒立于装满水的水槽内,最后剩余5 mL气体,则原混合气体中NO2的体积是
您最近一年使用:0次
名校
解题方法
9 . 现有浓度均为0.1mol·L-1的下列溶液:①硫酸②醋酸③氢氧化钠④氯化铵⑤醋酸铵⑥硫酸氢铵⑦氨水。
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是____ (填序号)。
(2)④、⑤、⑥、⑦四种溶液中 浓度由大到小的顺序是
浓度由大到小的顺序是____ (填序号)。
(3)将③和④按体积比1:2混合后显碱性,混合液中各离子浓度由大到小的顺序是____ 。
(4)已知t℃,Kw=1×10-13,在t℃时将pH=11的NaOH溶液aL与pH=2的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=7,则a___ b(填“>”或“<”或“=”)。
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是
(2)④、⑤、⑥、⑦四种溶液中
 浓度由大到小的顺序是
浓度由大到小的顺序是(3)将③和④按体积比1:2混合后显碱性,混合液中各离子浓度由大到小的顺序是
(4)已知t℃,Kw=1×10-13,在t℃时将pH=11的NaOH溶液aL与pH=2的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=7,则a
您最近一年使用:0次
名校
解题方法
10 . 配平以下方程式并用单线桥法标出下列反应电子转移的方向和数目。(若系数为“1”,请标出)
(1)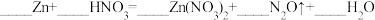
_______ 。
(2)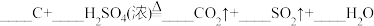
_______ 。
(3)
_______ 。
(4)
_______ 。
(5)
_______ 。
(6)
_______ 。
(1)
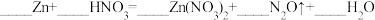
(2)
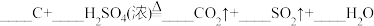
(3)

(4)

(5)

(6)

您最近一年使用:0次



