9-10高二下·福建厦门·期末
1 . 800K时将1mo A(g)和l molB(g)充人体积为1 L的固定容积反应器中,发生如下反应:A(g)+B(g) c(g)+D(g),在某条件下达到平衡时有2/3的A转化为D,求:
c(g)+D(g),在某条件下达到平衡时有2/3的A转化为D,求:
(1)该平衡混合物中D的体积分数___________ ;
(2)该温度下的平衡常数___________ ;
(3)B的转化率___________ 。
 c(g)+D(g),在某条件下达到平衡时有2/3的A转化为D,求:
c(g)+D(g),在某条件下达到平衡时有2/3的A转化为D,求:(1)该平衡混合物中D的体积分数
(2)该温度下的平衡常数
(3)B的转化率
您最近一年使用:0次
9-10高二下·福建福州·期末
2 . 按要求填空。
(1)经测定某含氧有机物的相对分子质量为94。现取9.4g该含氧有机物充分燃烧后的产物通过浓硫酸后增重5.4g,并收集到标准状况下CO2气体13.44L。则:
①该含氧有机物的分子式为_________________ ;
②请写出该含氧有机物中官能团的名称___________________ 。
(2)完成下列变化的化学方程式:
①苯与浓硫酸、浓硝酸的混合酸在50-60℃时的反应_________________________ 。
②苯酚与浓溴水反应_____________________________________ 。
③二氧化碳通入苯酚钠溶液,产生白色浑浊_________________________ 。
④家用液化气的主要成分之一是丁烷,当1g丁烷完全燃烧并生成二氧化碳和液态水时,放出热量为50kJ。丁烷燃烧的热化学方程式为___________________ 。
(1)经测定某含氧有机物的相对分子质量为94。现取9.4g该含氧有机物充分燃烧后的产物通过浓硫酸后增重5.4g,并收集到标准状况下CO2气体13.44L。则:
①该含氧有机物的分子式为
②请写出该含氧有机物中官能团的名称
(2)完成下列变化的化学方程式:
①苯与浓硫酸、浓硝酸的混合酸在50-60℃时的反应
②苯酚与浓溴水反应
③二氧化碳通入苯酚钠溶液,产生白色浑浊
④家用液化气的主要成分之一是丁烷,当1g丁烷完全燃烧并生成二氧化碳和液态水时,放出热量为50kJ。丁烷燃烧的热化学方程式为
您最近一年使用:0次
9-10高一下·福建·期末
解题方法
3 . 铝粉和氧化铁粉末的混合物制成的铝热剂可用于焊接钢轨。现取不同质量的该铝热剂分别和100ml同物质的量浓度的NaOH溶液反应,所取铝热剂的质量与产生气体的体积关系如下表(气体体积均在标准状况下测定):
试完成下列计算:
(1)NaOH溶液的物质的量浓度_______________ 。
(2)该铝热剂中铝的质量分数_____________ 
(3)20g该铝热剂发生铝热反应理论上产生铁的质量是多少?________ (写出步骤)
| ① | ② | ③ | ④ | |
| 铝热剂质量/g | 5g | 10g | 15g | 20g |
| 气体体积/L | 2.24L | 4.48L | 6.72L | 6.72L |
试完成下列计算:
(1)NaOH溶液的物质的量浓度
(2)该铝热剂中铝的质量分数

(3)20g该铝热剂发生铝热反应理论上产生铁的质量是多少?
您最近一年使用:0次
9-10高二下·福建福州·期末
4 . (1)3.4克NH3含质子的物质的量为_____ ,该气体在标准状况下的体积是____ 。
(2)已知500mL Al2(SO4)3溶液中含有Al3+为0.5mol,则Al2(SO4)3溶液的物质的量浓度为_____ mol/L,取上述溶液50mL加水到150mL,此溶液中SO42-的物质的量浓度为______ mol/L。
(2)已知500mL Al2(SO4)3溶液中含有Al3+为0.5mol,则Al2(SO4)3溶液的物质的量浓度为
您最近一年使用:0次
9-10高一下·福建福州·阶段练习
5 . 已知16.0 g CH4完全燃烧生成CO2和液态水时,放出890kJ热量。现有CH4和CO混合气体共0.75 mol,完全燃烧后生成CO2和18 g液态水,并放出516 kJ热量。求:
(1)混合气体中CH4的物质的量为___________ , CO的物质的量为__________ ;
(2)混合气体中由CO完全燃烧所放出的热量为__________ kJ?
(1)混合气体中CH4的物质的量为
(2)混合气体中由CO完全燃烧所放出的热量为
您最近一年使用:0次
9-10高二·福建厦门·假期作业
6 . 配平并完成方程式。
(1)_____ Pt+ _____ HNO3+ _____ HCl
_____ H2PtCl6+_____ NO↑+_____ ( )
(2)_____ Fe+ _____ HNO3(稀)
_____ Fe(NO3)3+ _____ NO↑+ _____ H2O,被还原与未被还原的氮元素质量之比__________ 。
(3)_____ Cu2S+_____ HNO3
_____ Cu(NO3)2+ _____ NO↑+_____ S↓+ _____ H2O,被还原与未被还原硝酸物质的量之比是_______ 被还原的元素是_____ 。
(1)

(2)

(3)

您最近一年使用:0次
9-10高一下·福建三明·期中
7 . 在一密闭容器中反应2SO2+O2 2SO3经5秒后,SO3的浓度增加了0.4mol·L-1,则在这段时间内用O2表示的反应速率为
2SO3经5秒后,SO3的浓度增加了0.4mol·L-1,则在这段时间内用O2表示的反应速率为_________ mol·L-1·s-1。
 2SO3经5秒后,SO3的浓度增加了0.4mol·L-1,则在这段时间内用O2表示的反应速率为
2SO3经5秒后,SO3的浓度增加了0.4mol·L-1,则在这段时间内用O2表示的反应速率为
您最近一年使用:0次
9-10高一下·辽宁本溪·阶段练习
8 . 常温下,在一刚性容器内部有一个不漏气且可以滑动的活塞,将容器分割成左右两室。左室充入N2,右室充入H2和O2,活塞正好使N2占容器体积的1/4(如图)。然后点燃H2和O2的混合气体,反应完毕后恢复至原来的温度,活塞正好停留在容器的中间。经检验,此时右室中气体可使带火星的木条复燃。
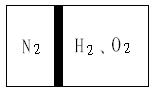
(1)求反应前H2和O2的物质的量之比。
(2)求反应前H2和O2混合气体的平均相对分子质量。

(1)求反应前H2和O2的物质的量之比。
(2)求反应前H2和O2混合气体的平均相对分子质量。
您最近一年使用:0次
9-10高一下·福建龙岩·期中
解题方法
9 . 某元素的同位素X,它的氯化物XCl 1.49g溶于水制成溶液后,加入1mol·L-1的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,试通过计算确定(写出计算过程):
(1)X元素在周期表中的位置________ ;
(2)把一小粒X的单质放入水中,有何现象_________ ? 写出反应的化学方程式____ 。
(1)X元素在周期表中的位置
(2)把一小粒X的单质放入水中,有何现象
您最近一年使用:0次
真题
名校
10 . 氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3-+4H++3e→NO+2H2O ;KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:_______________________________
(2)反应中硝酸体现了_________ 、_________ 性质。
(3)反应中若产生0.2mol气体,则转移电子的物质的量是________ mol。
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是:___________________________________ 。
(1)写出并配平该氧化还原反应的方程式:
(2)反应中硝酸体现了
(3)反应中若产生0.2mol气体,则转移电子的物质的量是
(4)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是:
您最近一年使用:0次
2009-11-16更新
|
1905次组卷
|
10卷引用:2015届福建省武平县第一中学高三上学期12月月考化学试卷
2015届福建省武平县第一中学高三上学期12月月考化学试卷2007年普通高等学校招生全国统一考试(上海卷)化学试题(已下线)2012届北京四中高三上学期期中测试化学试卷(已下线)2012-2013学年辽宁省丹东市宽甸二中高二4月月考(一)化学试卷(已下线)2014高考化学二轮专题突破 专题四氧化还原反应练习卷(已下线)2014届高考化学三轮复习排查 专题3离子反应 氧化还原反应练习卷(已下线)2015届四川省成都市高新区高三9月月考化学试卷(已下线)2015届浙江省江山实验中学高三9月月考化学试卷四川省南充高级中学2017-2018学年高一12月月考化学试题沪科版化学拓展性课程4《离子互换反应和氧化还原反应》测试题



