解题方法
1 . 填空。
(1)25℃、101KPa时,26gC2H2气体完全燃烧生成二氧化碳气体和液态水放出1299.6kJ的热,写出该反应的热化学方程式_______ 。
(2)研究NO2、SO2等大气污染气体的处理方法具有重要的意义。
已知:①2SO2(g)+O2(g)⇌2SO3(g) ∆H1=-196kJ∙mol-1
②2NO(g)+O2(g)⇌2NO2(g) ∆H2=-113.0kJ∙mol-1
则反应NO2(g)+SO2(g)⇌SO3(g)+NO(g)的∆H=_______ kJ∙mol-1。
(3)已知拆开1mol下列气态分子形成独立的气态原子时需要的能量数据如表。
则N2(g)+O2(g)=2NO(g) ΔH=_______ kJ·mol-1。
(1)25℃、101KPa时,26gC2H2气体完全燃烧生成二氧化碳气体和液态水放出1299.6kJ的热,写出该反应的热化学方程式
(2)研究NO2、SO2等大气污染气体的处理方法具有重要的意义。
已知:①2SO2(g)+O2(g)⇌2SO3(g) ∆H1=-196kJ∙mol-1
②2NO(g)+O2(g)⇌2NO2(g) ∆H2=-113.0kJ∙mol-1
则反应NO2(g)+SO2(g)⇌SO3(g)+NO(g)的∆H=
(3)已知拆开1mol下列气态分子形成独立的气态原子时需要的能量数据如表。
| 物质 | N2 | O2 | NO |
| 能量(kJ·mol-1) | 946 | 498 | 632 |
您最近一年使用:0次
2 . 现欲利用锌粒和稀盐酸制取标准状况下33.6LH2,则至少需消耗锌粒多少克_______ ?消耗稀盐酸中HCl的物质的量是多少_______ ?
您最近一年使用:0次
3 . 回答下列问题
(1)m gH2 含有n个H2分子,则阿伏加德罗常数为_______ (用含m和n表示)。
(2)在8克某物质中含有3.01×1023个分子,该物质的相对分子质量为:_______ 。
(3)若O2和O3的质量相等,则其物质的量之比_______ ,原子数之比 _______ 。
(4)标准状况下有CH43.36L,则该CH4气体的物质的量为_______ ,质量为_______ ,所含氢原子的物质的量为_______ ,所含质子的物质的量为_______ 。
(1)m gH2 含有n个H2分子,则阿伏加德罗常数为
(2)在8克某物质中含有3.01×1023个分子,该物质的相对分子质量为:
(3)若O2和O3的质量相等,则其物质的量之比
(4)标准状况下有CH43.36L,则该CH4气体的物质的量为
您最近一年使用:0次
解题方法
4 . 把11.2 L(标准状况)HCl气体溶于水,配制成250mL的溶液,求:
(1)该溶液的物质的量浓度_____
(2)将该溶液与足量的锌反应,在标准状况下,能生成多少升的H2_____ ? (反应的化学方程式为 Zn + 2HCl = ZnCl2 + H2↑)
(1)该溶液的物质的量浓度
(2)将该溶液与足量的锌反应,在标准状况下,能生成多少升的H2
您最近一年使用:0次
5 . 回答下列问题:
(1)0.5molSO2,含有的分子数为_______ 个,质量为_______ g,标准状况下体积为_______ L。
(2)标准状况下,14g N2所占有的体积为_______ L,所含氮原子个数为_______ 个。
(3)标准状况下,2mol NH3与_______ g CO2的体积相等。
(4)中和含0.2mol HCl的稀盐酸,需NaOH物质的量为_______ mol,如改用KOH,则所需KOH的质量为_______ g。
(5)已知14g A和40g B恰好完全反应生成0.25mol C和38g D,则C的摩尔质量为_______ 。
(6)在22.2g某二价金属的氯化物(RCl2)中含Cl- 离子0.4mol,则RCl2的摩尔质量为_______ ,R的相对原子质量为_______ 。
(1)0.5molSO2,含有的分子数为
(2)标准状况下,14g N2所占有的体积为
(3)标准状况下,2mol NH3与
(4)中和含0.2mol HCl的稀盐酸,需NaOH物质的量为
(5)已知14g A和40g B恰好完全反应生成0.25mol C和38g D,则C的摩尔质量为
(6)在22.2g某二价金属的氯化物(RCl2)中含Cl- 离子0.4mol,则RCl2的摩尔质量为
您最近一年使用:0次
6 . 已知在800 K时,反应:CO(g)+H2O(g)⇌H2(g)+CO2(g),若初始浓度c0(CO)=2 mol·L-1,c0(H2O)=3 mol·L-1,则反应达到平衡时,CO转化成CO2的转化率为60%。求:
(1)800 K时该反应的平衡常数_______ ;
(2)如果将H2O的初始浓度加大为6 mol·L-1,求此时CO转化为CO2的转化率______ 。
(1)800 K时该反应的平衡常数
(2)如果将H2O的初始浓度加大为6 mol·L-1,求此时CO转化为CO2的转化率
您最近一年使用:0次
7 . 回答下列问题:
(1)_______ 克NH3分子中所含氢原子数与0.3NA个水分子中所含氢原子数相等。
(2)已知O2和CO2的混合气体,标准状况下体积为11.2L,质量为18g,则该混合气体与相同状况下的CO的密度之比为_______ 。
(3)38g某二价金属氯化物ACl2中含有0.8molCl-,则A的相对原子质量是_______ 。
(4)100mL浓度为1.2mol/L的硫酸与6.5g锌充分反应后,最多可以收集到标准状况下氢气的体积_______ L。
(5)某同学制备氢氧化铁胶体的实验过程为:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2mLFeCl3饱和溶液,继续煮沸至混合液呈红褐色。请写出该过程的化学反应方程式:_______ 。
(1)
(2)已知O2和CO2的混合气体,标准状况下体积为11.2L,质量为18g,则该混合气体与相同状况下的CO的密度之比为
(3)38g某二价金属氯化物ACl2中含有0.8molCl-,则A的相对原子质量是
(4)100mL浓度为1.2mol/L的硫酸与6.5g锌充分反应后,最多可以收集到标准状况下氢气的体积
(5)某同学制备氢氧化铁胶体的实验过程为:取一小烧杯,加入25mL蒸馏水加热至沸腾,向沸水中逐滴加入1~2mLFeCl3饱和溶液,继续煮沸至混合液呈红褐色。请写出该过程的化学反应方程式:
您最近一年使用:0次
名校
8 . 回答下列问题:
(1)在下列物质中,可以导电的是_______ (填序号,下同),是电解质的有_______ 。
①氯化钠晶体②熔融的氢氧化钠③Cu④酒精⑤Na2SO4溶液⑥液氨⑦稀盐酸⑧BaSO4晶体
(2)某气体在标准状况下的密度为1.25g/L,则14g该气体所含有的物质的量为_______ 。
(3)从400mL2.0mol·L-1的Al2(SO4)3溶液中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中 的物质的量浓度为
的物质的量浓度为_______ mol·L-1。
(4)已知Mm+与Nn-具有相同的电子层结构(核外电子排布相同),若N的核电荷数为a,M的质量数为A,则M的中子数为_______ 。
(1)在下列物质中,可以导电的是
①氯化钠晶体②熔融的氢氧化钠③Cu④酒精⑤Na2SO4溶液⑥液氨⑦稀盐酸⑧BaSO4晶体
(2)某气体在标准状况下的密度为1.25g/L,则14g该气体所含有的物质的量为
(3)从400mL2.0mol·L-1的Al2(SO4)3溶液中取出10mL,将这10mL溶液用水稀释到100mL,所得溶液中
 的物质的量浓度为
的物质的量浓度为(4)已知Mm+与Nn-具有相同的电子层结构(核外电子排布相同),若N的核电荷数为a,M的质量数为A,则M的中子数为
您最近一年使用:0次
名校
解题方法
9 . 用CO与H2反应合成甲醇符合原子经济的绿色化学理念,反应过程中能量变化如图所示。
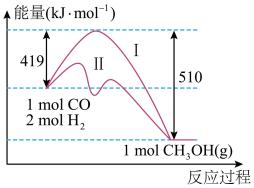
(1)请写出CO与H2反应合成甲醇的热化学方程式_______ ;
(2)该反应中相关的化学键键能数据如表所示:则C≡O中的键能为_______ kJ/mol;
(3)图中曲线I和II所对应的反应路径,比较容易发生的是_______ (填I或II);
(4)已知:①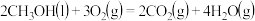
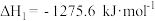 ,
,
②
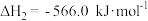 ,
,
③
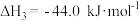 ,
,
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:_______ 。
(5)一定条件下,1 g甲醇蒸气完全燃烧生成二氧化碳和液态水,放出Q kJ的热量。则表示甲醇燃烧热的热化学方程式为_______ 。

(1)请写出CO与H2反应合成甲醇的热化学方程式
(2)该反应中相关的化学键键能数据如表所示:则C≡O中的键能为
| 化学键 | H-H | C-O | H-O | C-H |
| E/(kJ/mol) | 436 | 343 | 465 | 413 |
(3)图中曲线I和II所对应的反应路径,比较容易发生的是
(4)已知:①
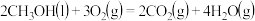
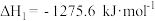 ,
,②

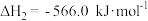 ,
,③

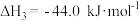 ,
,写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:
(5)一定条件下,1 g甲醇蒸气完全燃烧生成二氧化碳和液态水,放出Q kJ的热量。则表示甲醇燃烧热的热化学方程式为
您最近一年使用:0次
名校
解题方法
10 . 完成以下计算。
(1)12.4gNa2X中含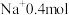 ,则
,则 的摩尔质量是
的摩尔质量是_______ 。
(2)标况下5.6L的CO2含有的电子数为_______ (用NA表示)。
(3)常温下,将20.0g14.0%的NaCl溶液,跟30.0g24.0%的NaCl溶液混合,得到密度为1.158g·cm-3的混合溶液。计算混合溶液中溶质的物质的量浓度:_______ (保留三位有效数字)
(4)将适量碳酸钙投入2L的盐酸中,恰好完全反应,标准状况下生成11.2LCO2,求碳酸钙的质量和盐酸的物质的量浓度_______ 。(写出计算过程和结果)
(1)12.4gNa2X中含
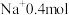 ,则
,则 的摩尔质量是
的摩尔质量是(2)标况下5.6L的CO2含有的电子数为
(3)常温下,将20.0g14.0%的NaCl溶液,跟30.0g24.0%的NaCl溶液混合,得到密度为1.158g·cm-3的混合溶液。计算混合溶液中溶质的物质的量浓度:
(4)将适量碳酸钙投入2L的盐酸中,恰好完全反应,标准状况下生成11.2LCO2,求碳酸钙的质量和盐酸的物质的量浓度
您最近一年使用:0次



