名校
解题方法
1 . 在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如下图所示,回答下列问题:
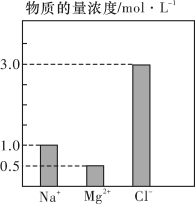
(1)混合液中,NaCl的物质的量为_______ ,含溶质MgCl2的质量为_______ 。
(2)该混合液中CaCl2的物质的量为_______ ,将该混合液加水稀释至体积为1L,稀释后溶液中Ca2+的物质的量浓度为_______ 。
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀的物质的量为_______ 。

(1)混合液中,NaCl的物质的量为
(2)该混合液中CaCl2的物质的量为
(3)向该稀释后的溶液中加入足量硝酸酸化的硝酸银溶液,可得到沉淀的物质的量为
您最近一年使用:0次
2 . 回答下列问题
(1)1.5molH2SO4的质量是_______ ,其中含有_______ molH,含有_______ g氧。
(2)4.4gCO2的物质的量是_______ ,其中含有二氧化碳分子_______ 个,电子_______ 个,它在标况下占有的体积为_______ 。
(3)等质量的HCl、NH3、CO2、O2四种气体,在相同温度和相同压强条件下,体积最大的是_______ 。
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为_______ ,R的相对原子质量为_______ 。
(5)实验室需要0.1mol/L的氢氧化钠溶液100mL,其中需要2mol/L的氢氧化钠溶液_______ mL,将71 g Na2SO4溶于水配成1 L溶液,该溶液中Na2 SO4的物质的量浓度为_______ ,溶液中Na+的物质的量浓度为_______
(1)1.5molH2SO4的质量是
(2)4.4gCO2的物质的量是
(3)等质量的HCl、NH3、CO2、O2四种气体,在相同温度和相同压强条件下,体积最大的是
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为
(5)实验室需要0.1mol/L的氢氧化钠溶液100mL,其中需要2mol/L的氢氧化钠溶液
您最近一年使用:0次
名校
3 . 回答下列问题:
(1)同温同压下的两个容积相同的容器中分别装有O2和O3气体,则两瓶气体中原子数之比是_______ 。
(2)下列所给出的几组物质中:标准状况下体积最大的是_______ ;质量最大的是_______ 。(填序号)
①1g H2; ②2.408×1023个CH4;③10.8 g H2O; ④标准状况下6.72 LCO2
(3)与0.2molH3PO4具有相同氢原子数的HNO3的物质的量是_______ mol,具有相同氧原子数的硫酸分子有_______ 个。
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为_______ ,R的相对原子质量为_______ 。
(5)已知一混合溶液中有Na+、Cl-、SO 、H+、K+,含Na+0.2 mol,SO
、H+、K+,含Na+0.2 mol,SO 0.5 mol,H+0.1 mol,K+ 0.8 mol,则Cl-的物质的量为
0.5 mol,H+0.1 mol,K+ 0.8 mol,则Cl-的物质的量为 _______ 。
(1)同温同压下的两个容积相同的容器中分别装有O2和O3气体,则两瓶气体中原子数之比是
(2)下列所给出的几组物质中:标准状况下体积最大的是
①1g H2; ②2.408×1023个CH4;③10.8 g H2O; ④标准状况下6.72 LCO2
(3)与0.2molH3PO4具有相同氢原子数的HNO3的物质的量是
(4)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为
(5)已知一混合溶液中有Na+、Cl-、SO
 、H+、K+,含Na+0.2 mol,SO
、H+、K+,含Na+0.2 mol,SO 0.5 mol,H+0.1 mol,K+ 0.8 mol,则Cl-的物质的量为
0.5 mol,H+0.1 mol,K+ 0.8 mol,则Cl-的物质的量为
您最近一年使用:0次
2022-10-30更新
|
275次组卷
|
2卷引用:四川省凉山宁南中学2021-2022学年高一上学期第一次月考化学试题
4 . 回答下列问题:
(1)含有6.02×1023个H的H2O,其物质的量是_______ ;1molNa2SO4溶于水能电离出_______ 个Na+、_______ 个SO 。
。
(2)_______ molH2O中含有的氧原子数与1.5molCO2中含有的氧原子数相等。
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为_______ 。
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为_______ 。
(5)标准状况下,密度为0.75g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为_______ ,该混合气体对氢气的相对密度为_______ 。
(6)某结晶水合物的化学式为A·nH2O,A的相对分子质量为M。如将ag该化合物加热至结晶水全部失去,剩余的残渣为bg,则n=_______ 。
(7)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为_______ 。
(1)含有6.02×1023个H的H2O,其物质的量是
 。
。(2)
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为
(5)标准状况下,密度为0.75g·L-1的NH3与CH4组成的混合气体中,NH3的体积分数为
(6)某结晶水合物的化学式为A·nH2O,A的相对分子质量为M。如将ag该化合物加热至结晶水全部失去,剩余的残渣为bg,则n=
(7)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为
您最近一年使用:0次
5 . 回答下列问题:
(1)12.4g Na2R含Na+0.4mol,则Na2R的摩尔质量为_______ ,R的相对原子质量为_______ 。含R的质量为1.6g 的Na2R的物质的量为_______ 。
(2)质量之比为16:7:6的三种气体SO2、CO、NO,分子个数之比为_______ ;氧原子个数之比为_______ ;相同条件下的体积之比为_______ 。
(3)标准状况下,1.7g NH3体积为_______ L,它与标准状况下 _______ L H2S含有相同数目的氢原子。
(4)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为_______ ,R的相对原子质量为_______ 。
(1)12.4g Na2R含Na+0.4mol,则Na2R的摩尔质量为
(2)质量之比为16:7:6的三种气体SO2、CO、NO,分子个数之比为
(3)标准状况下,1.7g NH3体积为
(4)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
您最近一年使用:0次
6 . 回答下列问题:
(1)3.6 g H2O的物质的量是_______ ,含有水分子的数目是_______ ,含有氢原子的物质的量是_______ 。
(2)1.5molCO2和_______ g CH4在标准状况下占有相同的体积,其体积为_______ 。
(3)在标准状况下,100mL某气体的质量为0.179g,该气体的相对分子质量_______ 。
(4)现有mg某X2气体,它的摩尔质量为M g/mol,阿伏加德罗常数用NA表示,则:该气体的物质的量为_______ mol;一个X原子的质量为_______ g;该气体在标准状况下的体积为_______ L。
(5)200 mL Al2(SO4)3溶液中含Al3+ 5.4 g,则溶液中c(SO )=
)=_______ 。
(6)标准状况下,将V L HCl溶解在1 L水中(水的密度近似为1g/cm3),所得溶液的密度为ρ g/cm3,物质的量浓度为c mol/L,则c=_______ 。(用含V、ρ的式子表示)
(1)3.6 g H2O的物质的量是
(2)1.5molCO2和
(3)在标准状况下,100mL某气体的质量为0.179g,该气体的相对分子质量
(4)现有mg某X2气体,它的摩尔质量为M g/mol,阿伏加德罗常数用NA表示,则:该气体的物质的量为
(5)200 mL Al2(SO4)3溶液中含Al3+ 5.4 g,则溶液中c(SO
 )=
)=(6)标准状况下,将V L HCl溶解在1 L水中(水的密度近似为1g/cm3),所得溶液的密度为ρ g/cm3,物质的量浓度为c mol/L,则c=
您最近一年使用:0次
7 . 计算
(1)3.01×1023个H2O的物质的量为_______ mol,其中,所含原子的物质的量为_______ mol,所含电子的物质的量为_______ mol。
(2)_______ g H2O中的氧原子数目与标准状况下22.4 LCO2中的氧原子数目相同。
(3)2g NaOH溶于水配制成_______ mL溶液时其物质的量浓度为2mol/L。
(4)在相同的条件下,等质量的N2、CO2、NH3的体积由大到小的顺序为_______ ,在相同条件下,等体积的N2、CO2、NH3的质量由大到小的顺序为_______ ,在相同条件下,等体积的N2、CO2、NH3密度由大到小的顺序为_______ 。
(5)某硫酸铝溶液中所含铝离子浓度为3mol/L,则硫酸根离子浓度为_______
(6)电解1.8 g H2O所得的H2在标准状况下的体积为_______
(1)3.01×1023个H2O的物质的量为
(2)
(3)2g NaOH溶于水配制成
(4)在相同的条件下,等质量的N2、CO2、NH3的体积由大到小的顺序为
(5)某硫酸铝溶液中所含铝离子浓度为3mol/L,则硫酸根离子浓度为
(6)电解1.8 g H2O所得的H2在标准状况下的体积为
您最近一年使用:0次
8 . 设NA表示阿伏加德罗常数的值,请回答下列问题:
(1)O2的摩尔质量为___________ g/mol,1molO2中含有___________ 个O2分子。
(2)6.02×1023个Na+约含有___________ molNa+,其质量为___________ g。
(3)0.5molCH4约含有___________ 个CH4分子,其标准状况的气体体积___________ L。
(4)0.2molO2与___________ molCH4原子数相等;质量相同的O3和O2物质的量之比为___________ 。
(5)0.2mol/LKCl溶液与___________ mol/LMgCl2溶液氯离子物质的量浓度相等,将这两种溶液按体积比1:2混合,不考虑混合时溶液体积变化,混合溶液中氯离子物质的量浓度为___________ 。
(1)O2的摩尔质量为
(2)6.02×1023个Na+约含有
(3)0.5molCH4约含有
(4)0.2molO2与
(5)0.2mol/LKCl溶液与
您最近一年使用:0次
名校
9 . 取10.6gNa2CO3溶于水配成100mL溶液,求:
(1)Na2CO3溶液的物质的量浓度_______ 。
(2)取出20.0mL该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.04mol/L,求稀释后溶液的体积_______ 。
(3)取出20.0mL该溶液,向其中滴加足量1mol/L的稀硫酸,计算产生的CO2在标准状况下的体积_______ 。
(1)Na2CO3溶液的物质的量浓度
(2)取出20.0mL该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.04mol/L,求稀释后溶液的体积
(3)取出20.0mL该溶液,向其中滴加足量1mol/L的稀硫酸,计算产生的CO2在标准状况下的体积
您最近一年使用:0次
名校
10 . 根据题意填空:
(1)3.01×1023个CO2分子的物质的量是_______ mol,在标准状况下其体积为_______ , 0.4molOH-的中有_______ 个电子。
(2)同温同压下,SO3与SO2的密度之比为_______ ;若体积相同时,两种气体的氧原子数之比为_______ 。
(3)19g某二价金属的氯化物ACl2中含有0.4mol氯离子,ACl2的摩尔质量是_______ ,该物质的化学式可能是_______ 。
(4)将标准状况下的VLHCl气体溶于1000 g水中,得到的盐酸密度为ρg/cm3,则该盐酸的物质的量浓度为_______ 。
(1)3.01×1023个CO2分子的物质的量是
(2)同温同压下,SO3与SO2的密度之比为
(3)19g某二价金属的氯化物ACl2中含有0.4mol氯离子,ACl2的摩尔质量是
(4)将标准状况下的VLHCl气体溶于1000 g水中,得到的盐酸密度为ρg/cm3,则该盐酸的物质的量浓度为
您最近一年使用:0次



