1 . 将35.8gNa2CO3和NaHCO3的固体混合物溶于足量水中,向其中逐滴加入1mol·L-1的盐酸至不再产生气体为止,测得共产生CO28.96L(标准状况)(气体溶解忽略不计)。回答下列问题:
(1)原混合物中Na2CO3为___________ g。
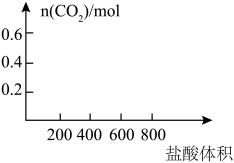
(2)若以滴加盐酸的体积为V(mL),产生气体的物质的量为n(mol),建立n=f(V)的函数关系,将V在不同取值范围时,n=f(V)的关系式填入下表并作图。
___________
(1)原混合物中Na2CO3为
(2)若以滴加盐酸的体积为V(mL),产生气体的物质的量为n(mol),建立n=f(V)的函数关系,将V在不同取值范围时,n=f(V)的关系式填入下表并作图。
| V的取值范围 | n=f(V) |
您最近一年使用:0次
2 . 在标准状况下,将336LHCl气体溶解于1L水中,所得盐酸溶液的密度为1.18g/cm3.试计算这种盐酸溶液中溶质的物质的量浓度为___________ 。
您最近一年使用:0次
名校
3 . 硝酸与金属的反应
①先将5.6克铁粉与200mL一定浓度的稀硝酸混合使其充分反应,固体完全溶解,并收集到气体VL(已折算为标准状况);
②往反应后的溶液中加入一定量铜粉,铜粉恰好完全溶解,且溶解过程中无气泡产生;
③继续往溶液中加入足量NaOH溶液并过滤,将滤渣充分加热后得共到12g固体X.
回答下列问题:
(1)①中产生的气体为______ ,其体积为______ (标况下),写出产生该气体的化学方程式______ 。
(2)铜粉的质量为______ 写出铜粉溶解的离子方程式______ 。
(3)固体X中主要成分的物质的量之比为______ 。
①先将5.6克铁粉与200mL一定浓度的稀硝酸混合使其充分反应,固体完全溶解,并收集到气体VL(已折算为标准状况);
②往反应后的溶液中加入一定量铜粉,铜粉恰好完全溶解,且溶解过程中无气泡产生;
③继续往溶液中加入足量NaOH溶液并过滤,将滤渣充分加热后得共到12g固体X.
回答下列问题:
(1)①中产生的气体为
(2)铜粉的质量为
(3)固体X中主要成分的物质的量之比为
您最近一年使用:0次
4 . 制取SO2的方程式为: ,将12.6g Na2SO3与足量浓硫酸反应,求制得标准状况下SO2的体积
,将12.6g Na2SO3与足量浓硫酸反应,求制得标准状况下SO2的体积
您最近一年使用:0次
名校
5 . 电解饱和食盐水的化学反应方程式为 ,现电解消耗
,现电解消耗 的质量为
的质量为 ,完全反应后,测得烧杯中剩余溶液的质量是
,完全反应后,测得烧杯中剩余溶液的质量是 ,请计算:
,请计算:
(1)求消耗的 的物质的量
的物质的量_______ 。
(2)求生成的 在标准状况下的体积
在标准状况下的体积_______ 。
(3)求生成的 的质量
的质量_______ 。
(4)反应后所得 溶液的溶质质量分数
溶液的溶质质量分数_______ 。
 ,现电解消耗
,现电解消耗 的质量为
的质量为 ,完全反应后,测得烧杯中剩余溶液的质量是
,完全反应后,测得烧杯中剩余溶液的质量是 ,请计算:
,请计算:(1)求消耗的
 的物质的量
的物质的量(2)求生成的
 在标准状况下的体积
在标准状况下的体积(3)求生成的
 的质量
的质量(4)反应后所得
 溶液的溶质质量分数
溶液的溶质质量分数
您最近一年使用:0次
名校
6 . 物质的量是高中化学常用的物理量,请完成以下有关计算。
(1)___________ mol  所含原子数与0.2 mol
所含原子数与0.2 mol  所含原子数相等。
所含原子数相等。
(2)483 g 中所含的
中所含的 的物质的量是
的物质的量是___________ mol,所含 的数目是
的数目是___________ 。
(3)1 mol 中含有
中含有___________ mol电子。
(4)在标准状况下,2.24 L CO与 的质量为3.6 g,则混合气体中CO与
的质量为3.6 g,则混合气体中CO与 的分子数之比为
的分子数之比为___________ 。
(5)4 g 物质的量是
物质的量是___________ mol,在标准状况下的体积是___________ L。
(6)在氯化镁和硫酸镁的混合液中,若 与
与 的物质的量之比为4∶3,则
的物质的量之比为4∶3,则 与
与 的物质的量之比为
的物质的量之比为___________ 。
(1)
 所含原子数与0.2 mol
所含原子数与0.2 mol  所含原子数相等。
所含原子数相等。(2)483 g
 中所含的
中所含的 的物质的量是
的物质的量是 的数目是
的数目是(3)1 mol
 中含有
中含有(4)在标准状况下,2.24 L CO与
 的质量为3.6 g,则混合气体中CO与
的质量为3.6 g,则混合气体中CO与 的分子数之比为
的分子数之比为(5)4 g
 物质的量是
物质的量是(6)在氯化镁和硫酸镁的混合液中,若
 与
与 的物质的量之比为4∶3,则
的物质的量之比为4∶3,则 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
7 . 回答下列问题:
(1)含有0.4molAl3+的Al2(SO4)3中,所含有的SO 的物质的量为
的物质的量为________ 。
(2)已知16gA和20gB恰好完全反应生成0.04mol的C和31.76g的D,则C的摩尔质量为_______ 。
(3)如果ag某气体中的分子数为b,则cg该气体在标准状况下的体积为_______ (设NA为阿伏加德罗常数)。
(4)把VL含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含amolNaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含bmolBaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为________ 。
(1)含有0.4molAl3+的Al2(SO4)3中,所含有的SO
 的物质的量为
的物质的量为(2)已知16gA和20gB恰好完全反应生成0.04mol的C和31.76g的D,则C的摩尔质量为
(3)如果ag某气体中的分子数为b,则cg该气体在标准状况下的体积为
(4)把VL含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含amolNaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含bmolBaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为
您最近一年使用:0次
名校
解题方法
8 . 物质的量是高中化学常用的物理量,请完成以下有关计算。
(1)0.5molCH4的质量是_______ ,在标准状况下的体积为_______ 。
(2)_______ molH2O2所含原子数与0.2molH3PO4所含原子数相等。
(3)3.1gNa2X含有Na+0.1mol,则X的相对原子质量为_______ 。
(4)a个X原子的总质量为bg,则X的相对原子质量可以表示为_______ (用NA表示阿伏加德罗常数的值)。
(5)在氯化镁和硫酸镁的混合液中,若Mg2+与Cl-的物质的量之比为4∶3,则Mg2+与 的物质的量之比为
的物质的量之比为_______ 。
(1)0.5molCH4的质量是
(2)
(3)3.1gNa2X含有Na+0.1mol,则X的相对原子质量为
(4)a个X原子的总质量为bg,则X的相对原子质量可以表示为
(5)在氯化镁和硫酸镁的混合液中,若Mg2+与Cl-的物质的量之比为4∶3,则Mg2+与
 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
9 . 化学反应过程伴随有热量的变化。
(1)在尿素合成塔中的主要反应可表示如下:
反应I:
反应Ⅱ: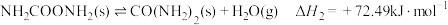
总反应: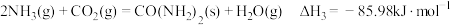
则反应I的
___________  。
。
(2)利用CH4可制备乙烯及合成气(CO、H2)。
①有关化学键键能(E)的数据如下表:
则

___________ 。(用a、b、c、d表示)
②制备合成气反应历程分两步(步骤I、步骤Ⅱ,反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:
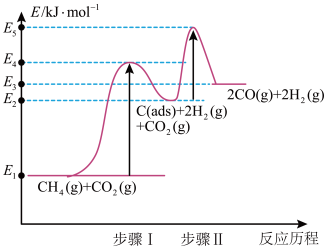
步骤1反应的焓变 为
为___________ kJ/mol(选用E1~E5的关系式表示)。
③反应 的焓变为
的焓变为 ,与步骤1焓变
,与步骤1焓变 相比,
相比,
___________  (填“>”或“<)。
(填“>”或“<)。
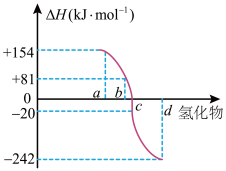
(3)一定条件下,由稳定单质反应生成1mol化合物的反应热叫该化合物的生成热( )。下图为VIA族元素(O、S、Se、Te)氢化物a、b、c、d的生成热数据示意图。已知非金属元素气态氢化物的稳定性越强,其氢化物的生成热
)。下图为VIA族元素(O、S、Se、Te)氢化物a、b、c、d的生成热数据示意图。已知非金属元素气态氢化物的稳定性越强,其氢化物的生成热 越小。硫化氢发生分解反应的热化学方程式为
越小。硫化氢发生分解反应的热化学方程式为___________ 。
(1)在尿素合成塔中的主要反应可表示如下:
反应I:

反应Ⅱ:
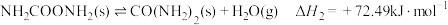
总反应:
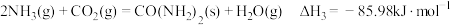
则反应I的

 。
。(2)利用CH4可制备乙烯及合成气(CO、H2)。
①有关化学键键能(E)的数据如下表:
| 化学键 | H—H | C=C | C—C | C—H |
| E(kJ/mol) | a | b | c | d |


②制备合成气反应历程分两步(步骤I、步骤Ⅱ,反应中C(ads)为吸附性活性炭,反应历程的能量变化如图:

步骤1反应的焓变
 为
为③反应
 的焓变为
的焓变为 ,与步骤1焓变
,与步骤1焓变 相比,
相比,
 (填“>”或“<)。
(填“>”或“<)。(3)一定条件下,由稳定单质反应生成1mol化合物的反应热叫该化合物的生成热(
 )。下图为VIA族元素(O、S、Se、Te)氢化物a、b、c、d的生成热数据示意图。已知非金属元素气态氢化物的稳定性越强,其氢化物的生成热
)。下图为VIA族元素(O、S、Se、Te)氢化物a、b、c、d的生成热数据示意图。已知非金属元素气态氢化物的稳定性越强,其氢化物的生成热 越小。硫化氢发生分解反应的热化学方程式为
越小。硫化氢发生分解反应的热化学方程式为
您最近一年使用:0次
名校
10 . 请根据要求回答下列问题:
(1)49g 的物质的量是
的物质的量是_______ mol,含_______ 个 分子,与
分子,与_______ mol NaOH恰好完全中和。
(2)在标准状况下,3.4g 所占的体积为
所占的体积为_______ L,它与标况下_______ L  所含的氢原子数目相同。
所含的氢原子数目相同。
(3)等质量的 和
和 ,它们的物质的量之比为
,它们的物质的量之比为_______ ,所含分子数之比为_______ ,所含原子数之比为_______ 。
(4)某气态氧化物的化学式为 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为_______ ,R的相对原子质量为_______ 。
(5)若a g某气体中含有的分子数为b个,则c g该气体在标准状况下的体积为_______ 。(设 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
(1)49g
 的物质的量是
的物质的量是 分子,与
分子,与(2)在标准状况下,3.4g
 所占的体积为
所占的体积为 所含的氢原子数目相同。
所含的氢原子数目相同。(3)等质量的
 和
和 ,它们的物质的量之比为
,它们的物质的量之比为(4)某气态氧化物的化学式为
 ,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为
,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩尔质量为(5)若a g某气体中含有的分子数为b个,则c g该气体在标准状况下的体积为
 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
您最近一年使用:0次



