名校
解题方法
1 . 现有 和
和 的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g,
的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g, 的质量分数为
的质量分数为___________ ?若参考值为0.850,则相对偏差为___________ ?请写出以上两个数据的计算过程。
 和
和 的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g,
的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38g, 的质量分数为
的质量分数为
您最近一年使用:0次
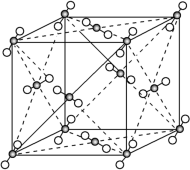
2 . 下图为干冰的晶胞:___________  。(设
。(设 为阿伏伽德罗常数,
为阿伏伽德罗常数,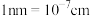 )
)
 。(设
。(设 为阿伏伽德罗常数,
为阿伏伽德罗常数,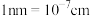 )
)
您最近一年使用:0次
名校
3 . 完全燃烧某气态烷烃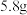 ,得到
,得到 二氧化碳和
二氧化碳和 水。求:
水。求:
(1)此烷烃的相对分子质量_____ 。
(2)此烷烃的化学式_____ 。
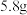 ,得到
,得到 二氧化碳和
二氧化碳和 水。求:
水。求:(1)此烷烃的相对分子质量
(2)此烷烃的化学式
您最近一年使用:0次
4 . 0.2mol某烃A在氧气中充分燃烧后,生成化合物B、C各1.2mol,试回答:
(1)烃A的分子式为______ 。
(2)若取一定量的烃A完全燃烧后,生成B、C各3mol,则有____ g烃A参加了反应,燃烧时消耗标准状况下的氧气____ L。
(3)若烃A不能使溴水褪色,但在一定条件下,能与氯气发生取代反应,其氯代物只有一种,则烃A的结构简式为_______ 。
(4)若烃A能使溴水褪色,且在催化剂作用下,与 加成所得产物的分子中含4个甲基,烃A可能的结构简式为
加成所得产物的分子中含4个甲基,烃A可能的结构简式为_______ ,比烃A少2个碳原子的同系物,且能和 发生加成反应生成2-甲基丙烷的是
发生加成反应生成2-甲基丙烷的是_______ (填结构简式),它与溴的四氯化碳溶液反应的化学方程式为_______ 。
(1)烃A的分子式为
(2)若取一定量的烃A完全燃烧后,生成B、C各3mol,则有
(3)若烃A不能使溴水褪色,但在一定条件下,能与氯气发生取代反应,其氯代物只有一种,则烃A的结构简式为
(4)若烃A能使溴水褪色,且在催化剂作用下,与
 加成所得产物的分子中含4个甲基,烃A可能的结构简式为
加成所得产物的分子中含4个甲基,烃A可能的结构简式为 发生加成反应生成2-甲基丙烷的是
发生加成反应生成2-甲基丙烷的是
您最近一年使用:0次
解题方法
5 . 现有一份部分被氧化的铜片(氧化产物为CuO),称取4.32g铜片,溶于一定体积1.00mol•L-1稀硝酸中,反应恰好完全进行,收集到无色气体448mL(已折算为标准状况)。
(1)该稀硝酸中所含HNO3的物质的量为___________ ;
(2)该铜片被氧化的百分数为___________ 。
(1)该稀硝酸中所含HNO3的物质的量为
(2)该铜片被氧化的百分数为
您最近一年使用:0次
名校
解题方法
6 . 现有下列8种物质:① ②小苏打 ③
②小苏打 ③ 溶液 ④
溶液 ④ ⑤酒精 ⑥
⑤酒精 ⑥ ⑦氢氧化铁胶体 ⑧空气
⑦氢氧化铁胶体 ⑧空气
(1) 属于分散系的是___________ (填物质序号),小苏打在水中的电离方程式为___________ 。工业制漂白粉的方程式是___________ 。
(2)若氢氧化铁胶体中混有少量的 溶液,提纯的方法是___________。
溶液,提纯的方法是___________。
(3) ⑤酒精分子中含氢原子的物质的量为
⑤酒精分子中含氢原子的物质的量为___________ ,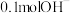 所含电子为
所含电子为___________ 个。
(4)同质量的 和
和 气体在相同条件下的体积比为
气体在相同条件下的体积比为___________ ,其中含有的氢原子数目比为___________ ,由 和
和 组成的混合气体20克,标准状态下体积
组成的混合气体20克,标准状态下体积 ,则氨气与氢气的物质的量为
,则氨气与氢气的物质的量为___________ 。
 ②小苏打 ③
②小苏打 ③ 溶液 ④
溶液 ④ ⑤酒精 ⑥
⑤酒精 ⑥ ⑦氢氧化铁胶体 ⑧空气
⑦氢氧化铁胶体 ⑧空气(1) 属于分散系的是
(2)若氢氧化铁胶体中混有少量的
 溶液,提纯的方法是___________。
溶液,提纯的方法是___________。| A.蒸馏(分馏) | B.过滤 | C.渗析 | D.蒸发 |
 ⑤酒精分子中含氢原子的物质的量为
⑤酒精分子中含氢原子的物质的量为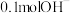 所含电子为
所含电子为(4)同质量的
 和
和 气体在相同条件下的体积比为
气体在相同条件下的体积比为 和
和 组成的混合气体20克,标准状态下体积
组成的混合气体20克,标准状态下体积 ,则氨气与氢气的物质的量为
,则氨气与氢气的物质的量为
您最近一年使用:0次
名校
解题方法
7 . 回答下列问题
(1)已知:
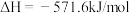

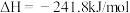
①则氢气的燃烧热
___________ ;
②计算

___________ ;
③计算1g氢气完全燃烧生成气态水时放出___________ kJ的热量。
(2)已知:①
 ;
;
②
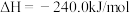 ;
;
③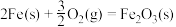
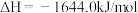 ;
;
则反应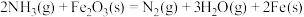

___________  。
。
(1)已知:

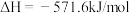

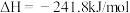
①则氢气的燃烧热

②计算


③计算1g氢气完全燃烧生成气态水时放出
(2)已知:①

 ;
;②

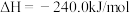 ;
;③
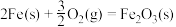
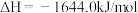 ;
;则反应
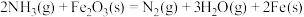

 。
。
您最近一年使用:0次
8 . 将35.8gNa2CO3和NaHCO3的固体混合物溶于足量水中,向其中逐滴加入1mol·L-1的盐酸至不再产生气体为止,测得共产生CO28.96L(标准状况)(气体溶解忽略不计)。回答下列问题:
(1)原混合物中Na2CO3为___________ g。
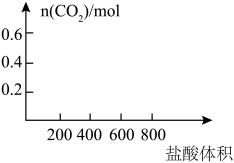
(2)若以滴加盐酸的体积为V(mL),产生气体的物质的量为n(mol),建立n=f(V)的函数关系,将V在不同取值范围时,n=f(V)的关系式填入下表并作图。
___________
(1)原混合物中Na2CO3为
(2)若以滴加盐酸的体积为V(mL),产生气体的物质的量为n(mol),建立n=f(V)的函数关系,将V在不同取值范围时,n=f(V)的关系式填入下表并作图。
| V的取值范围 | n=f(V) |
您最近一年使用:0次
9 . 在标准状况下,将336LHCl气体溶解于1L水中,所得盐酸溶液的密度为1.18g/cm3.试计算这种盐酸溶液中溶质的物质的量浓度为___________ 。
您最近一年使用:0次
解题方法
10 . 铝是典型的两性金属,既能与酸反应,又能与强碱溶液反应。回答下列问题:
(1)在铝分别与盐酸和氢氧化钠溶液的反应中,铝元素化合价的变化都是___________ (升高/降低),还原剂都是___________ 。
(2)1mol的铝分别与足量的稀盐酸和氢氧化钠溶液反应,生成氢气的体积在相同状况下比值为___________ ,消耗氯化氢和氢氧化钠的物质的量之比为___________ 。
甲、乙两个烧杯中分别盛有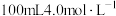 的盐酸和
的盐酸和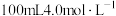 氢氧化钠溶液,向两个烧杯中都加入5.4g铝粉,在相同状况下产生气体的体积比为
氢氧化钠溶液,向两个烧杯中都加入5.4g铝粉,在相同状况下产生气体的体积比为___________ 。反应中消耗的NaOH与HCl的物质的量之比为___________ 。
(1)在铝分别与盐酸和氢氧化钠溶液的反应中,铝元素化合价的变化都是
(2)1mol的铝分别与足量的稀盐酸和氢氧化钠溶液反应,生成氢气的体积在相同状况下比值为
甲、乙两个烧杯中分别盛有
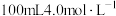 的盐酸和
的盐酸和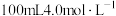 氢氧化钠溶液,向两个烧杯中都加入5.4g铝粉,在相同状况下产生气体的体积比为
氢氧化钠溶液,向两个烧杯中都加入5.4g铝粉,在相同状况下产生气体的体积比为
您最近一年使用:0次



