名校
1 . (1)在Fe+4HNO3=Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现的性质是_______
A.酸性 B.氧化性 C.还原性 D.碱性
若反应生成标准状况下11.2 L NO,则被还原的HNO3为_______ mol,转移电子为_______ mol。
(2)已知NO不溶于水,NO2易溶于水,且与水发生反应3NO2+H2O=2HNO3+NO。把盛有48 mL NO和NO2混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为24 mL,则:
①原混合气中,NO是_______ mL,NO2是_______ mL。
②若在剩余的24 mL气体中,通入6 mL O2,待液面稳定后,反应后容器内剩余气体体积为_______ mL。
③若在原48 mL NO、NO2中,通入_______ mLO2再倒置于水中,气体会全部被吸收。
A.酸性 B.氧化性 C.还原性 D.碱性
若反应生成标准状况下11.2 L NO,则被还原的HNO3为
(2)已知NO不溶于水,NO2易溶于水,且与水发生反应3NO2+H2O=2HNO3+NO。把盛有48 mL NO和NO2混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为24 mL,则:
①原混合气中,NO是
②若在剩余的24 mL气体中,通入6 mL O2,待液面稳定后,反应后容器内剩余气体体积为
③若在原48 mL NO、NO2中,通入
您最近一年使用:0次
2021-05-06更新
|
630次组卷
|
2卷引用:武汉市江夏实验高中2020-2021学年高一下学期3月月考化学试题
2 . 亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____ ___
___ ___=___
___=___ ___
___ ___
___ ___
___ ___
___ 。
。
(1)请完成该离子方程式并配平___________ 。
(2)从物质分类角度来看, 是
是___________ (填字母代号)。
a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质 f.钠盐
(3)用上述反应来处理 开不是最佳方法,其原因是
开不是最佳方法,其原因是___________ 。从环保角度来讲,要将 转化为氮气,所用物质的
转化为氮气,所用物质的___________ 填“氧化性”或“还原性”)应该比KI更___________ (填“强”或“弱”)。
(4)下列方法不能用来区分固体 和NaCl的是___________(填序号)
和NaCl的是___________(填序号)
(5)误食 会导致人体血红蛋白中的
会导致人体血红蛋白中的 车转化为
车转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列:
表现出的性质与下列:___________ (填序号)反应中 表现出的性质相同。
表现出的性质相同。
A.
B.
C.
(6) 可以与
可以与 反应制备
反应制备 纳米颗粒。若
纳米颗粒。若 与
与 的系数之比为1∶2,配平该反应的离子方程式:
的系数之比为1∶2,配平该反应的离子方程式:___________ 。
____ _____
_____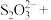 _____
_____ ____
____ ____
____ ______
______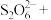 _____
_____
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____ ___
___ ___=___
___=___ ___
___ ___
___ ___
___ ___
___ 。
。(1)请完成该离子方程式并配平
(2)从物质分类角度来看,
 是
是a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质 f.钠盐
(3)用上述反应来处理
 开不是最佳方法,其原因是
开不是最佳方法,其原因是 转化为氮气,所用物质的
转化为氮气,所用物质的(4)下列方法不能用来区分固体
 和NaCl的是___________(填序号)
和NaCl的是___________(填序号)| A.分别溶于水,滴加酚酞试液 | B.分别溶于水并滴加 酸化的 酸化的 溶液 溶液 |
| C.分别加强热并收集气体检验 | D.用筷子分别蘸取固体品尝味道 |
 会导致人体血红蛋白中的
会导致人体血红蛋白中的 车转化为
车转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列:
表现出的性质与下列: 表现出的性质相同。
表现出的性质相同。A.

B.

C.

(6)
 可以与
可以与 反应制备
反应制备 纳米颗粒。若
纳米颗粒。若 与
与 的系数之比为1∶2,配平该反应的离子方程式:
的系数之比为1∶2,配平该反应的离子方程式:____
 _____
_____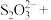 _____
_____ ____
____ ____
____ ______
______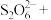 _____
_____
您最近一年使用:0次
19-20高三·浙江·阶段练习
3 . 工业次氯酸钠溶液中含有氯酸钠,测定次氯酸钠样品中的氯酸钠含量的方法如下:取10.00 mL碱性NaClO溶液试样,加入过量H2O2,将次氯酸钠完全还原为氯化钠(ClO 在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性)。加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol/L硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol/L酸性K2Cr2O7溶液滴定至终点,消耗该溶液20.00 mL。已知:
在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性)。加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol/L硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol/L酸性K2Cr2O7溶液滴定至终点,消耗该溶液20.00 mL。已知: +6Fe2++6H+=Cl-+6Fe3++3H2O;
+6Fe2++6H+=Cl-+6Fe3++3H2O; +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O
(1)与K2Cr2O7反应的硫酸亚铁的物质的量为_______ mol。
(2)计算样品中NaClO3的含量为_______ g/L,写出计算过程。
 在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性)。加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol/L硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol/L酸性K2Cr2O7溶液滴定至终点,消耗该溶液20.00 mL。已知:
在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性)。加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol/L硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol/L酸性K2Cr2O7溶液滴定至终点,消耗该溶液20.00 mL。已知: +6Fe2++6H+=Cl-+6Fe3++3H2O;
+6Fe2++6H+=Cl-+6Fe3++3H2O; +6Fe2++14H+=2Cr3++6Fe3++7H2O
+6Fe2++14H+=2Cr3++6Fe3++7H2O(1)与K2Cr2O7反应的硫酸亚铁的物质的量为
(2)计算样品中NaClO3的含量为
您最近一年使用:0次
4 . 实验室可以用高锰酸钾与浓盐酸反应制取氯气,反应方程式如下:
2KMnO4+16HCl = 2KCl+2MnCl2+5Cl2↑+8H2O
请完成下列问题:
(1)在上述方程式中用双线桥法标注电子转移情况____________ 。
(2)浓盐酸在该反应中表现了____________ (选填“氧化性”、“还原性”或“酸性”)。
(3)若15.8g KMnO4与足量的浓盐酸充分反应,则有______ mol HCl被氧化,产生的Cl2在标准状况下的体积为__________ L。
2KMnO4+16HCl = 2KCl+2MnCl2+5Cl2↑+8H2O
请完成下列问题:
(1)在上述方程式中用双线桥法标注电子转移情况
(2)浓盐酸在该反应中表现了
(3)若15.8g KMnO4与足量的浓盐酸充分反应,则有
您最近一年使用:0次
2018-12-30更新
|
358次组卷
|
3卷引用:河北省秦皇岛市昌黎县第八中学2019-2020学年高一上学期12月月考化学考试题
名校
5 . 肼是一种强还原剂,用NaClO与NH3反应可用于生产肼(N2H4),其反应的化学方程式为:NaClO+2NH3= N2H4+NaCl+H2O。
⑴生产1000 g质量分数为25.6%的肼溶液最少需要___________ L(标准状况)NH3。
⑵工业次氯酸钠溶液中含有氯酸钠会影响所得肼的产品质量。测定次氯酸钠样品中的氯酸钠含量的方法如下:取10.00 mL 碱性NaClO溶液试样,加入过量H2O2,将次氯酸钠完全还原( 在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性),加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol·L-1 硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol·L-1酸性K2Cr2O7溶液滴定至终点(
在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性),加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol·L-1 硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol·L-1酸性K2Cr2O7溶液滴定至终点( 被还原为Cr3+),消耗该溶液20.00 mL。
被还原为Cr3+),消耗该溶液20.00 mL。
①用H2O2与次氯酸钠反应的离子方程式为___________ 。
②实验中加热煮沸的目的是___________ 。
③计算样品中NaClO3的含量(以g·L-1表示),写出计算过程。___________
⑴生产1000 g质量分数为25.6%的肼溶液最少需要
⑵工业次氯酸钠溶液中含有氯酸钠会影响所得肼的产品质量。测定次氯酸钠样品中的氯酸钠含量的方法如下:取10.00 mL 碱性NaClO溶液试样,加入过量H2O2,将次氯酸钠完全还原(
 在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性),加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol·L-1 硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol·L-1酸性K2Cr2O7溶液滴定至终点(
在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性),加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol·L-1 硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol·L-1酸性K2Cr2O7溶液滴定至终点( 被还原为Cr3+),消耗该溶液20.00 mL。
被还原为Cr3+),消耗该溶液20.00 mL。①用H2O2与次氯酸钠反应的离子方程式为
②实验中加热煮沸的目的是
③计算样品中NaClO3的含量(以g·L-1表示),写出计算过程。
您最近一年使用:0次
2017-04-16更新
|
634次组卷
|
4卷引用:江苏省溧水高级中学2019届高三上学期10月学情调研考试化学试题
解题方法
6 . 含钠化合物与含硫化合物可发生多种反应,请回答下列问题:
(1)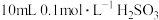 溶液与6.9gNa反应,生成的H2在标准状况下的体积为
溶液与6.9gNa反应,生成的H2在标准状况下的体积为___ L。
(2)SO2与少量NaOH溶液反应的离子方程式为___ 。
(3)查阅资料知Na2O2具有强氧化性,Na2O2与SO2反应的化学方程式为____ 。
(4)用热的NaOH溶液与硫粉反应中,氧化剂与还原剂的质量之比为___ ,当转移0.4mol电子时,生成Na2S的质量为___ g。
(1)
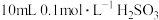 溶液与6.9gNa反应,生成的H2在标准状况下的体积为
溶液与6.9gNa反应,生成的H2在标准状况下的体积为(2)SO2与少量NaOH溶液反应的离子方程式为
(3)查阅资料知Na2O2具有强氧化性,Na2O2与SO2反应的化学方程式为
(4)用热的NaOH溶液与硫粉反应中,氧化剂与还原剂的质量之比为
您最近一年使用:0次
7 . 饮用水中NO 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO
的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO 还原为N2。
还原为N2。
(1)①配平方程式:_______Al+____NO +_____OH↑+____=_____[Al(OH)4] ↑+____N2↑
+_____OH↑+____=_____[Al(OH)4] ↑+____N2↑
______
②上述反应中,还原剂与还原产物的物质的量之比是_______ ,反应中转移电子0.3mol,生成_______ mLN2(标准状况下)。
(2)①已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为_______ 。
②Na2S2O3具有较强还原性,能作为织锦物漂白后的脱氯剂,脱氯后S2O 转变为SO
转变为SO 。现需处理含标准状况下2.24L Cl2的织锦物,理论上需要0.1mol/L Na2S2O3溶液的体积为
。现需处理含标准状况下2.24L Cl2的织锦物,理论上需要0.1mol/L Na2S2O3溶液的体积为_______ mL。
 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO
的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO 还原为N2。
还原为N2。(1)①配平方程式:_______Al+____NO
 +_____OH↑+____=_____[Al(OH)4] ↑+____N2↑
+_____OH↑+____=_____[Al(OH)4] ↑+____N2↑②上述反应中,还原剂与还原产物的物质的量之比是
(2)①已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为
②Na2S2O3具有较强还原性,能作为织锦物漂白后的脱氯剂,脱氯后S2O
 转变为SO
转变为SO 。现需处理含标准状况下2.24L Cl2的织锦物,理论上需要0.1mol/L Na2S2O3溶液的体积为
。现需处理含标准状况下2.24L Cl2的织锦物,理论上需要0.1mol/L Na2S2O3溶液的体积为
您最近一年使用:0次
名校
8 . 3.84g Fe和Fe2O3的混合物溶于100mL某浓度的盐酸中,恰好使混合物溶解,生成0.03mol H2,向反应后的溶液中加入KSCN检验,溶液无明显现象,设HCl无挥发,反应后溶液的体积不变.(已知:氧化性Fe3+>H+,还原性Fe>Cl﹣)
(1)求原混合物中Fe和Fe2O3的物质的量分别为多少?
(2)求反应后Cl﹣的物质的量浓度?
(1)求原混合物中Fe和Fe2O3的物质的量分别为多少?
(2)求反应后Cl﹣的物质的量浓度?
您最近一年使用:0次
2018-01-17更新
|
265次组卷
|
2卷引用:江西省南昌市八一中学2017-2018学年高一1月月考化学试题
名校
9 . I.氢化亚铜(CuH)是一种难溶物质,用CuSO4溶液和“另一物质”在40~50℃时反应可生成它。CuH具有的性质有:不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;Cu+在酸性条件下发生的反应是:2Cu+ = Cu2++Cu。根据以上信息,结合自己所掌握的化学知识,回答下列问题:
(1)用CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中作____ (填“氧化剂”或“还原剂”)。
(2)CuH溶解在稀盐酸中生成的气体是_____ (填化学式)。
(3)氯气具有很强的氧化性,能将多数物质氧化到较高价态,试写出CuH在氯气中燃烧的化学反应方程式:____
II.已知PbO2具有强氧化性,某强酸性反应体系中,反应物和生成物共六种物质:PbO2、PbSO4(难溶盐)、Pb(MnO4)2(强电解质)、H2O、X(水溶液呈无色)、H2SO4,已知X是一种盐,且0.1 mol X在该反应中失去3.01×1023个电子。
(4)写出X的化学式:_______ ;
(5)若有9.8 g H2SO4参加反应,则转移电子的物质的量为_______ mol
III.下列有关说法正确的有_______
①过氧化钠与二氧化硫反应类似于过氧化钠与二氧化碳反应
②室温下,Al与少量NaOH溶液反应生成Al(OH)3
③金属钠储存在装有煤油的广口瓶中
④可用浓硫酸干燥二氧化硫
⑤明矾可用作净水剂和消毒剂
⑥用二氧化碳灭火器扑灭金属钾的燃烧
⑦湿润的红色酚酞试纸遇氯化氢气体变无色
(1)用CuSO4溶液和“另一物质”制CuH的反应中,用氧化还原观点分析,这“另一物质”在反应中作
(2)CuH溶解在稀盐酸中生成的气体是
(3)氯气具有很强的氧化性,能将多数物质氧化到较高价态,试写出CuH在氯气中燃烧的化学反应方程式:
II.已知PbO2具有强氧化性,某强酸性反应体系中,反应物和生成物共六种物质:PbO2、PbSO4(难溶盐)、Pb(MnO4)2(强电解质)、H2O、X(水溶液呈无色)、H2SO4,已知X是一种盐,且0.1 mol X在该反应中失去3.01×1023个电子。
(4)写出X的化学式:
(5)若有9.8 g H2SO4参加反应,则转移电子的物质的量为
III.下列有关说法正确的有
①过氧化钠与二氧化硫反应类似于过氧化钠与二氧化碳反应
②室温下,Al与少量NaOH溶液反应生成Al(OH)3
③金属钠储存在装有煤油的广口瓶中
④可用浓硫酸干燥二氧化硫
⑤明矾可用作净水剂和消毒剂
⑥用二氧化碳灭火器扑灭金属钾的燃烧
⑦湿润的红色酚酞试纸遇氯化氢气体变无色
您最近一年使用:0次
10 . 一块表面已部分被氧化为氧化钠的金属钠样品5.4g,将其投入94.7g 水中,放出1120mL H2(标准状况下)。
(1)请写出该样品放入水中时发生的反应的化学方程式:_______ 。滴加酚酞后溶液颜色_______ ,由此可知溶液呈_______ (“酸性”“碱性” 、 或“中性”)。
(2)样品中含金属钠_______ g。
(3)所得的溶液的质量分数为_______ 。
(1)请写出该样品放入水中时发生的反应的化学方程式:
(2)样品中含金属钠
(3)所得的溶液的质量分数为
您最近一年使用:0次
2017-10-22更新
|
398次组卷
|
2卷引用:福建省三明市第一中学2017-2018学年高一上学期第一次月考化学试题



