亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____ ___
___ ___=___
___=___ ___
___ ___
___ ___
___ ___
___ 。
。
(1)请完成该离子方程式并配平___________ 。
(2)从物质分类角度来看, 是
是___________ (填字母代号)。
a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质 f.钠盐
(3)用上述反应来处理 开不是最佳方法,其原因是
开不是最佳方法,其原因是___________ 。从环保角度来讲,要将 转化为氮气,所用物质的
转化为氮气,所用物质的___________ 填“氧化性”或“还原性”)应该比KI更___________ (填“强”或“弱”)。
(4)下列方法不能用来区分固体 和NaCl的是___________(填序号)
和NaCl的是___________(填序号)
(5)误食 会导致人体血红蛋白中的
会导致人体血红蛋白中的 车转化为
车转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列:
表现出的性质与下列:___________ (填序号)反应中 表现出的性质相同。
表现出的性质相同。
A.
B.
C.
(6) 可以与
可以与 反应制备
反应制备 纳米颗粒。若
纳米颗粒。若 与
与 的系数之比为1∶2,配平该反应的离子方程式:
的系数之比为1∶2,配平该反应的离子方程式:___________ 。
____ _____
_____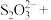 _____
_____ ____
____ ____
____ ______
______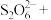 _____
_____
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性,能与
,其水溶液呈碱性,能与 溶液反应生成难溶于水、易溶于酸的
溶液反应生成难溶于水、易溶于酸的 。由于
。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:____ ___
___ ___=___
___=___ ___
___ ___
___ ___
___ ___
___ 。
。(1)请完成该离子方程式并配平
(2)从物质分类角度来看,
 是
是a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质 f.钠盐
(3)用上述反应来处理
 开不是最佳方法,其原因是
开不是最佳方法,其原因是 转化为氮气,所用物质的
转化为氮气,所用物质的(4)下列方法不能用来区分固体
 和NaCl的是___________(填序号)
和NaCl的是___________(填序号)| A.分别溶于水,滴加酚酞试液 | B.分别溶于水并滴加 酸化的 酸化的 溶液 溶液 |
| C.分别加强热并收集气体检验 | D.用筷子分别蘸取固体品尝味道 |
 会导致人体血红蛋白中的
会导致人体血红蛋白中的 车转化为
车转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列:
表现出的性质与下列: 表现出的性质相同。
表现出的性质相同。A.

B.

C.

(6)
 可以与
可以与 反应制备
反应制备 纳米颗粒。若
纳米颗粒。若 与
与 的系数之比为1∶2,配平该反应的离子方程式:
的系数之比为1∶2,配平该反应的离子方程式:____
 _____
_____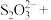 _____
_____ ____
____ ____
____ ______
______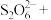 _____
_____
更新时间:2023-12-19 11:08:43
|
相似题推荐
计算题
|
较难
(0.4)
名校
【推荐1】根据要求,完成下列各题:
(1)把含有 和
和 的混合溶液VL分成两等份,一份加入含a mol
的混合溶液VL分成两等份,一份加入含a mol 的溶液,恰好使
的溶液,恰好使 完全沉淀:另一份加入含bmol NaOH的溶液,恰好使
完全沉淀:另一份加入含bmol NaOH的溶液,恰好使 完全转化为沉淀,则原混合溶液中
完全转化为沉淀,则原混合溶液中 的数目为
的数目为___________ 。
(2)某气态氧化物化学式为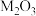 ,在标准状况下,1.52g该氧化物的体积是448mL,则M的摩尔质量为
,在标准状况下,1.52g该氧化物的体积是448mL,则M的摩尔质量为___________ 。
(3)标准状况下,把11.2L 通入一定量的过氧化钠固体中,充分反应后收集到8.96L气体,则这8.96L气体的质量是
通入一定量的过氧化钠固体中,充分反应后收集到8.96L气体,则这8.96L气体的质量是___________ g。
(4)现有下列10种物质:①铜②熔融NaCl③盐酸④液氯⑤ 晶体⑥胆矾⑦碳酸钙⑧
晶体⑥胆矾⑦碳酸钙⑧ ⑨氢氧化铁胶体⑩乙醇;上述物质中属于电解质的有
⑨氢氧化铁胶体⑩乙醇;上述物质中属于电解质的有___________ ,属于非电解质的有___________ ,能导电的有___________ 。(填序号)
(1)把含有
 和
和 的混合溶液VL分成两等份,一份加入含a mol
的混合溶液VL分成两等份,一份加入含a mol 的溶液,恰好使
的溶液,恰好使 完全沉淀:另一份加入含bmol NaOH的溶液,恰好使
完全沉淀:另一份加入含bmol NaOH的溶液,恰好使 完全转化为沉淀,则原混合溶液中
完全转化为沉淀,则原混合溶液中 的数目为
的数目为(2)某气态氧化物化学式为
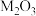 ,在标准状况下,1.52g该氧化物的体积是448mL,则M的摩尔质量为
,在标准状况下,1.52g该氧化物的体积是448mL,则M的摩尔质量为(3)标准状况下,把11.2L
 通入一定量的过氧化钠固体中,充分反应后收集到8.96L气体,则这8.96L气体的质量是
通入一定量的过氧化钠固体中,充分反应后收集到8.96L气体,则这8.96L气体的质量是(4)现有下列10种物质:①铜②熔融NaCl③盐酸④液氯⑤
 晶体⑥胆矾⑦碳酸钙⑧
晶体⑥胆矾⑦碳酸钙⑧ ⑨氢氧化铁胶体⑩乙醇;上述物质中属于电解质的有
⑨氢氧化铁胶体⑩乙醇;上述物质中属于电解质的有
您最近一年使用:0次
【推荐1】某反应中反应物与生成物有:NH3、H2SO4、KClO3、K2SO4、HNO3、H2O和一种未知物质X。
①已知KClO3在反应中得到电子,则该反应的还原剂是_____ 。
②已知0.2mol KClO3在反应中得到1mol电子生成X,则X的化学式为_____ 。
③根据上述反应可推知还原性:NH3_____ X (填>、<符号)。
①已知KClO3在反应中得到电子,则该反应的还原剂是
②已知0.2mol KClO3在反应中得到1mol电子生成X,则X的化学式为
③根据上述反应可推知还原性:NH3
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐2】在反应:8NH3+3Cl2==N2+6NH4Cl中,若共得到了28g氮气,试问:
(1)反应耗用的氧化剂的质量;_______________
(2)被氧化的还原剂的质量。_______________
(1)反应耗用的氧化剂的质量;
(2)被氧化的还原剂的质量。
您最近一年使用:0次
【推荐3】请按要求完成下列各题:
(1)黑火药爆炸时发生反应:2KNO3+S+3C═K2S+N2↑+3CO2↑,其中被还原的元素是___ ,被氧化的元素是___ 。
(2)配平以下方程式:___ K2Cr2O7+___ HCl═___ KCl+___ CrCl3+___ Cl2↑+___ H2O
(3)已知19.2gCu与过量的200ml5mol/L稀硝酸充分反应,反应方程式如下,请计算(忽略反应前后溶液体积的变化).
3Cu+8HNO3 3Cu(NO3)2+2NO↑+4H2O
3Cu(NO3)2+2NO↑+4H2O
①转移电子的物质的量为___ mol;标准状况下,产生NO气体的体积为___ mL。
②反应后,NO3-的物质的量浓度为___ mol/L。
(1)黑火药爆炸时发生反应:2KNO3+S+3C═K2S+N2↑+3CO2↑,其中被还原的元素是
(2)配平以下方程式:
(3)已知19.2gCu与过量的200ml5mol/L稀硝酸充分反应,反应方程式如下,请计算(忽略反应前后溶液体积的变化).
3Cu+8HNO3
 3Cu(NO3)2+2NO↑+4H2O
3Cu(NO3)2+2NO↑+4H2O①转移电子的物质的量为
②反应后,NO3-的物质的量浓度为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐1】(1)取300 mL 0.2 mol/L的 KI溶液与一定量的酸性 KMnO4 溶液恰好反应,生成等物质的量的 I2和 KIO3,则消耗 KMnO4的物质的量是________ mol。
(2)在 Fe(NO3)3 溶液中加入 Na2SO3 溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是___________________ ,又变为棕黄色的原因是(用离子方程式解释)________________________________________________ 。
(3)在 100 mLFeBr2 溶液中通入标准状况下3.36 L Cl2,溶液中有 1/4的 Br-被氧化成单质 Br2,则原 FeBr2溶液中 FeBr2 的物质的量浓度为________ mol/L。
(4)将Al、Al2O3和Al(OH)3的混合物恰好与NaOH溶液反应,反应后溶液中溶质的化学式__________________ 。向反应后的溶液中通入过量CO2,反应的离子方程式为__________________ 。
(5)三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式_______________________________________ ,反应中生成0.2 mol HNO3,转移的电子数目为_______________________ 。
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是_______ 。
(2)在 Fe(NO3)3 溶液中加入 Na2SO3 溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是
(3)在 100 mLFeBr2 溶液中通入标准状况下3.36 L Cl2,溶液中有 1/4的 Br-被氧化成单质 Br2,则原 FeBr2溶液中 FeBr2 的物质的量浓度为
(4)将Al、Al2O3和Al(OH)3的混合物恰好与NaOH溶液反应,反应后溶液中溶质的化学式
(5)三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】填写下列空白:
(1)工业上湿法制备高铁酸钾( )的反应体系中有六种微粒:
)的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 。写出并配平该反应的离子方程式
。写出并配平该反应的离子方程式___________ ;若反应过程中转移了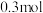 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为___________  。
。
(2)一定条件下,下列物质可以通过化合反应制得的有(写序号)___________ 。
①小苏打 ②硫酸铝 ③氯化亚铁 ④磁性氧化铁 ⑤铜绿(碱式碳酸铜) ⑥氢氧化铁
(3)向一定量的 的混合物中加入
的混合物中加入 的盐酸,恰好使混合物完全溶解,放出
的盐酸,恰好使混合物完全溶解,放出 (标准状况)的气体,在所得溶液中加入
(标准状况)的气体,在所得溶液中加入 溶液无血红色出现。若用足量的
溶液无血红色出现。若用足量的 在高温下还原相同质量的此混合物,能得到铁的质量是
在高温下还原相同质量的此混合物,能得到铁的质量是___________ g。
(4)将 铁粉与含有
铁粉与含有 的
的 溶液完全反应,铁粉全部溶解,并得到
溶液完全反应,铁粉全部溶解,并得到 铜,则参加反应的
铜,则参加反应的 与
与 的物质的量之比为
的物质的量之比为___________ 。
(5)等质量的铝分别与 浓度均为
浓度均为 的盐酸和氢氧化钠溶液反应,生成气体体积比为
的盐酸和氢氧化钠溶液反应,生成气体体积比为 ,铝与氢氧化钠溶液反应的离子方程式:
,铝与氢氧化钠溶液反应的离子方程式:___________ ;铝的质量为___________ g。
(6)将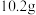 镁铝合金置于
镁铝合金置于 的盐酸中充分反应,无金属剩余,向反应后的溶液中加入
的盐酸中充分反应,无金属剩余,向反应后的溶液中加入 烧碱溶液,沉淀达到最大值,加入的烧碱的物质的量浓度为
烧碱溶液,沉淀达到最大值,加入的烧碱的物质的量浓度为___________  。
。
(1)工业上湿法制备高铁酸钾(
 )的反应体系中有六种微粒:
)的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 。写出并配平该反应的离子方程式
。写出并配平该反应的离子方程式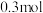 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为 。
。(2)一定条件下,下列物质可以通过化合反应制得的有(写序号)
①小苏打 ②硫酸铝 ③氯化亚铁 ④磁性氧化铁 ⑤铜绿(碱式碳酸铜) ⑥氢氧化铁
(3)向一定量的
 的混合物中加入
的混合物中加入 的盐酸,恰好使混合物完全溶解,放出
的盐酸,恰好使混合物完全溶解,放出 (标准状况)的气体,在所得溶液中加入
(标准状况)的气体,在所得溶液中加入 溶液无血红色出现。若用足量的
溶液无血红色出现。若用足量的 在高温下还原相同质量的此混合物,能得到铁的质量是
在高温下还原相同质量的此混合物,能得到铁的质量是(4)将
 铁粉与含有
铁粉与含有 的
的 溶液完全反应,铁粉全部溶解,并得到
溶液完全反应,铁粉全部溶解,并得到 铜,则参加反应的
铜,则参加反应的 与
与 的物质的量之比为
的物质的量之比为(5)等质量的铝分别与
 浓度均为
浓度均为 的盐酸和氢氧化钠溶液反应,生成气体体积比为
的盐酸和氢氧化钠溶液反应,生成气体体积比为 ,铝与氢氧化钠溶液反应的离子方程式:
,铝与氢氧化钠溶液反应的离子方程式:(6)将
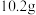 镁铝合金置于
镁铝合金置于 的盐酸中充分反应,无金属剩余,向反应后的溶液中加入
的盐酸中充分反应,无金属剩余,向反应后的溶液中加入 烧碱溶液,沉淀达到最大值,加入的烧碱的物质的量浓度为
烧碱溶液,沉淀达到最大值,加入的烧碱的物质的量浓度为 。
。
您最近一年使用:0次
【推荐3】已知 和
和 在常温下可快速反应生成氮气:
在常温下可快速反应生成氮气: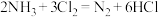 。当
。当 和
和 比例不同时,产物有差异。请回答:
比例不同时,产物有差异。请回答:
 若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则
若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则 和
和 的最佳体积比为
的最佳体积比为___________ 。
 体积为
体积为 的
的 和
和 的混合气体通过浓氨水后,体积变为
的混合气体通过浓氨水后,体积变为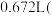 其中
其中 体积分数为
体积分数为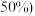 ,则原混合气体中
,则原混合气体中 的体积为
的体积为_____________ 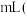 气体体积均为标准状况下测定
气体体积均为标准状况下测定 。
。
 有
有 和
和 的混合气体,其中
的混合气体,其中 的体积分数为x,将
的体积分数为x,将 该混合气体与1L氨气混合,讨论当x取不同范围的数值时,所得气体体积y与x的关系式
该混合气体与1L氨气混合,讨论当x取不同范围的数值时,所得气体体积y与x的关系式 气体体积均在相同状况下测定
气体体积均在相同状况下测定 。
。
 和
和 在常温下可快速反应生成氮气:
在常温下可快速反应生成氮气: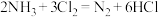 。当
。当 和
和 比例不同时,产物有差异。请回答:
比例不同时,产物有差异。请回答: 若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则
若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则 和
和 的最佳体积比为
的最佳体积比为 体积为
体积为 的
的 和
和 的混合气体通过浓氨水后,体积变为
的混合气体通过浓氨水后,体积变为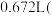 其中
其中 体积分数为
体积分数为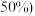 ,则原混合气体中
,则原混合气体中 的体积为
的体积为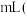 气体体积均为标准状况下测定
气体体积均为标准状况下测定 。
。 有
有 和
和 的混合气体,其中
的混合气体,其中 的体积分数为x,将
的体积分数为x,将 该混合气体与1L氨气混合,讨论当x取不同范围的数值时,所得气体体积y与x的关系式
该混合气体与1L氨气混合,讨论当x取不同范围的数值时,所得气体体积y与x的关系式 气体体积均在相同状况下测定
气体体积均在相同状况下测定 。
。| x的取值范围 | y与x的关系式 |
  |  |
 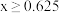 |  |
您最近一年使用:0次
【推荐1】氧化还原反应原理及物质的量的相关计算在生产、生活中应用广泛。
(1)某同学写出以下化学反应方程式(未配平):①NH3+NO→HNO2+H2O,②NO+HNO3→N2O3+H2O,③N2O4+H2O→HNO2+HNO3,其中一定不可能实现的是(填序号)_______ 。
(2)ClO2可用于污水的杀菌和饮用水的净化。KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为 ,此反应的离子方程式为
,此反应的离子方程式为_______ 。
(3)已知亚硝酸钠(NaNO2)可以与氯化铵(NH4Cl)反应生成氮气、氯化钠及其它产物,写出该反应的化学反应方程式_______ 。
(4)一定条件下,当溶液中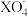 与H2O2物质的量比恰好为2:5时,溶液中
与H2O2物质的量比恰好为2:5时,溶液中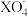 离子被还原为较低价态,则X元素的化合价变为
离子被还原为较低价态,则X元素的化合价变为_______ 。
(5)将不纯的NaOH样品2g(含少量Na2CO3和水),放入50mL2mol/L的盐酸中,充分反应后,溶液呈酸性,中和剩余的酸又用去40mLlmol/L的NaOH溶液。蒸发中和后的溶液,最终得到固体的质量为_______ 。
(6)臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压,放电管来制取臭氧:
①在臭氧发生装置中装入氧气100mL,经反应最后气体体积变为95mL(体积均在标准状况下测定),则混合气体的密度是_______ g/L(保留一位小数);
②实验室将氧气和臭氧的混合气体0.896L(标准状况),通入盛有20.0g铜粉的反应容器中,充分加热后,粉末的质量最终变为21.6g。则原混合气中臭氧的体积分数_______ 。
(1)某同学写出以下化学反应方程式(未配平):①NH3+NO→HNO2+H2O,②NO+HNO3→N2O3+H2O,③N2O4+H2O→HNO2+HNO3,其中一定不可能实现的是(填序号)
(2)ClO2可用于污水的杀菌和饮用水的净化。KClO3与SO2在强酸性溶液中反应可制得ClO2,SO2被氧化为
 ,此反应的离子方程式为
,此反应的离子方程式为(3)已知亚硝酸钠(NaNO2)可以与氯化铵(NH4Cl)反应生成氮气、氯化钠及其它产物,写出该反应的化学反应方程式
(4)一定条件下,当溶液中
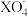 与H2O2物质的量比恰好为2:5时,溶液中
与H2O2物质的量比恰好为2:5时,溶液中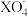 离子被还原为较低价态,则X元素的化合价变为
离子被还原为较低价态,则X元素的化合价变为(5)将不纯的NaOH样品2g(含少量Na2CO3和水),放入50mL2mol/L的盐酸中,充分反应后,溶液呈酸性,中和剩余的酸又用去40mLlmol/L的NaOH溶液。蒸发中和后的溶液,最终得到固体的质量为
(6)臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压,放电管来制取臭氧:
①在臭氧发生装置中装入氧气100mL,经反应最后气体体积变为95mL(体积均在标准状况下测定),则混合气体的密度是
②实验室将氧气和臭氧的混合气体0.896L(标准状况),通入盛有20.0g铜粉的反应容器中,充分加热后,粉末的质量最终变为21.6g。则原混合气中臭氧的体积分数
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐2】实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量铁铝合金与100mL某浓度的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入 的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。
的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。
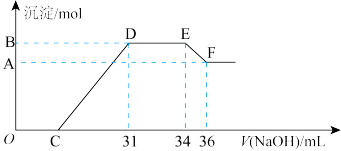
试回答:
(1)写出铁与该硝酸反应的离子方程式_______ ;
(2)合金中铁的质量为_______ g;
(3)原硝酸的物质的量浓度为_______  。
。
 的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。
的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。
试回答:
(1)写出铁与该硝酸反应的离子方程式
(2)合金中铁的质量为
(3)原硝酸的物质的量浓度为
 。
。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐3】Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是___________________ (填化学式),被2molFeSO4还原的过氧化钠为_________ mol
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:
、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:__________________________
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1molFeI2和2molFeBr2的溶液中通入2molCl2,此时被氧化的离子是____________ ,被氧化的离子的物质的量分别是_____________________________________________
(2)若向含amolFeI2和bmolFeBr2的溶液中通入cmolCl2,当I-、Fe2+被氧化时,c为_____________ (用含a、b的代数式表示)。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO
 、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:
、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1molFeI2和2molFeBr2的溶液中通入2molCl2,此时被氧化的离子是
(2)若向含amolFeI2和bmolFeBr2的溶液中通入cmolCl2,当I-、Fe2+被氧化时,c为
您最近一年使用:0次



