已知 和
和 在常温下可快速反应生成氮气:
在常温下可快速反应生成氮气: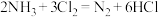 。当
。当 和
和 比例不同时,产物有差异。请回答:
比例不同时,产物有差异。请回答:
 若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则
若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则 和
和 的最佳体积比为
的最佳体积比为___________ 。
 体积为
体积为 的
的 和
和 的混合气体通过浓氨水后,体积变为
的混合气体通过浓氨水后,体积变为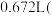 其中
其中 体积分数为
体积分数为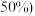 ,则原混合气体中
,则原混合气体中 的体积为
的体积为_____________ 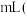 气体体积均为标准状况下测定
气体体积均为标准状况下测定 。
。
 有
有 和
和 的混合气体,其中
的混合气体,其中 的体积分数为x,将
的体积分数为x,将 该混合气体与1L氨气混合,讨论当x取不同范围的数值时,所得气体体积y与x的关系式
该混合气体与1L氨气混合,讨论当x取不同范围的数值时,所得气体体积y与x的关系式 气体体积均在相同状况下测定
气体体积均在相同状况下测定 。
。
 和
和 在常温下可快速反应生成氮气:
在常温下可快速反应生成氮气: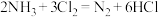 。当
。当 和
和 比例不同时,产物有差异。请回答:
比例不同时,产物有差异。请回答: 若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则
若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则 和
和 的最佳体积比为
的最佳体积比为 体积为
体积为 的
的 和
和 的混合气体通过浓氨水后,体积变为
的混合气体通过浓氨水后,体积变为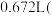 其中
其中 体积分数为
体积分数为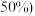 ,则原混合气体中
,则原混合气体中 的体积为
的体积为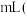 气体体积均为标准状况下测定
气体体积均为标准状况下测定 。
。 有
有 和
和 的混合气体,其中
的混合气体,其中 的体积分数为x,将
的体积分数为x,将 该混合气体与1L氨气混合,讨论当x取不同范围的数值时,所得气体体积y与x的关系式
该混合气体与1L氨气混合,讨论当x取不同范围的数值时,所得气体体积y与x的关系式 气体体积均在相同状况下测定
气体体积均在相同状况下测定 。
。| x的取值范围 | y与x的关系式 |
  |  |
 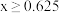 |  |
更新时间:2019-12-26 15:41:37
|
相似题推荐
计算题
|
较难
(0.4)
名校
【推荐1】Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是___________________ (填化学式),被2molFeSO4还原的过氧化钠为_________ mol
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:
、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:__________________________
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1molFeI2和2molFeBr2的溶液中通入2molCl2,此时被氧化的离子是____________ ,被氧化的离子的物质的量分别是_____________________________________________
(2)若向含amolFeI2和bmolFeBr2的溶液中通入cmolCl2,当I-、Fe2+被氧化时,c为_____________ (用含a、b的代数式表示)。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO
 、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:
、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1molFeI2和2molFeBr2的溶液中通入2molCl2,此时被氧化的离子是
(2)若向含amolFeI2和bmolFeBr2的溶液中通入cmolCl2,当I-、Fe2+被氧化时,c为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐2】(1)取300 mL 0.2 mol/L的 KI溶液与一定量的酸性 KMnO4 溶液恰好反应,生成等物质的量的 I2和 KIO3,则消耗 KMnO4的物质的量是________ mol。
(2)在 Fe(NO3)3 溶液中加入 Na2SO3 溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是___________________ ,又变为棕黄色的原因是(用离子方程式解释)________________________________________________ 。
(3)在 100 mLFeBr2 溶液中通入标准状况下3.36 L Cl2,溶液中有 1/4的 Br-被氧化成单质 Br2,则原 FeBr2溶液中 FeBr2 的物质的量浓度为________ mol/L。
(4)将Al、Al2O3和Al(OH)3的混合物恰好与NaOH溶液反应,反应后溶液中溶质的化学式__________________ 。向反应后的溶液中通入过量CO2,反应的离子方程式为__________________ 。
(5)三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式_______________________________________ ,反应中生成0.2 mol HNO3,转移的电子数目为_______________________ 。
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是_______ 。
(2)在 Fe(NO3)3 溶液中加入 Na2SO3 溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是
(3)在 100 mLFeBr2 溶液中通入标准状况下3.36 L Cl2,溶液中有 1/4的 Br-被氧化成单质 Br2,则原 FeBr2溶液中 FeBr2 的物质的量浓度为
(4)将Al、Al2O3和Al(OH)3的混合物恰好与NaOH溶液反应,反应后溶液中溶质的化学式
(5)三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐3】甲酸和乙酸都是重要的化工原料。移取20.00mL甲酸和乙酸的混合溶液,以0.1000mol·L-1NaOH标准溶液滴定至终点,消耗25.00mL。另取20.00mL上述混合溶液,加入50.00mL0.02500mol·L-1KMnO4强碱性溶液,反应完全后,调节至酸性,加入40.00mL0.02000mol·L-1Fe2+标准溶液,用上述KMnO4标准溶液滴定至终点,消耗24.00mL。
(1)计算混合溶液中甲酸和乙酸的总量_______ 。
(2)写出氧化还原滴定反应的化学方程式_______ 。
(3)计算混合酸溶液中甲酸和乙酸的浓度_______ 。
(1)计算混合溶液中甲酸和乙酸的总量
(2)写出氧化还原滴定反应的化学方程式
(3)计算混合酸溶液中甲酸和乙酸的浓度
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】工业甲醇的质量分数可以用下列方法测定:
①在稀H2SO4中甲醇被Cr2O72—氧化成CO2和H2O,
反应式为:CH3OH+Cr2O72—+8H+=CO2↑+2Cr3++6H2O;
②过量的Cr2O72—可用Fe2+与之完全反应:
___ Cr2O72—+___ Fe2++____ H+—_____ Cr3++____ Fe3++____ H2O
现有0.12 g工业甲醇,在H2SO4溶液中与25 mL 0.2 mol·L-1K2Cr2O7溶液反应,多余的K2Cr2O7再用1 mol·L—1FeSO4与其反应,结果用去FeSO4溶液9.6 mL。
(1)配平第②步的离子方程式。
(2)计算工业甲醇的质量分数_______________ 。
①在稀H2SO4中甲醇被Cr2O72—氧化成CO2和H2O,
反应式为:CH3OH+Cr2O72—+8H+=CO2↑+2Cr3++6H2O;
②过量的Cr2O72—可用Fe2+与之完全反应:
现有0.12 g工业甲醇,在H2SO4溶液中与25 mL 0.2 mol·L-1K2Cr2O7溶液反应,多余的K2Cr2O7再用1 mol·L—1FeSO4与其反应,结果用去FeSO4溶液9.6 mL。
(1)配平第②步的离子方程式。
(2)计算工业甲醇的质量分数
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】烟道气中的 NO 是主要的大气污染物之一,为了监测其含量,选用如下检测方法:将vL气样通入适量酸化的 H2O2 溶液中,恰好使 NO 完全被氧化成NO3-,加水稀释至 100.00mL。量取20.00mL该溶液,加入v1mLc1mol·L-1FeSO4标准溶液(过量),充分反应后,用c2 mol·L-1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗 v2mL。回答下列问题:
(1)NO被H2O2氧化为NO3-的离子方程式为:_____ 。
(2)滴定过程中发生下列反应:
3Fe2++NO3-+4H+=NO↑+3Fe3++2H2O
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
则气样中NO的物质的量为_______ mol。
(3)下列操作会使 NO 测定结果偏高的是_____
A.滴定管未用标准液润洗
B.锥形瓶洗净后还存留少量的水
C.滴定管滴定前读数正确,滴定后俯视读数
D.FeSO4 标准溶液部分变质
(1)NO被H2O2氧化为NO3-的离子方程式为:
(2)滴定过程中发生下列反应:
3Fe2++NO3-+4H+=NO↑+3Fe3++2H2O
Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
则气样中NO的物质的量为
(3)下列操作会使 NO 测定结果偏高的是
A.滴定管未用标准液润洗
B.锥形瓶洗净后还存留少量的水
C.滴定管滴定前读数正确,滴定后俯视读数
D.FeSO4 标准溶液部分变质
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】绿矾(FeSO4•7H2O)在化学合成上用作还原剂及催化剂,工业上常用废铁屑溶于一定浓度的硫酸溶液制备绿矾。
(1)98% 1.84g/cm3的浓硫酸在稀释过程中,密度下降,当稀释至50%时,密度为1.4g/cm3,50%的硫酸物质的量浓度为______ (保留两位小数),50%的硫酸与30%的硫酸等体积混合,混合酸的浓度为______ (填>、<、=)40%。
(2)实际生产用20%发烟硫酸(100克发烟硫酸含SO320克)配制稀硫酸,若用SO3•nH2O表示20%的发烟硫酸,则n=______ (保留两位小数)。
(3)某厂废水中含1.00×10﹣3mol/L的Cr2O72-,其毒性较大.某研究性学习小组为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4 (Cr的化合价为+3,Fe的化合价依次为+3、+2).欲使1L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4.理论上需要加入______ g FeSO4•7H2O。
(4)硫酸亚铁铵[(NH4)2SO4•FeSO4•6H2O](俗称莫尔盐),较绿矾稳定,在分析化学中常用来配制Fe2+的标准溶液,用此Fe2+的标准溶液可以测定剩余稀硝酸的量.现取8.64克Cu2S和CuS的混合物用200mL2mol/L稀硝酸溶液处理,发生反应如下:
10NO3﹣+3Cu2S+16H+→6Cu2++10NO↑+3SO42﹣+8H2O
8NO3﹣+3CuS+8H+→3Cu2++3 SO42﹣+8NO↑+4H2O
剩余的稀硝酸恰好与48mL 2mol/L (NH4)2Fe(SO4)2溶液完全反应.
已知:NO3﹣+3Fe2++4H+→NO↑+3Fe3++2H2O
试计算混合物中CuS的质量分数(保留两位小数)。______________
(1)98% 1.84g/cm3的浓硫酸在稀释过程中,密度下降,当稀释至50%时,密度为1.4g/cm3,50%的硫酸物质的量浓度为
(2)实际生产用20%发烟硫酸(100克发烟硫酸含SO320克)配制稀硫酸,若用SO3•nH2O表示20%的发烟硫酸,则n=
(3)某厂废水中含1.00×10﹣3mol/L的Cr2O72-,其毒性较大.某研究性学习小组为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4 (Cr的化合价为+3,Fe的化合价依次为+3、+2).欲使1L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4.理论上需要加入
(4)硫酸亚铁铵[(NH4)2SO4•FeSO4•6H2O](俗称莫尔盐),较绿矾稳定,在分析化学中常用来配制Fe2+的标准溶液,用此Fe2+的标准溶液可以测定剩余稀硝酸的量.现取8.64克Cu2S和CuS的混合物用200mL2mol/L稀硝酸溶液处理,发生反应如下:
10NO3﹣+3Cu2S+16H+→6Cu2++10NO↑+3SO42﹣+8H2O
8NO3﹣+3CuS+8H+→3Cu2++3 SO42﹣+8NO↑+4H2O
剩余的稀硝酸恰好与48mL 2mol/L (NH4)2Fe(SO4)2溶液完全反应.
已知:NO3﹣+3Fe2++4H+→NO↑+3Fe3++2H2O
试计算混合物中CuS的质量分数(保留两位小数)。
您最近一年使用:0次



