解题方法
1 . 某大学研究团队推出一种新型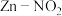 电池。该电池能有效地捕获
电池。该电池能有效地捕获 ,将其转化为
,将其转化为 ,再将产生的
,再将产生的 电解制氨,过程如图所示。下列说法正确的是
电解制氨,过程如图所示。下列说法正确的是
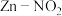 电池。该电池能有效地捕获
电池。该电池能有效地捕获 ,将其转化为
,将其转化为 ,再将产生的
,再将产生的 电解制氨,过程如图所示。下列说法正确的是
电解制氨,过程如图所示。下列说法正确的是
A. 电极的电势比 电极的电势比 电极的电势高 电极的电势高 |
B. 的空间结构为平面三角形 的空间结构为平面三角形 |
C. 极的电极反应为 极的电极反应为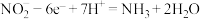 |
D.电路中转移0.2mol 时,理论上能得到1.12L 时,理论上能得到1.12L |
您最近一年使用:0次
解题方法
2 . 醛酮在酸或碱的催化下生成偕二醇的反应历程如下:
下列说法不正确的是
酸催化历程: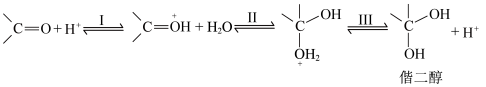
碱催化历程: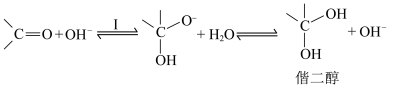
| 羰基化合物 |  |  |  |
| 平衡常数K | 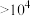 | 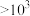 | 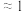 |
A.酸催化历程的步骤I中 与羰基中的O结合,增大了碳氧双键的极性 与羰基中的O结合,增大了碳氧双键的极性 |
B.对比酸和碱的催化历程可知,与羰基反应的活性: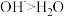 |
C.无论酸或碱催化,生成偕二醇的平衡常数: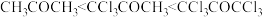 |
D.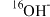 催化下, 催化下,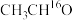 的 的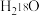 溶液中无法生成 溶液中无法生成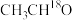 |
您最近一年使用:0次
名校
3 . 某化学兴趣小组在阴暗的地方用如图所示装置探究CH4与Cl2的反应,灯泡接通电源后,开始实验。下列说法错误的是

| A.软管内会发生取代反应,生成物可能有5种 |
| B.透明软管内气体颜色会逐渐变浅,透明软管的体积会缩小直至完全凹瘪 |
| C.软管内会有油状液滴产生 |
| D.充分反应后,打开K1,导管口可能会有白雾出现 |
您最近一年使用:0次
今日更新
|
223次组卷
|
2卷引用:河北省保定市定州市第二中学2023-2024学年高一下学期5月月考化学试题
4 . Au溶于食盐和硝酸混合液发生反应: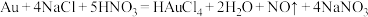 ,(已知:
,(已知: ),下列说法
),下列说法不正确 的是
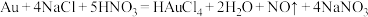 ,(已知:
,(已知: ),下列说法
),下列说法| A.Au是还原剂,HNO3是氧化剂 |
| B. HAuCl4是氧化产物,NO是还原产物 |
| C.Au消耗0.5mol得到1.5mol电子 |
| D.Au也能溶于王水(浓硝酸和浓盐酸体积比1∶3) |
您最近一年使用:0次
名校
解题方法
5 . 对于可逆反应 ,在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
,在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
 ,在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
,在不同条件下的化学反应速率如下,其中表示的反应速率最快的是A.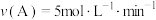 | B. |
C.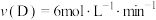 | D. |
您最近一年使用:0次
6 . 磷酸(H3PO4)、亚磷酸(H3PO3)和次磷酸(H3PO2)都是重要的化工产品。已知:1mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3mol、2mol、1mol。亚磷酸易溶于水和醇,加热到180℃时分解成磷酸和磷化氢 。经实验检测发现
。经实验检测发现 溶液显碱性。已知:25℃时
溶液显碱性。已知:25℃时 。常温下,用
。常温下,用 溶液滴定
溶液滴定 溶液的滴定曲线如图所示,下列说法正确的是
溶液的滴定曲线如图所示,下列说法正确的是
 。经实验检测发现
。经实验检测发现 溶液显碱性。已知:25℃时
溶液显碱性。已知:25℃时 。常温下,用
。常温下,用 溶液滴定
溶液滴定 溶液的滴定曲线如图所示,下列说法正确的是
溶液的滴定曲线如图所示,下列说法正确的是
A. 点加入氢氧化钠的体积 点加入氢氧化钠的体积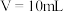 |
B.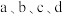 中, 中, 点水的电离程度最小 点水的电离程度最小 |
C. 点存在: 点存在: |
D. 点存在: 点存在: |
您最近一年使用:0次
名校
解题方法
7 . 硫酸是重要的化工原料,属于大宗化学品。下列说法正确的是
| A.S是第三周期第ⅣA族元素 |
B.工业上用稀硫酸吸收 制备硫酸 制备硫酸 |
| C.98%浓硫酸滴在pH试纸上,先变红后变白 |
| D.酸雨中含有硫酸和亚硫酸,露置一段时间酸性变强 |
您最近一年使用:0次
8 . 7下表是醋酸电离常数与温度的关系。下列说法不正确 的是
| 温度/℃ | 0 | 30 | 50 |
 | 1.65 | 1.75 | 1.63 |
A.醋酸在水中的电离方程式: |
| B.0.1mol/L醋酸中加水稀释,醋酸和水的电离程度均增加 |
| C.醋酸溶液升温中可能涉及共价键和氢键断裂、离子水合的过程 |
| D.0~30℃电离总过程是放热的,30~50℃电离总过程是吸热的 |
您最近一年使用:0次
9 . 设 为阿伏加德常数的值,下列说法
为阿伏加德常数的值,下列说法不正确 的是
 为阿伏加德常数的值,下列说法
为阿伏加德常数的值,下列说法A.78g  固体中含有的阴离子个数为 固体中含有的阴离子个数为 |
B.常温常压下,22.4L  气体含有的分子数大于 气体含有的分子数大于 |
C.32g硫在足量的氧气中充分燃烧转移的电子数为4 |
D.31g  中的共价键数目为1.5 中的共价键数目为1.5 |
您最近一年使用:0次
解题方法
10 . 一种新型短路膜电池分离 装置如下图所示。
装置如下图所示。
 装置如下图所示。
装置如下图所示。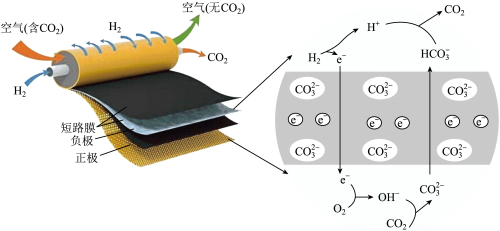
| A.短路膜既能传递阴离子,也能传递电子 |
B.电池工作过程中,正极 增大,工作结束后,短路膜中 增大,工作结束后,短路膜中 减小 减小 |
C.标准状况下,每分离出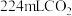 ,进出短路膜前后空气的体积差为 ,进出短路膜前后空气的体积差为 |
D.空气(含 )的流速越快, )的流速越快, 的去除率不一定越高 的去除率不一定越高 |
您最近一年使用:0次



