回答下列问题
(1)已知:
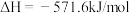

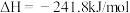
①则氢气的燃烧热
___________ ;
②计算

___________ ;
③计算1g氢气完全燃烧生成气态水时放出___________ kJ的热量。
(2)已知:①
 ;
;
②
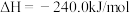 ;
;
③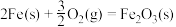
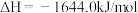 ;
;
则反应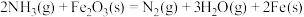

___________  。
。
(1)已知:

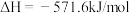

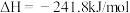
①则氢气的燃烧热

②计算


③计算1g氢气完全燃烧生成气态水时放出
(2)已知:①

 ;
;②

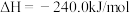 ;
;③
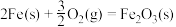
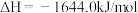 ;
;则反应
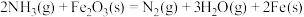

 。
。
更新时间:2024-05-01 20:26:41
|
【知识点】 盖斯定律与热化学方程式解读
相似题推荐
【推荐1】甲醇是人们开发和利用的一种新能源。已知:
①2H2(g)+O2(g)=2H2O(l) △H1=-571.8kJ· mol-1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ· mol-1
O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ· mol-1
(1)甲醇蒸汽完全燃烧的热化学方程式为_____________ 。
(2)反应②中的能量变化如下图所示,则△H2=______ (用E1和E2表示)。

(3)H2(g)的燃烧热为__________ kJ· mol-1。
(4)请你分析H2(g)作为能源比甲醇蒸汽作为能源的优点:__________________ (写出一点)
①2H2(g)+O2(g)=2H2O(l) △H1=-571.8kJ· mol-1
②CH3OH(g)+
 O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ· mol-1
O2(g)=CO2(g)+2H2(g) △H=-192.9 kJ· mol-1(1)甲醇蒸汽完全燃烧的热化学方程式为
(2)反应②中的能量变化如下图所示,则△H2=

(3)H2(g)的燃烧热为
(4)请你分析H2(g)作为能源比甲醇蒸汽作为能源的优点:
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】采用科学技术减少氮氧化物等物质的排放可促进社会主义生态文明建设。
用CH4催化还原氮氧化物的相关热化学方程式如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(1)∆H=-662kJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(l)∆H=-1248kJ•mol-1
反应CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l)∆H=_____ kJ•mol-1
用CH4催化还原氮氧化物的相关热化学方程式如下:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(1)∆H=-662kJ•mol-1
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(l)∆H=-1248kJ•mol-1
反应CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l)∆H=
您最近一年使用:0次



